Язвенная болезнь
Язвенная болезнь (ЯБ) представляет собой хроническое рецидивирующее заболевание, протекающее с чередованием периодов обострения и ремиссии, ведущим проявлением которого служит образование дефекта (язвы) в стенке желудка и двенадцатиперстной кишки.
Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
Язва желудка (К25)
К25.0 — острая с кровотечением
К25.1 – острая с прободением
К25.2 – острая с кровотечением и прободением
К25.3 – острая без кровотечения и прободения
К25.4 — хроническая или неуточненная с кровотечением
К25.5 – хроническая или неуточненная с прободением
К25.6 – хроническая или неуточненная с кровотечением и прободением
К25.7 – хроническая без кровотечения и прободения
К25.9. – не уточненная как острая или хроническая без кровотечения и прободения
Язва двенадцатиперстной кишки (К26)
К26.0 – острая с кровотечением
К26.1 – острая с прободением
К26.2– острая с кровотечением и прободением
К26.3 – острая без кровотечения и прободения
К26.4 — хроническая или неуточненная с кровотечением
К26.5 – хроническая или неуточненная с прободением
К26.6 – хроническая или неуточненная с кровотечением и прободением
К26.7 – хроническая без кровотечения и прободения
К26.9. – не уточненная как острая или хроническая без кровотечения и прободения
Облачная МИС «МедЭлемент»

Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
— 800 RUB / 5500 KZT / 27 BYN — 1 рабочее место в месяц
Облачная МИС «МедЭлемент»

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место — 800 RUB / 5500 KZT / 27 BYN в месяц
+7 938 489 4483 / +7 707 707 0716 / + 375 29 602 2356 / office@medelement.com
Мне интересно! Свяжитесь со мной
Классификация
Классификация заболевания или состояния (группы заболеваний или состояний)
Общепринятой классификации ЯБ не существует. Прежде всего, в зависимости от наличия или отсутствия инфекции Н. pylori выделяют ЯБ, ассоциированную и не ассоциированную с инфекцией Н. pylori. Последнюю форму иногда также называют идиопатической. Также различают ЯБ как самостоятельное заболевание (эссенциальная язвенная болезнь) и симптоматические язвы желудка и двенадцатиперстной кишки (лекарственные, «стрессовые», при эндокринной патологии, при других хронических заболеваниях внутренних органов), которые возникают на фоне других заболеваний и по механизмам своего развития связаны с особыми этиологическими и патогенетическими факторами.
В зависимости от локализации выделяют язвы желудка (кардиального и субкардиального отделов, тела желудка, антрального отдела, пилорического канала), язвы двенадцатиперстной кишки (луковицы, постбульбарного отдела, а также сочетанные язвы желудка и двенадцатиперстной кишки. При этом язвы могут располагаться на малой или большой кривизне, передней и задней стенках желудка и двенадцатиперстной кишки.
По числу язвенных поражений различают одиночные и множественные язвы, а в зависимости от размеров язвенного дефекта – язвы малых (до 0,5 см в диаметре) и средних (0,6-1,9 см в диаметре) размеров, большие (2,0 — 3,0 см в диаметре) и гигантские (свыше 3,0 см в диаметре) язвы.
В диагнозе отмечаются стадия течения заболевания: обострения, заживления, рубцевания (эндоскопически подтвержденная стадия «красного» и «белого» рубца) и ремиссии, а также имеющаяся рубцово-язвенная деформация желудка и/или двенадцатиперстной кишки.
При формулировке диагноза указывается наличие осложнений ЯБ (в том числе, и анамнестических): кровотечения, прободения, пенетрации, рубцово-язвенного стеноза, а также характер оперативных вмешательств, если они проводились.
Этиология и патогенез
Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Согласно современным представлениям, патогенез ЯБ в общем виде сводится к нарушению равновесия между факторами кислотно-пептической агрессии желудочного содержимого и элементами защиты слизистой оболочки желудка и двенадцатиперстной кишки [1].
Агрессивное звено язвообразования включает в себя увеличение массы обкладочных клеток (часто наследственно обусловленное), гиперпродукцию гастрина, нарушение нервной и гуморальной регуляции желудочного кислотовыделения, повышение выработки пепсиногена и пепсина, нарушение гастродуоденальной моторики (задержка или, наоборот, ускорение эвакуации из желудка, обсеменение слизистой оболочки желудка микроорганизмами Helicobacter pylori (H. pylori).
Ослабление защитных свойств слизистой оболочки желудка и двенадцатиперстной кишки может возникнуть в результате снижения выработки и нарушения качественного состава желудочной слизи, уменьшения секреции бикарбонатов, снижения регенераторной активности эпителиальных клеток, ухудшения кровоснабжения слизистой оболочки желудка, уменьшения содержания простагландинов в стенке желудка (например, при приеме нестероидных противовоспалительных препаратов (НПВП).
Решающая роль в развитии ЯБ в настоящее время отводится микроорганизмам H. pylori, обнаруженным в 1983 г. австралийскими учеными Б. Маршаллом (B. Marshall) и Дж.Уорреном (J. Warren).
Спектр неблагоприятного влияния Н. pylori на слизистую оболочку желудка и двенадцатиперстной кишки достаточно многообразен. Эти бактерии вырабатывают целый ряд ферментов (уреаза, протеазы, фосфолипазы), повреждающих защитный барьер слизистой оболочки, а также различные цитотоксины. Наиболее патогенными являются VacA-штамм Н. pylori, продуцирующий вакуолизирующий цитотоксин, приводящий к образованию цитоплазматических вакуолей и гибели эпителиальных клеток, и CagA-штамм, экспрессирующий ген, ассоциированный с цитотоксином. Н. pylori способствуют высвобождению в слизистой оболочке желудка интерлейкинов, лизосомальных энзимов, фактора некроза опухолей, что вызывает развитие воспалительных процессов в слизистой оболочке желудка.
Обсеменение слизистой оболочки желудка Н. pylori сопровождается развитием поверхностного антрального гастрита и дуоденита и ведет к повышению уровня гастрина с последующим усилением секреции соляной кислоты. Избыточное количество соляной кислоты, попадая в просвет двенадцатиперстной кишки, в условиях относительного дефицита панкреатических бикарбонатов способствует прогрессированию дуоденита и, кроме того, обусловливает появление в двенадцатиперстной кишке участков желудочной метаплазии (перестройки эпителия дуоденальной слизистой оболочки по желудочному типу), которые быстро заселяются Н. pylori. В дальнейшем при неблагоприятном течении, особенно при наличии дополнительных этиологических факторов (наследственная предрасположенность, 0(I) группа крови, курение, нервно-психические стрессы и др.) в участках метаплазированной слизистой оболочки формируется язвенный дефект.
Ассоциированными с Н. pylori оказываются около 80% язв двенадцатиперстной кишки и 60% язв желудка [2]. Н. pylori-негативные язвы чаще всего бывают обусловлены приемом НПВП.
Эпидемиология
Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Показано, что 11 — 14% мужчин и 8 — 11% женщин в течение своей жизни могут заболеть ЯБ [3]. В США ежегодно выявляют 500000 пациентов с впервые обнаруженной ЯБ и более 4 млн. пациентов с рецидивами заболевания [2, 4]. ЯБ с локализацией в двенадцатиперстной кишке встречается в 4 раза чаще, чем ЯБ с локализацией в желудке. Среди пациентов с дуоденальными язвами мужчины преобладают над женщинами, тогда как среди пациентов с язвами желудка соотношение мужчин и женщин оказывается примерно одинаковым [5].
В последние годы отмечена тенденция к снижению госпитализации пациентов с неосложненными формами ЯБ как в зарубежных странах [6], так и в России. Анализ частоты и распространенности ЯБ в Российской Федерации, по статистическим данным Министерства здравоохранения РФ, за период с 2006 по 2017 г. заболеваемость ЯБ снизилась со 128,7 до 79,5 на 100 000 населения [7, 8]. В то же время во всем мире отмечено увеличение частоты осложнений ЯБ (кровотечений, перфорации), что обусловливается растущим приемом НПВП [6]. В Великобритании от осложнений язвенных поражений желудка и двенадцатиперстной кишки, связанных с приемом НПВП, ежегодно погибает более 2000 пациентов, в США – более 16500 пациентов [9].
В настоящее время во всем мире наметилась тенденция к снижению числа пациентов с осложненными формами течения язвенной болезни, во многом благодаря эффективности современных схем противоязвенной терапии, повышению доступности эндоскопической диагностики и активному использованию скрининговых тестов для уточнения наличия Н. pylori. Согласно докладу главного хирурга МЗ РФ от 25 октября 2018 г., в России с 2000 по 2017 год существует тенденция к снижению абсолютного числа пациентов с перфоративной язвой желудка и двенадцатиперстной кишки (с 37,6 до 19,1 тыс. чел), при этом увеличивается доля поздних госпитализации (спустя 24 часа – с 13,7% до 23,4%) и наблюдается рост послеоперационной летальности. Абсолютное число пациентов с желудочно-кишечными кровотечениями, в том числе язвенной этиологии, за анализируемый период времени также уменьшилось, однако послеоперационная летальность снизилась незначительно. Аналогичная ситуация отмечена группой японских ученых, указавших на снижение значимости наличия Н. pylori для пациентов с язвенными кровотечениями [10].
Клиническая картина
Cимптомы, течение
Клиническая картина заболевания или состояния (группы заболеваний или состояний)
Ведущим симптомом обострения ЯБ являются боли в подложечной области, которые могут иррадиировать в левую половину грудной клетки и левую лопатку, грудной или поясничный отдел позвоночника, Боли возникают сразу после приема пищи (при язвах кардиального и субкардиального отделов желудка), через полчаса-час после еды (при язвах тела желудка). При язвах пилорического канала и луковицы двенадцатиперстной кишки обычно наблюдаются поздние боли (через 2-3 часа после еды), «голодные» боли, возникающие натощак и проходящие после приема пищи, а также ночные боли, Боли проходят после приема антисекреторных и антацидных препаратов [5].
При обострении ЯБ часто встречаются также отрыжка кислым, тошнота, запоры. Рвота кислым желудочным содержимым, приносящая облегчение и потому вызываемая пациентами искусственно, всегда считалась признаком ЯБ, однако, в настоящее время она встречается сравнительно редко. При обострении заболевания нередко отмечается похудание, поскольку, несмотря на сохраненный, а иногда даже повышенный аппетит, пациенты ограничивают себя в еде, опасаясь усиления болей.
Клинические симптомы, наблюдаемые при обострении язвенной болезни, не являются патогномоничными и могут встречаться при других заболеваниях (например, хроническом гастрите и дуодените с синдромом функциональной диспепсии), поэтому диагноз ЯБ должен обязательно подтверждаться инструментальными методами исследования.
В период обострения ЯБ при объективном исследовании часто удается выявить болезненность в эпигастральной области при пальпации, сочетающуюся с умеренной резистентностью мышц передней брюшной стенки. Также может обнаруживаться локальная перкуторная болезненность в этой же области (симптом Менделя). Однако эти признаки не являются строго специфичными для обострения ЯБ.
Типичными для ЯБ являются сезонные (весной и осенью) периоды усиления болей и диспепсических симптомов.
В неосложненных случаях ЯБ протекает обычно с чередованием периодов обострения (продолжительностью от 3-4 до 6-8 недель) и ремиссии (длительностью от нескольких недель до многих лет). Под влиянием неблагоприятных факторов (например, таких, как физическое перенапряжение, прием НПВП и/или препаратов, снижающих свертываемость крови, злоупотребление алкоголем) возможно развитие осложнений. К ним относятся кровотечение, перфорация и пенетрация язвы, формирование рубцово-язвенного стеноза, малигнизация язвы).
Язвенное кровотечение наблюдается у 15-20% пациентов с ЯБ. Факторами риска его возникновения служат прием ацетилсалициловой кислоты и НПВП, инфекция Н. pylori и размеры язв >1 cм [6]. Язвенное кровотечение проявляется рвотой содержимым типа «кофейной гущи» (гематемезис) или черным дегтеобразным стулом (мелена). При массивном кровотечении и невысокой секреции соляной кислоты, а также локализации язвы в кардиальном отделе желудка в рвотных массах может отмечаться примесь неизмененной крови. Иногда на первое место в клинической картине язвенного кровотечения выступают общие жалобы (слабость, потеря сознания, снижение артериального давления, тахикардия), тогда как мелена может появиться лишь спустя несколько часов.
Перфорация (прободение) язвы встречается у 5 — 15% пациентов с ЯБ, чаще у мужчин. К ее развитию предрасполагают физическое перенапряжение, прием алкоголя, переедание. Иногда перфорация возникает внезапно, на фоне бессимптомного («немого») течения ЯБ. Перфорация язвы клинически манифестируется острейшими («кинжальными») болями в подложечной области, развитием коллаптоидного состояния. При обследовании пациента обнаруживаются «доскообразное» напряжение мышц передней брюшной стенки и резкая болезненность при пальпации живота, положительный симптом Щеткина-Блюмберга. В дальнейшем, иногда после периода мнимого улучшения, прогрессирует картина разлитого перитонита.
Под пенетрацией понимают проникновение язвы желудка или двенадцатиперстной кишки в окружающие ткани: поджелудочную железу, малый сальник, желчный пузырь и общий желчный проток. При пенетрации язвы возникают упорные боли, которые теряют прежнюю связь с приемом пищи, повышается температура тела, в анализах крови выявляется повышение СОЭ. Наличие пенетрации язвы подтверждается рентгенологически и эндоскопически.
Стеноз привратника формируется обычно после рубцевания язв, расположенных в пилорическом канале или начальной части двенадцатиперстной кишки. Нередко развитию данного осложнения способствует операция ушивания прободной язвы данной области. Наиболее характерными клиническими симптомами стеноза привратника являются рвота пищей, съеденной накануне, а также отрыжка с запахом сероводорода. При пальпации живота в подложечной области можно выявить «поздний шум плеска» (симптом Василенко), у худых пациентов становится иногда видимой перистальтика желудка. При декомпенсированном стенозе привратника может прогрессировать истощение пациентов, присоединяются электролитные нарушения.
Малигнизация (озлокачествление) доброкачественной язвы желудка является не таким частым осложнением, как считалось раньше. За малигнизацию язвы нередко ошибочно принимаются случаи своевременно не распознанного инфильтративно-язвенного рака желудка. Диагностика малигнизации язвы не всегда оказывается простой. Клинически иногда удается отметить изменение характера течения ЯБ с утратой периодичности и сезонности обострений. В анализах крови обнаруживаются анемия, повышение СОЭ. Окончательное заключение ставится при гистологическом исследовании биоптатов, взятых из различных участков язвы.
Определенные особенности клинической картины присущи симптоматическим язвам, возникающим на фоне других заболеваний или при приеме лекарственных препаратов.
Так, к стрессовым гастродуоденальным язвам относят острые, обычно множественные язвы желудка и двенадцатиперстной кишки, возникающие при распространенных ожогах (язвы Курлинга), после черепно-мозговых травм и нейрохирургических операций (язвы Кушинга), после обширных полостных операций, особенно связанных с трансплантацией органов, при остром инфаркте миокарда, у пациентов с терминальной стадией хронической почечной и печеночной недостаточности и других критических состояниях. Стрессовые язвы обычно бывают острыми, множественными, часто протекают малосимптомно, отличаются наклонностью к желудочно-кишечным кровотечениям и характеризуются высокой летальностью, обусловленной часто тяжелым течением фонового заболевания.
Среди лекарственных язв желудка и двенадцатиперстной кишки наибольшее значение имеют острые эрозивно-язвенные поражения, связанные с приемом НПВП (НПВП-гастропатия), блокирующих фермент циклооксигеназу-1, отвечающий за синтез простагландинов в стенке желудка. Гастродуоденальные язвы возникают у 20 — 25% пациентов, длительно принимающих НПВП, эрозивные поражения — более чем у 50% пациентов. К факторам риска их развития относятся пожилой возраст пациентов, наличие в анамнезе ЯБ, сопутствующие заболевания сердечно-сосудистой системы и печени, высокая доза НПВП, одновременный прием антикоагулянтов.
Гастродуоденальные язвы и эрозии, обусловленные приемом НПВП, также часто имеют множественный характер, нередко протекают малосимптомно и манифестируются внезапными желудочно-кишечными кровотечениями (меленой или рвотой содержимым типа «кофейной гущи»). Риск их развития у таких пациентов возрастает в 4-5 раз (11)
Диагностика
Диагностика
Критерии установления диагноза заболевания/состояния:
Диагноз язвенной болезни устанавливается на основании
1. анамнестических данных (характерные жалобы, выявление язвенной болезни прежде)
2. физикального обследования (обнаружение болезненности и резистентности мыщц брюшной стенки при пальпации)
3) инструментального обследования (обнаружение язвенного дефекта при эндоскопическом и рентгенологическом исследовании желудка и двенадцатиперстной кишки)
Жалобы и анамнез
Характерные для пациентов с ЯБ жалобы и данные анамнеза указаны в подразделе Клиническая картина.
Физикальное обследование
Характерные для пациентов с ЯБ данные физикального обследования приведены в подразделе Клиническая картина.
Лабораторные диагностические исследования
- Всем пациентам с ЯБ с целью исключения анемии как следствия скрытых язвенных кровотечений рекомендуется выполнение общего (клинического) анализа крови с определением уровня гемоглобина и оценкой гематокрита [12]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: Клинический анализ крови при неосложненном течении ЯБ чаще всего остается без существенных изменений, но может обнаруживаться и анемия, свидетельствующая о явных или скрытых кровотечениях.
- Всем пациентам с ЯБ с целью исключения скрытых язвенных кровотечений рекомендуется проведение исследования кала на скрытую кровь [13].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
Комментарии: Определенное место в диагностике обострений ЯБ занимает анализ кала на скрытую кровь. При интерпретации его результатов необходимо помнить, что положительная реакция кала на скрытую кровь встречается и при многих других заболеваниях, что требует их обязательного исключения.
- У пациентов с рефрактерным течением язвенной болезни c целью исключения синдрома Золлингера-Эллисона рекомендуется исследование уровня гастрина сыворотки крови [22].
Уровень убедительности рекомендаций — С (уровень достоверности доказательств – 5 )
Комментарии: Патогенез гастродуоденальных язв при синдроме Золлингера-Эллисона связан с резкой гиперсекрецией соляной кислоты в результате наличия у пациентов гастринпродуцирующей опухоли (чаще всего в поджелудочной железе). Эти язвы обычно бывают множественными, локализуются не только в желудке и двенадцатиперстной кишке, но и в тощей кишке, а иногда и пищеводе, протекают с выраженным болевым синдромом, упорной диареей. При обследовании таких пациентов отмечается резко повышенный уровень желудочного кислотовыделения (особенно в базальных условиях), определяется увеличенное содержание сывороточного гастрина (в 3-4 раза по сравнению с нормой). В распознавании синдрома Золлингера-Эллисона помогают провокационные тесты (с секретином, глюкагоном), ультразвуковое исследование и КТ поджелудочной железы, эндоскопическое ультразвуковое исследование.
Инструментальные диагностические исследования
- Всем пациентам с подозрением на ЯБ, при отсутствии противопоказаний, с целью подтверждения диагноза рекомендуется проведение эзофагогастродуоденоскопии (ЭГДС) [2].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Плановое эндоскопическое исследование подтверждает наличие язвенного дефекта, уточняет его локализацию, форму, размеры, глубину, состояние дна и краев язвы, позволяет выявить признаки пенетрации, рубцовой деформации и стенозирования просвета органа. Плановое эндоскопическое исследование дает возможность обнаружить другие сопутствующие изменения слизистой оболочки и определить нарушения гастродуоденальной моторики. Для оценки стадии язвенного процесса (обострение, заживление, рубцевание) целесообразно использовать общепринятую классификации Sakita и Miwa.

При локализации язвы в желудке практически во всех случаях рекомендуется проводить множественную щипцовую биопсию из краев язвенного дефекта с последующим патолого-анатомическим исследованием биопсийного материала, позволяющим исключить злокачественный характер язвенного поражения.
При локализации язвы в двенадцатиперстной кишке выполнение биопсии из краёв язвенного дефекта обычно не рекомендуется, так как подобные язвы крайне редко бывают злокачественными. Доброкачественные язвы двенадцатиперстной кишки следует дифференцировать с изъязвленными формами нейроэндокринных и субэпителиальных опухолей, а также с прорастанием в двенадцатиперстную кишку опухоли соседних органов, чаще всего — поджелудочной железы. В этих случаях выполнение биопсии безусловно необходимо.
Пациентам с язвой желудка рекомендуется выполнить контрольное эндоскопическое исследование с повторным взятием множественной щипцовой биопсии по окончании курса консервативного лечения. Это в первую очередь, касается пациентов, у которых сохраняются симптомы язвенной болезни, несмотря на соответствующий курс медикаментозной терапии, либо этиология язвы остается недостаточно ясной.
Пациентам с язвой двенадцатиперстной кишки рекомендуется выполнить контрольное эндоскопическое исследование в тех случаях, если сохраняется отчетливая клиническая симптоматика, несмотря на проведенное лечение, для исключения рефрактерной язвенной болезни и непептической этиологии язвы.
- Пациентам с подозрением на ЯБ, которым невозможно выполнение эндоскопического исследования, с целью подтверждения диагноза рекомендуется проведение рентгенографии желудка и двенадцатиперстной кишки [55].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
Комментарии: При рентгенологическом исследовании обнаруживается прямой признак ЯБ – «ниша» на контуре или на рельефе слизистой оболочки и косвенные признаки заболевания (местный циркулярный спазм мышечных волокон на противоположной по отношению к язве стенке желудка в виде «указующего перста», конвергенция складок слизистой оболочки к «нише», рубцово-язвенная деформация желудка и луковицы двенадцатиперстной кишки, гиперсекреция натощак, нарушения гастродуоденальной моторики.
В настоящее время к рентгенологическому исследованию с целью диагностики ЯБ прибегают не столь часто, как раньше. Его применяют в тех случаях, когда по каким-то причинам (например, наличие противопоказаний) не удается провести эндоскопическое исследование, когда с целью дифференциального диагноза с инфильтративно-язвенной формой рака необходимо оценить перистальтику стенки желудка, когда нужно оценить характер эвакуации из желудка.
- Пациентам с подозрением на перфорацию язвы с целью ее подтверждения рекомендуется проведение компьютерной томографии органов брюшной полости [14, 15, 16, 17, 18].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4)
Комментарии: Данный метод позволяет определить наличие свободного газа в брюшной полости, объем и характер выпота, локализовать патологические изменения, в том числе определить расположение перфорационного отверстия.
- У пациентов с подозрением на перфорацию или пенетрацию язвы, при невозможности проведения КТ, с целью диагностики данных осложнений рекомендуется выполнение УЗИ и обзорной рентгенографии органов брюшной полости [18, 19].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4)
Комментарии: Важным критерием сохранения жизни пациента и успеха в лечении перфоративной язвы желудка и/или двенадцатиперстной кишки является предоперационный срок — время от начала заболевания до момента выполнения операции. Длительный диагностический поиск может привести к ухудшению состояния пациента с последующим неблагоприятным прогнозом. Только при отсутствии в лечебном учреждении КТ возможно выполнение УЗИ и рентгенографии брюшной полости для диагностики перфорации язвы. Необходимо помнить, что чувствительность и специфичность этих методов ниже таковых по сравнению с КТ, а результат во многом зависит от квалификации специалиста по ультразвуковой диагностике.
Иные диагностические исследования
- Всем пациентам с ЯБ с целью определения показаний к эрадикационной терапии рекомендуется проведение тестирования на наличие инфекции Н. рylori с помощью С-дыхательного уреазного теста или определения антигена H.pylori в кале, а при одновременном проведении ЭГДС — с помощью быстрого уреазного теста. [20, 21].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
Комментарии: В соответствии с рекомендациями согласительного совещания «Маастрихт-V» (2016) [20] наиболее оптимальными тестами первичной диагностики инфекции H. pylori служат 13 С-дыхательный уреазный тест и определение антигена H. pylori в кале. Так, согласно оследнему Кокрейновскому обзору и мета-анализу, чувствительность 13 С-дыхательного уреазного теста составляет 94% (95% ДИ: 0,89 — 0,97), а определение антигена H. pylori в кале – 83% (95% ДИ: 0,73 — 0,90) при фиксированной специфичности в 90% [21].
Если пациентам одновременно проводится ЭГДС, то методом первичной диагностики может быть быстрый уреазный тест. При использовании эндоскопических методов диагностики Н.pylori берут, как минимум, 2 биоптата из тела желудка и 1 биоптат из антрального отдела. Серологический метод выявления антител к Н. pylori может применяться для первичной диагностики инфекции H. pylori, однако, только в том случае, если определяемые антитела относятся к классу IgG. Микробиологический (бактериологический) метод применяется в настоящее время для определения индивидуальной чувствительности H. pylori к антибиотикам в случаях неэффективности лечения.
Для контроля эрадикации, который проводят через 4-6 недель после окончания эрадикационной терапии, лучше всего применять 13 С-уреазный дыхательный тест или определение антигена Н.pylori в кале. Во избежание ложноотрицательных результатов прием ингибиторов протонного насоса (ИПН) необходимо прекратить за 2 недели до предполагаемого контрольного исследования. Кроме того, отрицательный результат исследования на инфекцию Н. pylori должен быть обязательно подтвержден другим методом диагностики.
- Пациентам с язвенными кровотечениями при определении у них инфицированности H.pylori рекомендуется проведение С-уреазного дыхательного теста в связи с низкой чувствительностью быстрого уреазного теста и гистологического патолого-анатомического исследованиям [51].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии: Мета-анализ работ, посвященных применению различных методов тестирования на наличие инфекции H.pylori у пациентов с язвенными кровотечениями, показал низкую чувствительность быстрого уреазного теста и патолого-анатомического исследованияа. Наиболее высокая точность дагностики инфекции H.pylori у пациентов с язвенными кровотечениями была отмечена при применении 13С-уреазного дыхательного теста [51].
Лечение
Лечение
Лечение ЯБ должно быть комплексным и включать в себя не только назначение лекарственных препаратов, но и проведение широкого круга различных мероприятий: диетическое питание, прекращение курения и злоупотребления алкоголем, отказ от приема препаратов, обладающих ульцерогенным действием, нормализацию режима труда и отдыха, санаторно-курортное лечение.
Пациенты с неосложненным течением ЯБ подлежат консервативному лечению. В большинстве случаев оно проводится амбулаторно. Однако при выраженном болевом синдроме, высоком риске развитии осложнений (например, большие и гигантские размеры язв), необходимости дообследования с целью верификации диагноза (например, при неясном характер язвенного поражения желудка), тяжелых сопутствующих заболеваниях целесообразна госпитализация пациентов.
1. Диетотерапия
- Всем пациентам с ЯБ с целью ускорения заживления язв рекомендуется диетотерапия [23].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Основные принципы диетического питания пациентов с язвенной болезнью, выработанные много лет назад, сохраняют свою актуальность и в настоящее время. Остаются в силе рекомендации частого (5-6 раз в сутки), дробного питания, соответствующие правилу: “шесть маленьких приемов пищи лучше, чем три больших”, механического, термического и химического щажения. Из пищевого рациона необходимо исключить продукты, раздражающие слизистую оболочку желудка и возбуждающие секрецию соляной кислоты: крепкие мясные и рыбные бульоны, жареную и наперченную пищу, копчености и консервы, приправы и специи (лук, чеснок, перец, горчицу), соления и маринады, газированные фруктовые воды, пиво, белое сухое вино, шампанское, кофе, цитрусовые.
Следует отдавать предпочтение продуктам, обладающим выраженными буферными свойствами (т.е. способностью связывать и нейтрализовывать соляную кислоту). К ним относятся мясо и рыба (отварные или приготовленные на пару), яйца, молоко и молочные продукты). Разрешаются также макаронные изделия, черствый белый хлеб, сухой бисквит и сухое печенье, молочные и вегетарианские супы. Овощи (картофель, морковь, кабачки, цветная капуста) можно готовить тушеными или в виде пюре и паровых суфле. В пищевой рацион можно включать каши, кисели из сладких сортов ягод, муссы, желе, сырые тертые и печеные яблоки, какао с молоком, некрепкий чай.
Нужно помнить и о таких простых, но в то же время важных рекомендациях, как необходимость принимать пищу в спокойной обстановке, не спеша, сидя, тщательно прожевывать пищу. Это способствует лучшему пропитыванию пищи слюной, буферные возможности которой являются достаточно выраженными.
2. Консервативное лечение
- Пациентам с обострением ЯБ с целью достижения заживления язв рекомендуется проведение антисекреторной терапии ингибиторами протонного насоса (ИПН) течение 4-6 недель [2, 3].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: В 1990 г. W. Burget и соавт. [24] опубликовали данные мета-анализа 300 работ, на основании которого пришли к заключению, что язвы желудка и двенадцатиперстной кишки рубцуются почти во всех случаях, если в течение суток удается поддерживать рН внутрижелудочного содержимого> 3 около 18 часов в сутки. В последующем все работы, посвященные применению антисекреторных препаратов, содержат в себе ссылку на эти данные, получившие название «правила Бурже (Burget)». С учетом указанного правила в качестве базисной противоязвенной терапии в настоящее время могут рассматриваться только антациды, блокаторы Н2-гистаминовых рецепторов (Н -блокаторы) и ИПН. Согласно одному из последних мета-анализов, Н -блокаторы и ИПН достовернее эффективнее плацебо в рамках достижения рубцевания язвенного дефекта (ОШ 3,49, 95% ДИ: 3,28-3,72; p <0,0001) и снижения риска повторного кровотечения при осложнённом течении заболевания (ОШ 0,68, 95% ДИ: 0,60-0,78; p <0,0001) [25].
Лишь препараты этой группы могут выполнить после их приема условия правила продолжительности повышения рН в желудке, необходимой для заживления гастродуоденальных язв. В настоящее время ИПН являются средством базисной терапии обострения ЯБ. Они назначаются с целью купирования болевого синдрома и диспепсических расстройств, а также для достижения рубцевания язвенного дефекта в возможно более короткие сроки. Многочисленные рандомизированные сравнительные исследования (включая мета-аналитические) свидетельствовали о значительно более высокой эффективности ИПН по сравнению с Н -блокаторами в устранении клинических симптомов и достижении рубцевания язв [26, 27]. Недавний мета-анализ продемонстрировал, что ИПН практически в 1,5 раза эффективнее Н -блокаторов в рамках эпителизации язвенного дефекта (ОШ 5,22, 95% ДИ: 4,00-6,80 против ОШ 3,80, 95% ДИ: 3,44-4,20; p <0,0001) [25].
В настоящее время существует протокол фармакотерапии ЯБ, который предусматривает назначение выбранного препарата в суточной дозе: омепразола** — в дозе 20 мг, лансопразола – в дозе 30 мг, пантопразола – в дозе 40 мг, рабепразола – в дозе 20 мг, эзомепразола** – в дозе 20 мг. Продолжительность лечения определяется результатами эндоскопического контроля, который проводится с интервалами 2-4 недели. Базисная антисекреторная терапия с применением ИПН служит основным методом лечения идиопатических гастродуоденальных язв.
При применении ИПН, метаболизирующихся системой цитохрома Р450, могут остро вставать вопросы конкурентного лекарственного взаимодействия с препаратами, метаболизм которых также осуществляется с помощью указанной системы. Среди всех ИПН самое низкое сродство к системе цитохрома Р450 проявляют пантопразол и рабепразол, основной метаболизм которых осуществляется без участия данной ферментной системы.
- При неэффективности ИПН или наличии противопоказаний к их применению пациентам с обострением ЯБ с целью достижения заживления язв рекомендуется назначение в течение 4-6 недель Н2-блокаторов [2].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Н2-блокаторы (ранитидин**, фамотидин**) подавляют секрецию соляной кислоты за счет вытеснения гистамина из связи с Н2 -рецепторами париетальных клеток. Эти препараты поддерживают показатели внутрижелудочного рН> 3 на протяжении суток в течение 8-10 часов. Многочисленные проведенные исследования показали, что применение Н2— блокаторов в течение 4-6 недель приводит к рубцеванию язвенного дефекта у 70-80% пациентов с дуоденальными язвами и у 55-60% пациентов с язвами желудка [2]. Последний мета-анализ продемонстрировал, что Н2-блокаторы значительнее эффективнее плацебо в достижении рубцевания язвенного дефекта (ОШ 3,80, 95% ДИ: 3,44-4,20; p <0,0001) [25]. Тем не менее, после того как в клинической практике в качестве базисной антисекреторной терапии стали широко применяться ИПН, Н2-блокаторы утратили свои позиции и в настоящее время применяются редко, главным образом, при невозможности применения ИПН или же в комбинации с ними с целью усиления антисекреторного действия.
- Всем пациентам с ЯБ с положительными результатами тестирования на инфекцию H.рylori с целью профилактики последующих рецидивов ЯБ рекомендуется проведение эрадикационной терапии [20, 28].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2).
Комментарии: В мета-анализе, обобщившем результаты 5 рандомизированных контролируемых исследований в популяции пациентов с язвенной болезнью, осложненной перфорацией, было продемонстрировано, что эрадикационная терапия значительно снижает риск рецидива заболевания в течение года после ушивания дефекта (ОР 1,49; 95% ДИ: 1,10-2,03) [28]. Согласно Кокрейновскому обзору и другому мета-анализу, эрадикационная терапия инфекции H. pylori у инфицированных пациентов с снижает риск рецидива язвенной болезни двенадцатиперстной кишки (ОР = 0,20; 95% ДИ: 0,15 — 0,26) и желудка (ОР = 0,29; 95% ДИ 0,20, 0,42) в сравнении с плацебо [29].
Согласно рекомендациям последнего согласительного совещания Европейской рабочей группы по изучению H. pylori «Маастрихт-V» (2016) [20], выбор той или схемы эрадикации зависит от частоты резистентности штаммов Н. pylori в данном регионе к кларитромицину**, Если показатели резистентности к кларитромицину** в регионе не превышают 15%, то в качестве схемы первой линии назначается стандартная тройная терапия без предварительного тестирования. Поскольку показатели устойчивости штаммов Н. pylori к кларитромицину** в России не превышают 10%, схемой первой линии является стандартная тройная схема эрадикационной терапии, включающая в себя ИПН (в стандартной дозе 2 раза в сутки), кларитромицин** (по 500 мг 2 раза в сутки) амоксициллин** (по 1000 мг 2 раза в сутки).
В настоящее время разработаны меры, которые позволяют повысить эффективность стандартной тройной терапии:
1. Назначение дважды в день повышенной дозы ИПН (удвоенной по сравнению со стандартной) [20]
2. Увеличение продолжительности тройной терапии с ИПН и кларитромицином** до 14 дней. В настоящее время отмечено, что только такая продолжительность обеспечивает сопоставимую эффективность стандартной тройной терапии с эффективностью других схем [20].
3. Подробное инструктирование пациента и контроль за точным соблюдением назначенного режима приема лекарственных средств.
Как вариант эрадикационной терапии первой линии (например, при непереносимости препаратов группы пенициллина) может быть назначена классическая четырехкомпонентная схема на основе висмута трикалия дицитрата** (120 мг 4 раза в сутки) в комбинации с ИПН (в стандартной дозе 2 раза в сутки), тетрациклином (500 мг 4 раза в сутки), метронидазолом** (по 500 мг 3 раза в сутки) в течение 10 дней [20].
Квадротерапия с висмута трикалия дицитратом** применяется также как основная схема терапии второй линии при неэффективности стандартной тройной терапии. Другой схемой терапии второй линии служит эрадикационная схема, включающая в себя ИПН (в стандартной дозе 2 раза в сутки), левофлоксацин** (в дозе 500 мг 2 раза в сутки) и амоксициллин** (в дозе 1000 мг 2 раза в сутки). Тройная терапия с левофлоксацином** может быть назначена только врачом-гастроэнтерологом по взвешенным показаниям.
Терапия третьей линии основывается на определении индивидуальной чувствительности Н.pylori к антибиотикам [30].
- Пациентам с лабораторно и эндоскопически подтвержденным язвенным кровотечением с целью его остановки в рамках других мероприятий по достижению гемостаза рекомендуется внутривенное введение ингибиторов протонного насоса [56].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии: Остановке язвенных кровотечений и снижению риска развития повторных кровотечений способствует применение ИПН [31]. При этом одномоментно болюсно внутривенно вводится 80 мг эзомепразола** с последующей непрерывной внутривенной инфузией этого препарата (в дозе 8 мг в час) в течение 72 часов [32]. Согласно одному из последних мета-анализов, внутривенное применение ИПН способствует значительному снижению риска повторных кровотечений (ОШ 2,24, 95% ДИ: 1,02 – 4,90) [31]. После перевода пациента на пероральный прием препаратов проводится эрадикационная терапия.
3. Хирургическое лечение
- Пациентов с осложненными формами ЯБ желудка и двенадцатиперстной кишки (кровотечение, перфорация и др.) рекомендуется госпитализировать с целью оперативного лечения в стационар хирургического профиля [16, 33, 34, 35, 36, 37].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Пациентов, страдающих осложненным течением язвенной болезни, как правило, необходимо госпитализировать в стационар в экстренном порядке. Лечение язвенного кровотечения целесообразно начинать в отделении интенсивной терапии. Главной задачей лечения в отделении интенсивной терапии является стабилизация состояния пациента – восполнение объема циркулирующей крови, борьба с проявлениями гиповолемического шока, адекватное обезболивание, лечение декомпенсированных сопутствующих заболеваний и синдрома системной воспалительной реакции, после чего могут быть применены хирургический и/или эндоскопический методы лечения [10, 33, 34, 38, 39]. Важно отметить, что при язвенном кровотечении риск смерти коморбидного пациента прямо коррелирует с количеством сопутствующих заболеваний [40]. Это, в свою очередь, требует от врача очень большой внимательности при работе с коморбидными пациентами и анализа всех факторов риска развития осложнений язвенной болезни до момента их реализации [41].
- Пациентам с язвенным кровотечением проведение эзофагогастродуоденоскопии с целью верификации источника кровотечения и выполнения эндоскопического гемостаза рекомендуется проводить в первые 2 часа после госпитализации [33, 35].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
- Пациентам с язвенным кровотечением повторную эзофагогастродуоденоскопию с целью динамического контроля источника кровотечения и выполнения эндоскопического гемостаза рекомендуется проводить только при рецидиве кровотечения и в случае высокого риска его развития [42, 43].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии: Ряд исследований подтверждают, что выполнение лечебной эндоскопии для остановки язвенного кровотечения достоверно снижают смертность, необходимость хирургического вмешательства, риск рецидива кровотечения, а также время продолжающегося кровотечения в сравнении с фармакотерапией [44]. По данным литературы, эндоскопическая остановка кровотечения является «золотым стандартом» в лечении пациентов с язвенными кровотечениями. Своевременное и правильное эндоскопическое пособие позволяет достичь устойчивого гемостаза в 89-92% случаев. Оценка язвенного кровотечения производиться по классификации Forrest. Наиболее эффективным эндоскопическим способом остановки кровотечения являются клипирование кровоточащего сосуда и аргоно-плазменная коагуляция. Другие методы эндоскопической остановки кровотечении, такие как электрокоагуляция, обкалывание язвы, нанесение пленкообразующих препаратов, использование полисахаридной гемостатической системы должны использоваться в комбинации с основными методами.
По данным систематического обзора B. J. Elmunzer с соавт., факторами риска рецидива кровотечения являются: большой размер язвы (более 1 см в диаметре), расположение язвы на малой кривизне желудка и на задней стенке двенадцатиперстной кишки, а также нестабильная гемодинамика – снижение артериального давления во время кровотечения с последующим повышением на фоне восполнения объема циркулирующей крови [42]. Также важно отметить, что прием антикоагулянтов и дезагрегантов существенно повышает риск развития язвенного кровотечения, в том числе повторного, равно как и резкое повышение артериального давления (например, как реакция на боль или вследствие пропущенной дозы антигипертензивного препарата). Выполнение повторной ЭГДС у пациентов с низким риском рецидива кровотечения не влияет на частоту рецидивов кровотечения и экономически нецелесообразно [33, 34, 43].
- Пациентам с язвенным кровотечением экстренное хирургическое вмешательство с целью верификации источника кровотечения и его остановки рекомендуется проводить при неэффективности эндоскопического гемостаза в максимально ранние сроки [10, 33, 34, 45].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Хирургическое лечение пациентов с язвенным кровотечением показано в тех случаях, когда нет возможности контролировать его эндоскопически (при продолжающемся кровотечении или при его рецидиве). Несвоевременное хирургическое лечение ухудшает прогноз пациента и увеличивает риск летального исхода. Операция необходима для достижения надежного гемостаза и снижения риска рецидива кровотечения. Объем предполагаемой операции зависит от состояния пациента, но важно помнить, что хирургическое вмешательство должно носить максимально щадящий характер. У пациентов с высоким риском хирургического вмешательства предпочтительно выполнение рентгеноэндоваскулярной селективной ангиографии с последующей окклюзией кровоточащего сосуда. Согласно зарубежным рекомендациям, наиболее предпочтительным является выполнение гастротомии (пилородуоденотомии) с прошиванием кровоточащего сосуда и ушиванием язвенного дефекта, однако этот метод уступает по своей надежности резекционным операциям [10]. Наилучший результат при лечении рефрактерных осложненных язв отмечен при сочетании резекция желудка с наложением гастроеюноанастомоза и ваготомией [46], однако в зарубежной литературе ваготомия рассматривается как сложная, ограниченно применимая опция, для полноценного признания которой должны быть проведены исследования высокого уровня доказательности [47]. Российское научное хирургическое сообщество рекомендует выполнение ваготомии, ограничивая при этом показания к ее проведению [35].
Резекцию 2/3 желудка по поводу язвенной болезни необходимо выполнять по Б-II в модификации Гофмейстера-Финстерера. При этой виде резекции желудка щелочное содержимое двенадцатиперстной кишки попадает в культю желудка и ощелачивает содержимое, что предупреждает развитие рецидива язвы в культе и в гастроэнтероанастомозе. При резекции желудка по Ру ощелачивания не происходит, и вероятность рецидива язвы значительно выше.
- Пациентам с перфорацией язвы желудка и/или двенадцатиперстной кишки рекомендуется проведение экстренной операции с целью ликвидации перфорационного отверстия [16, 34, 48].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2)
Комментарии: Перфорация язвы — это распространенное осложнение, которое неизбежно ведет к развитию перитонита и имеет высокую летальность среди пациентов, достигающую 30%. Наиболее высокая летальность наблюдается среди пожилых пациентов, а наибольшая смертность отмечена в группе пациентов с поздней госпитализацией (больше 24 часов от развития данного осложнения). Лапаротомный доступ не имеет преимуществ перед лапароскопическим. Предпочтительным является выполнение лапараскопического вмешательства – ушивание перфоративного отверстия с санацией и дренированием брюшной полости [16, 34, 48]. Однако, клиническая картина течения столь грозного осложнения может быть очень разнообразной, и эксперты признают, что объем операции зависит прежде всего от состояния пациента [48]. В отечественных клинических рекомендациях по лечению перфоративной язвы более подробно рассмотрены варианты хирургического лечения [36].
- Пациентам с язвенной болезнью после хирургического лечения рекомендуется выполнение диагностических исследований, направленых на выявление H.pylori (см. раздел по диагностике) и проведение эрадикационной и поддерживающей терапии с целью предупреждения рецидивов ЯБ и ее осложнений [33, 49, 50].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии: Выполненный этап хирургического лечения не снижает риска развития нового витка хирургических осложнений язвенной болезни, прежде всего кровотечений, поэтому важно продолжить курс консервативного лечения заболевания до полного излечения пациента.
- Пациентам с пилородуоденальным стенозом с целью его устранения рекомендуется проведение эндоскопической баллонной дилатации. При ее неэффективности рекомендуется проведение пилоропластики и дренирующих операций [34].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Показания к хирургическому лечению пациентов с пилородуоденальным стенозом определяются степенью его компенсации, а также состоянием пациентов. Эндоскопическая баллонная дилатация возможна только у пациентов с субкомпенсированным стенозом и с локализацией рубца по передней стенки двенадцатиперстной кишки. Данное эндоскопическое пособие часто носит временный успех и сопровождается высокой частотой рецидивирования стеноза.
Дополнительная информация, влияющая на течение и исход заболевания
1. Особенности течения ЯБ у отдельных групп пациентов
1.1 Особенности течения ЯБ при беременности
Течение ЯБ при беременности в целом мало отличается от такового у небеременных женщин. Диагноз устанавливается на основании клинических проявлений, анамнестических данных, результатов ЭГДС и ультразвукового исследования [53]. Рентгенологическое исследование желудка и двенадцатиперстной кишки беременным противопоказано.
В диагностически не ясных случаях, при подозрении на развитие осложнений (кровотечение, стеноз антрального отдела желудка, рак) ЭГДС в силу своей безопасности для плода может быть проведена при любом сроке беременности [54]. для исключения оккультного кровотечения проводятся исследование кала на скрытую кровь, общий (клинический) анализ крови.
Дифференциальный диагноз обострения язвенной болезни затруднен, его необходимо проводить с эрозивным гастродуоденитом, панкреатитом, заболеваниями желчевыводящих путей, острым аппендицитом и ранним токсикозом – рвотой. Стенозирующая язва антрального отдела желудка может симулировать чрезмерную рвоту беременных. Для раннего токсикоза характерны мучительная, почти постоянная тошнота, усиливающаяся на различные запахи, слюнотечение. При этом рвота бывает независимо от еды, особенно по утрам, боль в животе, как правило, отсутствует. Кровотечение, обусловленное язвенной болезнью, необходимо дифференцировать с эрозивным гастритом, синдромом Маллори-Вейсса, кровотечением из дыхательных путей, раком желудка.
Беременность оказывает благоприятное влияние на течение язвенной болезни: у 75-80% женщин отмечается ремиссия заболевания, и оно не оказывает заметного влияния на ее исход. Однако у некоторых пациенток может произойти обострение. Чаще это наблюдается в I триместре беременности (14,8%), третьем (10,2%), за 2-4 недели до срока родов или раннем послеродовом периоде). Неосложненная язвенная болезнь не оказывает отрицательного влияния на развитие плода.
Лечение включает соблюдение общепринятых «режимных» мероприятий и диеты; прием в обычных терапевтических дозах невсасывающихся антацидов (например, коллоидного фосфата алюминия и адсорбентов в виде диоктаэдрического смектита). При отсутствии эффекта назначаются Н2-блокаторы.
При выраженных болях, обусловленных моторными нарушениями возможно назначение спазмолитиков (дротаверин** по 40 мг 3-4 раза в день). Препараты висмута беременным противопоказаны. Эрадикационная терапия инфекции Н. pylori у беременных не проводится.
1.2 Особенности течения ЯБ у лиц пожилого и старческого возраста
В развитии гастродуоденальных язв у пациентов пожилого возраста — помимо инфекции НР и кислотно-пептического фактора – могут также играть роль атеросклеротические изменения сосудов желудка, некоторые фоновые заболевания (например, хронические неспецифические заболевания легких), снижающие защитные свойства слизистой оболочки желудка, прием лекарственных препаратов (в первую очередь, НПВП), обладающих ульцерогенным действием.
Гастродуоденальные язвы у пациентов пожилого и старческого возраста локализуются преимущественно в желудке (по малой кривизне тела или в субкардиальном отделе), имеют иногда очень большие размеры, часто протекают со стертой и неопределенной клинической симптоматикой, отличаются наклонностью к развитию осложнений (прежде всего, желудочно-кишечных кровотечений). При обнаружении у пожилых пациентов язв в желудке важное значение имеет проведение дифференциального диагноза с инфильтративно-язвенной формой рака желудка.
Гастродуоденальные язвы у лиц пожилого и старческого возраста характеризуются медленным рубцеванием. При проведении медикаментозной терапии следует соблюдать осторожность, учитывая более высокий риск развития побочных эффектов у пожилых пациентов по сравнению с пациентами молодого и среднего возраста.
Язва двенадцатиперстной кишки — симптомы и лечение
Что такое язва двенадцатиперстной кишки? Причины возникновения, диагностику и методы лечения разберем в статье доктора Аверина Александра Анатольевича, гастроэнтеролога со стажем в 16 лет.
Над статьей доктора Аверина Александра Анатольевича работали литературный редактор Маргарита Тихонова , научный редактор Роман Васильев

Гастроэнтеролог Cтаж — 16 лет
Медицинский центр «Норма»
Дата публикации 22 марта 2019 Обновлено 31 января 2023
Определение болезни. Причины заболевания
Язвенная болезнь двенадцатиперстной кишки (ДПК) — это хроническое рецидивирующее заболевание, которое протекает с чередованием периодов обострения и ремиссии. Его основным морфологическим признаком является образование язвы в ДПК. [1]
Краткое содержание статьи — в видео:
Распространённость
На территории России данной болезнью страдает 5-10 % взрослого населения. Болеют в основном мужчины до 50 лет. [2] Считается, что болезнь может возникнуть у 11-14 % мужчин и 8-11 % женщин в течение жизни. [7]
Факторы риска
Язвенная болезнь ДПК может возникнуть по различным причинам. Чаще всего к развитию этой болезни приводят следующие факторы:
- наследственная предрасположенность — генетически обусловленное увеличение массы обкладочных клеток, вырабатывающих соляную кислоту желудочного сока, повышенная чувствительность этих клеток к гастрину (гормону, участвующему в пищеварении), увеличение количества пепсиногена-1, нарушение моторики желудка и другие;
- нейропсихические факторы — дисбаланс в регуляции моторной функции желудка и ДПК со стороны нервной системы, приводящий к забросу агрессивного желудочного содержимого в просвет кишки;
- алиментарные факторы — погрешности в диете (частое употребление острой и грубой пищи, чрезмерное увлечение напитками с кофеином);
- вредные привычки — неумеренное потребление алкоголя, курение;
- неконтролируемый приём НПВП — происходит истончение и снижение защитных свойств слизистого барьера ДПК;
- инфекция Helicobacter pylori— вызывает воспалительные изменения в слизистой оболочке ДПК, что приводит к повышению чувствительности к факторам агрессии.
Наиболее значимыми причинами заболевания в настоящий момент считают инфекцию Helicobacter pylori и наследственную предрасположенность. Стоит отметить, что наследуется не сама болезнь, а факторы, предрасполагающие к его развитию.
Второй по значимости причиной является приём лекарств, поражающих ЖКТ, в частности антикоагулянтов и НПВП (Аспирина, Диклофенака, Кеторолака, Ибупрофена и др.).
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы язвы двенадцатиперстной кишки
Ведущие симптомы язвы двенадцатиперстной кишки — боль, диспепсия (расстройство пищеварения), астения и кровотечение (при развитии осложнений).
Болевой синдром
Боли при язве ДПК, как правило, связаны с приёмами пищи: они могут возникнуть как через 0,5-1 час после трапезы (ранние боли), так и спустя 1,5-2 часа после приёма пищи (поздние боли). Также характерны «голодные» боли (болезненные ощущения на голодный желудок, проходящие после приёма пищи) и аналогичные им «ночные» боли. При язвах пилорического канала и луковицы двенадцатиперстной кишки обычно наблюдаются поздние боли (через 2-3 часа после еды). [7]
Пациенты характеризуют болезненные ощущения как ноющие или режущие с постепенным усилением или снижением интенсивности. Как правило, боли носят постоянный характер, проходят или становятся менее интенсивными после приёма пищи, а также антисекреторных и/или антацидных препаратов.
Так же отмечается сезонный характер боли, что совпадает с периодами течения язвенной болезни — фазы ремиссии и обострения. Чаще всего обострение возникает весной и осенью и длится от трёх до шести недель, после чего сменяется периодом ремиссии.
Часть язв (по некоторым источникам, до 25% случаев) вообще протекает без болевого синдрома — т. н. «немые язвы». [2]
Болезненные ощущения чаще локализуются в эпигастрии, но могут распространятся и на правое подреберье. Наиболее ярко болевой синдром выражен при расположении язвенного дефекта в области луковицы и привратника (перехода между желудком и ДПК).
Пациентам необходимо прислушиваться к своему организму и при длительном болевом синдроме (более 3-4 недель), сезонности приступов боли и их связи с приёмами пищи следует обязательно обратиться к врачу.
Синдром диспепсии
Диспепсия проявляется целой группой симптомов, связанных с нарушениями пищеварения. Они тоже связаны с приёмами пищи и носят сезонный и периодичный характер (часто встречаются при обострении).
В основном встречаются следующие проявления (расположены по убыванию их частоты):
- изжога (испытывают 60-80% больных);
- отрыжка кислым;
- тошнота;
- рвота;
- запор.
Иногда симптомы диспепсии преобладают над болевым синдромом.
После рвоты может стать легче, поэтому пациенты иногда вызывают её специально. Но такая рвота встречается сравнительно редко. [7]
Астенический синдром
Астения проявляется повышенной утомляемостью, плохим настроением, незначительным снижением веса: не смотря на повышенный аппетит, больные стараются ограничивать себя в еде, опасаясь усиления болей.
Кровотечение
Хотя кровотечение из язвы относится к осложнениям язвенной болезни, иногда оно может быть первым и единственным симптомом наличия язвенного дефекта в ДПК. Проявляется либо рвотой с примесью свежей и/или изменённой крови по типу «кофейной гущи», либо стулом чёрного цвета, напоминающего дёготь, с резким неприятным запахом — милена.
При наличии данного симптома требуется немедленно обратиться за медицинской помощью. Так как именно это осложнение приводит к наибольшей летальности при язвенной болезни. Игнорировать его нельзя!
Обострения язвы
Первые симптомы при обострении язвенной болезни: боль, диспепсия (расстройство пищеварения), астения и при осложнённом течении — кровотечение. Частота обострений при хроническом течении: 1-2 раза в год, как правило весной и осенью.
Патогенез язвы двенадцатиперстной кишки
В основе патогенеза язвенной болезни ДПК лежит лежит дисбаланс между факторами агрессии и защитными свойствами слизистой оболочки ДПК. Данный факт наглядно иллюстрируют «весы», предложенные H. Shay и D.C.H. Sun. [1] Будет ли развиваться язва ДПК или нет, зависит от того, какая чаша перевесит — «агрессии» или «защиты».
Основными факторами агрессии являются:
- соляная кислота и её гиперпродукция;
- пепсиноген и пепсин;
- увеличение массы обкладочных клеток;
- гиперпродукция гастрина; [5]
- нарушение эвакуации содержимого из желудка и ДПК;
- инфекция Helicobacter pylori;
- токсические вещества (курение, алкоголь, лекарства).
Противостоят им факторы защиты:
- выработка и качественный состав защитной слизи;
- секреция бикарбонатов;
- регенераторная активность эпителиальных клеток слизистой;
- адекватное кровоснабжение слизистой;
- достаточное содержание простагландинов в кишечной стенке (уменьшается при приёме НПВС).
Низкая сопротивляемость факторам агрессии, как правило, носит наследственный характер. При длительном воздействии агрессивной среды (прямое разрушающее действие соляной кислоты и пепсина) на слизистую оболочку с низкой защитой и способностью к восстановлению происходит локальное разрушение слизистого барьера, а затем и слизистой оболочки с образованием сначала поверхностного дефекта. Затем происходит разрушение стенки кишки до подслизистого и мышечного слоя с образованием язвы, а при осложнениях (пенетрации или перфорации) разрушаются все слои кишечной стенки. При попадании в зону язвенного некроза крупного кровеносного сосуда, язва осложняется кровотечением.
Из всех факторов, снижающих способность слизистой к защите и восстановлению, ведущую роль играют:
- снижение толщины и качества слизистого барьера и бикарбонатного буфера, который поддерживает кислотно-щелочное равновесие и не даёт агрессивному содержимому контактировать с эпителием напрямую;
- снижение способности слизистой к регенерации;
- нарушение кровотока;
- длительный приём НПВС;
- инфекция Helicobacter pylori.
После образования язвенного дефекта в слизистой в ответ на чрезмерную агрессию и повреждение начинают активироваться факторы защиты и регенерации. Развивается местная воспалительная реакция, усиливается кровоток, происходит лейкоцитарная инфильтрация слизистой по краям язвенного дефекта. Дно язвы покрывается фибрином, который защищает кишечную стенку от дальнейшего повреждения кислотой и пепсином. По краям язвы повышается способность клеток эпителия слизистой к делению, и постепенно происходит эпителизация язвенного дефекта (от краёв к центру).
Когда растущий новый эпителий слизистой сходится в центре, на месте язвенного дефекта образуется рубец.
В области рубца, образующегося на месте язвы, слизистая оболочка уже неполноценная. Часть функциональных клеток замещается клетками соединительной ткани и не может полноценно выполнять свою защитную функцию, а также быстро регенерировать. Поэтому при следующем преобладании факторов «агрессии» над факторами «защиты» происходит повторное образование язвенного дефекта слизистой. При хронических рецидивирующих язвах дефекты слизистой, как правило, образуются в том же месте. Таким образом, фаза ремиссии сменяется фазой обострения.
Классификация и стадии развития язвы двенадцатиперстной кишки
В настоящий момент общепринятой классификации язвенной болезни ДПК не существует. Однако в клинической практике принято различать это заболевание по следующим критериям:
- Клиническая форма:
- острая;
- хроническая.
- По локализации:
- язвы луковицы ДПК;
- постбульбарные язвы.
- По сочетанию с инфекцией Helicobacter pylori:
- язва луковицы, ассоциированная с Helicobacter pylori;
- идиопатическая язва — при отсутствии инфекции Helicobacter pylori.
- По характеру заболевания:
- первичная язва — как самостоятельное заболевание;
- вторичная язва — как следствие другого заболевания («стрессовых», лекарственных, других хронических заболеваний и эндокринных патологий).
- По размеру:
- малые — ≤ 0,5 см;
- средние — 0,6-1,9 см;
- большие — 2,0-3,0 см;
- гигантские — > 3,0 см.
- По наличию осложнений:
- без осложнений;
- с кровотечением;
- с перфорацией;
- с пенетрацией;
- с рубцовым стенозом.
В течении хронической язвенной болезни ДПК различают несколько стадий. К основным относятся:
- период обострения — острая язва;
- период рубцевания — язва в фазе заживления и рубцевания;
- период ремиссии — отсутствие клинических и эндоскопических проявлений язвенной болезни (язвенного дефекта).
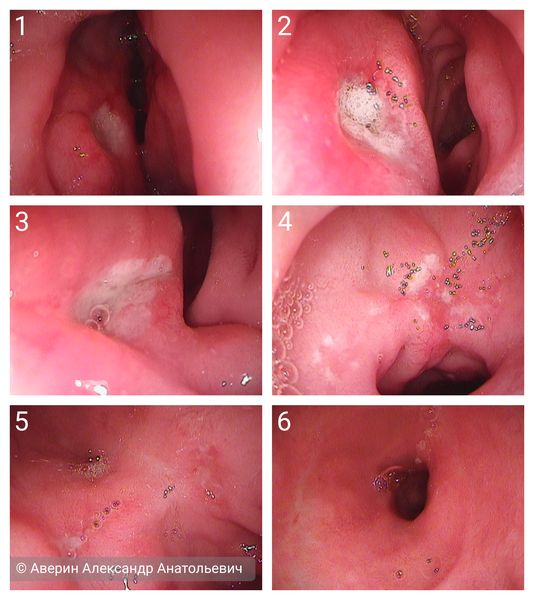
В зависимости от характерных признаков заболевания при проведении эндоскопии (ЭГДС) стадии язвенной болезни выглядят следующим образом: [3]
- острая фаза — язва округлой формы размером от 1-2 мм до нескольких см с чёткими краями, выраженным воспалительным валом в виде кольца, дно покрыто фибрином, один из краёв подрытый, слизистая вокруг гиперемирована;
- фаза стихания воспаления — воспалительный вал менее выражен, края чёткие, форма овальная, дно в центре покрыто фибрином, по краям появляются ярко красные грануляции, слизистая вокруг гиперемирована, имеются мелкие радиальные складки;
- начало заживления — края язвы становятся плоскими, форма становится вытянутой или щелевидной, воспалительный вал не дифференцируется, дно язвы на 2/3 покрыто свежим эпителием, в центре сохраняется тонкий белый налёт, слизистая вокруг слабо гиперемирована, имеются чёткие радиальные складки;
- заживления — язва в виде щели или округлая, размеры значительно уменьшились, нет угла наклона между краем язвы и дном, в центре расположен маленький участок с белым налётом, окружающая слизистая розовая, наблюдается конвергенция складок;
- свежий рубец (красный рубец) — дно язвы полностью покрыто свежим розовым эпителием, налёта нет, при близком осмотре в новой слизистой видно много мелких сосудов;
- старый рубец (белый рубец) — воспалительных изменений нет, слизистая вокруг розовая, рубец имеет белесоватый цвет.
Осложнения язвы двенадцатиперстной кишки
В стадии обострения язвенная болезнь может осложнятся кровотечением, перфорацией или пенетрацией. В стадии рубцевания и ремиссии может возникнуть такое осложнение, как рубцовый стеноз ДПК, вплоть до кишечной непроходимости.
Кровотечение
Кровотечение из крупных сосудов, попавших в зону язвенного дефекта, является наиболее частым и грозным осложнением язвенной болезни — встречается в 15-20% случаев. Большинство кровотечений развиваются при расположении язвы на передней стенке луковицы ДПК и в постбульбарных отделах. Проявляется выделением изменённой крови по типу «кофейной гущи» при рвоте и/или с изменённым стулом по типу «мелены» (чёрный жидкий стул). В клиническом анализе крови будут изменятся показатели красной крови: падает гемоглобин, снижается уровень эритроцитов и гематокрита. Неинтенсивные кровотечения могут давать положительный результат кала на скрытую кровь. Данный вид осложнения нуждается в экстренной эндоскопической или хирургической помощи. [2] [5]
Перфорация
Данное осложнение представляет собой нарушение целостности стенки ДПК в месте язвенного дефекта. Оно возникает при распространении язвы вглубь стенки. Так, образуется отверстие, соединяющее просвет кишки с брюшной полостью. Его возникновение проявляется остро возникшей «кинжальной болью» с последующим развитием перитонита (как результат излития содержимого кишечника в брюшную полость). Встречается в 5-15% случаев. Требует хирургического лечения. [2] [5]
Пенетрация
При разрушении стенки ДПК в месте язвенного дефекта и фиксации его с близлежащим органом происходит разрушение тканей данного органа. Иными словами, язва проникает в соседние ткани. Чаще всего пенетрация распространяется на поджелудочную железу, малый сальник, печень, желчный пузырь и протоковую систему.
При этом осложнении боли теряют связь с приёмом пищи и становятся более интенсивными и постоянными. В анализе крови происходят воспалительные изменения. Такое осложнение устраняется хирургическим методом. [2]
Стеноз
При формировании грубых рубцовых изменений стенки ДПК происходит сужение и в дальнейшем полное перекрытие просвета кишки. Это приводит к переполнению желудка содержимым и, как следствие, рвотам. Стул при этом отсутствует — развивается клиника высокой кишечной непроходимости. [2] [5]
Малигнизация — трансформация доброкачественных клеток в злокачественные — для язвенной болезни ДПК, в отличие от язв желудка, не характерна.
Диагностика язвы двенадцатиперстной кишки
К какому врачу обратится при наличии симптомов
При подозрении на язвенную болезнь двенадцатиперстной кишки следует обратиться к терапевту и/или гастроэнтерологу. В случае развития осложнений потребуется консультация хирурга.
Постановка диагноза «Язвенная болезнь ДПК» основывается на сборе анамнеза, оценке наследственной предрасположенности к заболеванию, клинической картине и инструментальных методах обследования.
К обязательным обследованиям относятся: [6]
- ЭГДС (ВЭГДС или ФГДС) — «золотой» стандарт диагностики язвенной болезни;
- определение инфекции Helicobacter pylori — важное исследование, так как наличие этой инфекции радикально меняет тактику лечения и прогноз;
- РН-метрия — для определения кислотообразующей функции желудка;
- клинический анализ крови — помогает заподозрить и дифференцировать осложнения язвенной болезни при их стёртом течении.
Сдавать анализ кала на скрытую кровь не обязательно, так как он кардинально не влияет на тактику лечения. Его назначают во время скрининга, чтобы определить, нужно ли проводить ЭГДС.
К вспомогательным методам относятся:
- рентгенография с контрастом — применяется при подозрении на осложнения язвенной болезни (пенетрации, перфорации, рубцовой деформации ДПК со стенозом) или на локализацию язвы в постбульбарных отделах;
- определение уровня гастрина и паратгормона — проводится при часто рецидивирующих язвах (более двух обострений в год) для уточнения причины заболевания. У многих пациентов с язвой секреция кислоты повышается в ответ на стимуляцию секреции желудочного сока пентагастрином. Часто у пациентов с синдромом Золлингера — Эллисона (результат опухоли, секретирующей гастрин) наблюдаются значительная гиперсекреция кислоты, и обычно имеются множественные язвы двенадцатиперстной кишки. [5]
Несколько слов об ЭГДС
Данный вид исследования оброс множеством мифов и предрассудков. Какие же ощущения на самом деле испытывает человек при проведении эндоскопа через глотку, пищевод, желудок и ДПК:
- ощущение тошноты и рвотный рефлекс, похожие на ощущения при осмотре горла при помощи шпателя или ручки ложки (обычный осмотр при ОРЗ);
- ощущение застрявшего комка в горле (как будто вы что-то плохо прожевали и попытались проглотить). В редких случаях могут быть болезненными;
- распирание, вздутие и тяжесть в животе при инсуфляции желудка воздухом;
- ощущение движения или шевеления внутри живота при манипуляции эндоскопом;
- иногда появляется чувство нехватки воздуха, чаще субъективного характера (так как дыхательные пути эндоскоп не перекрывает).
Никаких других ощущений при проведении ЭГДС не возникает. Их сила и выраженность строго индивидуальна и зависит от многих факторов. Но если правильно себя вести, слушаться подсказок медицинского персонала и хорошо подготовиться к исследованию, то процедура проходит с минимальными затратами времени и минимумом неприятных ощущений.
Как вести себя во время ЭГДС:
- Хорошо подготовьтесь к исследованию. Процедура проводится строго натощак, последний приём пищи возможен за 6-8 часов до исследования. Это позволит эндоскописту как можно быстрее осмотреть всю поверхность слизистой и обнаружить даже минимальные изменения на ней. Также это поможет снизить рвотный рефлекс и тошноту.
- При проведении эндоскопа через рот и глотку старайтесь не трогать его языком. Иначе это затрудняет проведение эндоскопа (современные аппараты очень гибкие) и повышает рвотный рефлекс, так как часть рвотных рецепторов расположена как раз на языке у его корня.
- Старайтесь глубоко и равномерно дышать ртом, не замирайте и не останавливайте дыхание. Глубокие и равномерные вдохи и выдохи успокаивают и отчасти снижают тошноту. Дышать лучше сразу ртом, так как во время самого исследования трудно переключить дыхание, а при дыхании через нос происходит рефлекторный отёк слизистой и выделение слизи, в результате чего нос закладывает, и дыхание сбивается.
- Крепко обнимите себя за живот, не размахивайте руками. Это поможет сосредоточиться на дыхании и не будет мешать эндоскописту руками.
- Старайтесь не сопротивляться проведению эндоскопа и не мешать медицинскому персоналу. Тем самым вы существенно сократите время процедуры. Также старайтесь не срыгивать воздух: уменьшиться время на инсуфляцию, а следовательно и вся процедура.
ЭГДС считается «золотым стандартом» диагностики язвенной болезни ДПК, так как с его помощью язва чётко видна как дефект слизистой оболочки (частота выявления близка к 100%), есть возможность проследить все стадии течения заболевания, возможно проведение биопсии, диагностики инфекции Helicobacter pylori и определение уровня кислотности. В случае обнаружения такого осложнения, как кровотечение, проводится эндоскопический гемостаз. Также с помощью ЭГДС можно обнаружить и другие заболевания (онкологию, полипы, гастрит и т.д.).
Если пациент не в силах немного потерпеть (длится исследование обычно 3-6 минут) и преодолеть свои страхи, то возможно выполнение ЭГДС под наркозом (медикаментозным сном).
Отказ от проведения данного исследования повышает риски неточной постановки диагноза и назначения неадекватного лечения. А при несвоевременной диагностике осложнений всё может закончиться для пациента фатально.
Лечение язвы двенадцатиперстной кишки
К обязательным мероприятиям при лечении я звы желудка и двенадцатиперстной кишки относятся:
- соблюдение щадящей диеты (механическое и химическое щажение);
- исключение таких факторов агрессии, как курение, алкоголь;
- снижение дозы или ограничение приёма некоторых лекарств (НПВС, антикоагулянты).
Если пациентам трудно соблюдать диету, врачи рекомендуют придерживаться общих принципов здорового питания и 1-2 недели при остром периоде болезни не употреблять пищу, которая стимулирует выработку излишней соляной кислоты и пепсина: не есть грубую клетчатку, наваристые рыбные, мясные или грибные бульоны и супы, томаты, консервированные продукты и специи.
Медикаментозное лечение
Медикаментозное лечение направлено на снижение уровня соляной кислоты, защиту и повышение регенерации слизистой ДПК. Для снижения кислотности применяются ингибиторы протонной помпы (ИПП) как «золотой» стандарт лечения и Н2-гистамино блокаторы. [6] Для повышения защитных свойств слизистой применяются обволакивающие средства и антациды. Для повышения регенерации слизистой используются препараты висмута и сукральфата. При наличии инфекции Helicobacter pylori проводится эрадикационная терапия первой или последующих линий. [6] В меньшей степени применяются:
- препараты, регулирующие моторно-эвакуаторную функцию желудка и кишечника — назначаются при язвенной болезни, сочетающейся с рефлюксами и недостаточностью пилорического сфинктера;
- психотропные препараты — применяются для купирования депрессии и стрессовых факторов, когда болезнь протекает очень длительно, и присоединяется психосоматический компонент.
В случае развития осложнений применяются эндоскопические или хирургические методы лечения.
Хирургическое лечение
Хирургические методы сводятся к лечению таких осложнений, как:
- перфорация — проводится ушивание язвенного дефекта или удаление повреждённого участка кишки и желудка с наложением анастомоза;
- пенетрация — производится удаление повреждённых тканей и части кишки с наложением анастомоза;
- рубцовый стеноз — выполняется резекция (частичное удаление) с наложением анастомоза.
К эндоскопическим методам относится в первую очередь эндоскопический гемостаз. Данный метод позволяет в большинстве случаев остановить кровотечение из язвы и профилактировать его рецидив (при остановившемся кровотечении). [4] При рубцовом стенозе и сужении просвета ДПК иногда может применятся стентирование (при противопоказаниях к полостной операции).
В целом курс медикаментозного лечения при обострении язвенной болезни или при впервые выявленной язве длится 1-2 месяца. К хирургическим и эндоскопическим методам прибегают только при развитии соответствующих осложнений.
Экстренная помощь при приступе
Экстренная помощь проводится при осложнениях язвенной болезни (кровотечение, прободение, стеноз просвета ДПК). При развитии этих осложнений необходимо обратиться в клинику для консультации хирурга. При выраженном болевом синдроме, падении артериального давления, слабости и других признаках внутреннего кровотечения необходимо вызвать скорую помощь для оказания неотложной медицинской помощи.
Для уменьшения болевого синдрома в качестве препаратов экстренной помощи применяются альгинаты и антациды и/или быстродействующие препараты из группы ингибиторов протонной помпы (ИПП) — рабепразол, эзомепразол, пантопразол, омепразол.
Диета при язвенной болезни
В период обострения язвенной болезни ДПК применяется щадящая диета с протёртым вариантом готовки блюд. В основе диеты лежат следующие принципы:
- Механическое щажение обеспечивается за счёт выбора пищевых продуктов с небольшм содержанием в них грубой клетчатки, непродолжительного пребывания пищи в желудке и специальной кулинарной обработки продуктов (тушение, готовка на пару, измельчение пищи до консистенции пюре).
- Химическое щажение основано на повышении содержания жиров растительного происхождения и белков животного происхождения (творог, сыр, яйца, отварные мясо и рыба) на фоне физиологической нормы углеводов, витаминов, микроэлементов, так как жиры тормозят желудочную секрецию, а белки инактивируют соляную кислоту.
- Термическое щажение достигается исключением слишком холодной и горячей пищи, которая травмирует слизистую желудка, оптимальная температура горячих блюд +30-40 ° С.
- Ограничение объёма одновременно принятой пищи с целью предупреждения перерастяжения желудка: пищу принимают 4-5 раз в день и небольшими порциями. Приём пищи должен соответстввать ритму желудочной секреции и проводиться с интервалом 3,5-4,5 часа.
Исключаются продукты, сильно повышающие выработку соляной кислоты желудком. Такие как: солёные приправы, крепкие мясные, рыбные или овощные бульоны, чёрный хлеб, мягкий хлеб и выпечка, газированные напитки, крепкий чай, кофе.
Рекомендуются продукты, обладающие средним уровнем стимуляции выработки соляной кислоты: отварное мясо, рыба, большинство ягод и фруктов и слабым уровнем: яйца всмятку, белые сухари или подсушенный хлеб (из муки тонкого помола), каши, сладкие фрукты и овощи.
В щадящей диете с протёртой пищей в ассортимент блюд включают:
- творог пресный, сыр неострый и нежирный, протёртый;
- супы протёртые из сборных овощей (кроме щей и борща), супы овоще-крупяные, молочные крупяные, с вермишелью или измельченными макаронами;
- овощи отварные протёртые – кабачки, цветная и брюссельская капуста, томаты, морковь, свекла (обязательное исключение белокочанной капусты, репы, редьки, редиса и бобовых, которые богаты растительными волокнами и эфирными маслами);
- спелые фрукты и ягоды сладких сортов (после тепловой обработки);
- компоты с протёртыми сухофруктами;
- хлеб пшеничный подсушенный.
Блюда готовят на пару, отваривают, разваривают до мягкости, пюрируют, измельчают, подают в тёплом виде.
Рекомендуемые блюда щадящей диеты с непротертой пищей те же, что и для варианта, описанного выше. Блюда готовят на пару, отваривают, размельчают до мягкости, но не измельчают, подают в теплом виде 5-6 раз в день.
В период ремиссии рекомендуется придерживаться основных принципов здорового питания. При этом исключаются крепкие мясные и рыбные бульоны, грибной отвар, пряности, острые блюда, маринованные и копчёные продукты, обладающие раздражающим действием на слизистую оболочку и способные повышать образование соляной кислоты в желудке. Ограничивается сдобное тесто, пироги, блины, кофе, минеральные воды и напитки, содержащие углекислоту в большом количестве. Вредным является длительное (свыше 10-15 минут) использование жевательной резинки.
Физиотерапия и лечебная гимнастика при язвенной болезни
Эффективность методов физиотерапии при язвенной болезни ДПК не доказана, так же как и лечебной гимнастики. Поэтому эти методы в лечении язвенной болезни не применяются.
Прогноз. Профилактика
В большинстве случаев при своевременном лечении и соблюдении основных принципов профилактики прогноз благоприятный. При частых рецидивах и развитии осложнений прогноз, соответственно, неблагоприятный. Онкологического потенциала язвенная болезнь ДПК не несёт.
В основе профилактики лежат такие направления, как:
- оздоровление образа жизни — отказ от вредных привычек (алкоголь, курение), улучшение эмоционального фона;
- улучшение условий труда — ограничение или полное исключение вредных факторов;
- организация рационального питания;
- медикаментозная профилактика (эрадикационная терапия при наличии Helicobacter pylori и рациональная фармакотерапия НПВП и антикоагулянтами) [7] ;
- санаторно-курортное лечение в оздоровительных учреждениях гастроэнтерологического профиля.
Питанию отводится особая роль в профилактике язвенной болезни. Оно должно быть сбалансированным, без строгих ограничений. Принимать пищу следует 4-5 раз в день в одно и то же время. Стоит избегать, а лучше полностью ограничить продукты, вызывающие чувство изжоги или боль в животе.
Нужно помнить и о таких простых, но в то же время важных рекомендациях, как приём пищи в спокойной обстановке, не спеша, сидя, тщательно прожёвывая еду. Это способствует лучшему пропитыванию пищи слюной, которая нейтрализует соляную кислоту. [2] [6]
Медикаментозная профилактика предполагает уничтожение Helicobacter pylori и возможное назначение невсасывающихся антацидов за месяц до начала предполагаемого обострения. Профилактические приёмы ИПП и Н2-гистамино блокаторов не проводятся в связи с наличием у этих групп препаратов побочных эффектов, проявляющихся при длительном приёме.
Стойкая эрадикация Helicobacter pylori позволяет снизить риск повторных кровотечений. Такое осложнение выявляется не всегда, в 25–55 % результат может быть ложноотрицательным, поэтому после лечения важно провести повторный тест и убедиться, что Helicobacter pylori больше нет. [7]
Можно ли полностью вылечить язву
Язвенная болезнь двенадцатиперстной кишки — это хроническое рецидивирующее заболевание, поэтому при нарушении баланса между предрасполагающими факторами и защитными свойствами слизистой оболочки ДПК болезнь может проявиться снова. Но при проведении эрадикации, уничтожении Helicobacter pylori, часто сохраняется стойкая ремиссия. [7]
Список литературы
- Гастроэнтерология: руководство / Я.С. Циммерман. — 2-е изд., перераб. и доп. — М.: ГЭОТАР-Медиа, 2015. — 816 с.
- Руководство по Гастроэнтерологии : научное издание / под ред. Ф.И. Комарова, С.И. Рапопорта. — М.: ООО «Медицинское информационное агентство», 2010. — 859 с.
- Чернеховская Н.Е., Андреев В.Г., Черепянцев Д.П., Поваляев А.В. Эндоскопическая диагностика заболеваний пищевода, желудка и тонкой кишки. — М.: «МЕДпрес-информ», 2008. — 199 с.
- Чернеховская Н.Е., Андреев В.Г., Черепянцев Д.П., Поваляев А.В. Лечебная эзофагогастродуоденоскопия. — М.: «МЕДпрес-информ», 2009. — 176 с.
- Форбс А.,Мисиевич Дж.Дж., Комптон К.К., Левин М.С. и другие. Атлас клинической гастроэнтерологии. — М.: ООО «Рид Элсивер», 2010. — 392 с.
- Министерство здравоохранения РФ. Российская гастроэнтерологическая ассоциация. Язвенная болезнь у взрослых / Клинические рекомендации. — 2016.
- Ивашкин В. Т. и др. Диагностика и лечение язвенной болезни у взрослых (Клинические рекомендации Российской гастроэнтерологической ассоциации, Российского общества колоректальных хирургов и Российского эндоскопического общества) // Российский журнал гастроэнтерологии, гепатологии и колопроктологии. — 2020. — № 1. — С. 49-70.
Язва желудка и двенадцатиперстной кишки лечение схема лечения
(1).jpg)
Об актуальных изменениях в КС узнаете, став участником программы, разработанной совместно с АО »СБЕР А». Слушателям, успешно освоившим программу, выдаются удостоверения установленного образца.
15 июня 2023
Программа разработана совместно с АО »СБЕР А». Слушателям, успешно освоившим программу, выдаются удостоверения установленного образца.
Продукты и услуги Информационно-правовое обеспечение ПРАЙМ Документы ленты ПРАЙМ Клинические рекомендации «Язвенная болезнь желудка и/или двенадцатиперстной кишки» (утв. Министерством здравоохранения РФ, 2021 г.)

Обзор документа
Клинические рекомендации «Язвенная болезнь желудка и/или двенадцатиперстной кишки» (утв. Министерством здравоохранения РФ, 2021 г.)
18 октября 2021
Кодирование по Международной статистической классификации болезней и проблем, связанных со здоровьем: K25, K26
Год утверждения (частота пересмотра): 2021
Возрастная категория: Дети
Год окончания действия: 2023
Разработчик клинической рекомендации
— Союз педиатров России
— Межрегиональная ассоциация по клинической микробиологии и антимикробной химиотерапии
— Общероссийская общественная организация «Российская ассоциация детских хирургов»
— Автономная некоммерческая организация «Общество детских гастроэнтерологов, гепатологов и нутрициологов»
Одобрено Научно-практическим Советом Минздрава РФ
Список сокращений
АБС — абдоминальный болевой синдром
АД — артериальное давление
АФК — активные формы кислорода
БУТ — быстрый уреазный тест
ВНС — вегетативная нервная система
ВОПТ — верхние отделы пищеварительного тракта
ДПК — двенадцатиперстная кишка
ЖКТ — желудочно-кишечный тракт
ИПН — ингибиторы протонного насоса
ЛФК — лечебная физкультура
НПВП — нестероидные противовоспалительные препараты
H. pylori — Helicobacter pylori
СО — слизистая оболочка
УЗИ — ультразвуковое исследование
ЯБ — язвенная болезнь
ЯБДПК — язвенная болезнь двенадцатиперстной кишки
ЯБЖ — язвенная болезнь желудка
CMV — цитомегаловирус (герпес-вирус 5 типа)
EBV — Эпштейн-Барр вирус (герпес-вирус 4 типа)
HHV 1 типа — герпес-вирус человека 1 типа
HHV 2 типа — герпес-вирус человека 2 типа
Термины и определения
Новые и узконаправленные профессиональные термины в настоящих клинических рекомендациях не используются
1. Краткая информация по заболеванию или состоянию (группы заболеваний или состояний)
1.1 Определение заболевания или состояния (группы заболеваний или состояний)
Язвенная болезнь (ЯБ) — хроническое рецидивирующее мультифакторное заболевание, проявляющееся образованием язвенных дефектов в желудке и/или двенадцатиперстной кишке (ДПК) с возможным прогрессированием и развитием осложнений.
1.2 Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Патогенез ЯБ сводится к нарушению равновесия между факторами защиты слизистой оболочки желудка и ДПК и агрессивными свойствами желудочного и дуоденального содержимого [1].
Основными факторами, усиливающими агрессивные свойства желудочного и дуоденального содержимого, являются:
— увеличение массы обкладочных клеток желудка (часто наследственно обусловленное);
— нарушение нервной и гуморальной регуляции желудочной кислотопродукции;
— повышение выработки пепсиногена и пепсина;
— нарушение гастродуоденальной моторики (замедление или ускорение);
— заброс желчи в желудок.
— обсеменение слизистой оболочки желудка H. pylori.
Основными факторами, ослабляющими защитные свойства слизистой оболочки желудка и ДПК являются:
— нарушение клеточной регенерации;
— нарушение местного кровотока (локальная ишемия);
— снижение продукции слизи и интенсивности муцинообразования и продукции сиаловых кислот;
— снижение продукции бикарбонатов поджелудочной железой;
— антродуоденальный кислотный тормоз;
— уменьшение содержания простагландинов в слизистой оболочке желудка и ДПК;
— прием препаратов групп «Другие анальгетики и антипиретики» и/или «Нестероидные противовоспалительные и противоревматические препараты» (нестероидные противовоспалительные препараты — НПВП).
Кроме НПВП причиной развития язвенного процесса является прием анаболических стероидов (стероидных препаратов), противоопухолевых препаратов (цитостатических препаратов) и иммунодепрессантов [2].
На состояние равновесия между факторами защиты и агрессии также влияют такие инфекционные агенты, как Candida albicans, герпес-вирусы (HHV 1 и 2 типа, EBV, CMV).
Представители Prevotella spp. и Streptococcus spp. в составе бактериальных сообществ могут принимать участие в развитии гастродуоденальной патологии [11].
Большое значение в развитии ЯБ имеет наследственная предрасположенность: при ЯБЖ она составляет 15-40%, а при ЯБДПК она может достигать 60-80% [3].
Наследственно-генетические факторы ассоциированы с увеличением желудочной кислотопродукции (генетически детерминированное увеличение массы обкладочных клеток и гиперактивностью секреторного аппарата СО); увеличением уровня гастрина и пепсиногена (сывороточного пепсиногена I), которое передается по аутосомно-доминантному типу; дефектом слизеобразования СОЖ и СОДК, проявляющимся в виде дефицита мукополисахаридов, в том числе фукогликопротеинов, синдрохондроитинсульфатов и глюкозаминогликанов; наличием определенных фенотипических полиморфизмов (группа крови I и II, отрицательный Rh-фактор, определенные виды HLA антигенов); в формировании ЯБ имеет значение полиморфизм генов матриксных металлопротеиназ-1, -3, -9 и тканевого ингибитора металлопротеиназ-3, носительство 607C- и -251T/A-аллелей гена провоспалительного IL-8, полиморфизм HLA — (HLA-DQB1*0602, DQB1*0301), особенности строения TLR-9 и TLR-4, белка теплового шока 70-2 [4, 5, 6].
В современной гастроэнтерологии решающая роль в развитии ЯБ отводится микроорганизму H. pylori, обнаруженному в 1983 г. австралийскими учеными Б. Маршаллом (B. Marshall) и Дж. Уорреном (J. Warren); позднее была доказана роль этой бактерии в том числе и в развитии язвенной болезни. Следует подчеркнуть, что у детей в отличие от взрослых инфицирование H. pylori намного реже сопровождается изъязвлением слизистой оболочки желудка и двенадцатиперстной кишки. По данным крупного европейского многоцентрового исследования, у 1233 детей с симптоматической H. pylori-инфекцией, ЯБ была диагностирована менее чем у 5% детей до 12 лет и лишь у 10% подростков [19].
Доказано как прямое повреждающее действие H. pylori на слизистую оболочку желудка и ДПК за счет выработки комплекса ферментов (уреаза, протеазы, фосфолипазы) и цитотоксинов (VacA, CagA), так и опосредованное повреждение слизистой оболочки за счет высвобождения интерлейкинов, лизосомальных энзимов, фактора некроза опухоли с развитием воспалительных процессов. Развитие в процессе персистирования в слизистой и подслизистой оболочках желудка и ДПК H. pylori приводит к формированию хронического гастрита и дуоденита с повышением продукции гастрина, усиливающего секрецию соляной кислоты. В то же время, избыточное закисление ДПК соляной кислотой при относительном дефиците панкреатических бикарбонатов, приводит к поддержанию воспалительного процесса в ДПК (прежде всего в луковице), появлению участков метаплазии слизистой оболочки ДПК с замещением кишечного эпителия на желудочный, который в свою очередь заселяется H. pylori. В дальнейшем при персистировании H. pylori именно на участках с метаплазией эпителия желудочного типа формируются язвенные дефекты. У детей до 18 лет обсеменённость слизистой оболочки антрального отдела желудка H. pylori при обострении ЯБДК отмечается у 33-100% (медиана 92%), при ЯБЖ — у 11-75% (медиана 25%); обсеменённость H. pylori при рецидивирующем язвенном процессе фиксируется от 0 до 81% случаев (медиана 22%) [7].
Более 2/3 детей развивающихся стран инфицируются до 2-летнего возраста и распространенность инфекции достигает 80-100% при этом наиболее важными факторами распространения являются плохие социально-экономические условия и плохое гигиеническое состояние [8, 9].
В развитии ЯБ немаловажную роль играет состояние иммунитета ребенка и связано как с дефектами иммунной реактивности организма (наследственной или приобретенной природы), так и воздействием на иммунную систему факторов патогенности H. pylori и расстройством микробиоты верхних отделов пищеварительного тракта (ВОПТ). Исследования состояния иммунной системы у детей с ЯБДК, ассоциированной с H. pylori инфекцией, выявили наличие нарушений иммунного статуса, связанных с дисбалансом в системе цитокинов (IL-1, IL-4, IL-6, IL-8, IL-10, IL-12, , ), повышением уровня IgG-антител к тканевым (органоспецифическим и органонеспецифическим) и бактериальным антигенам, усилением продукции нейтрофилами активных форм кислорода (АФК). Выявленная у детей с ЯБДК продукция антител класса IgG к структурам тканей организма (эластину, коллагену, денатурированной ДНК) и к антигенам тканей желудочно-кишечного тракта (ЖКТ) — к антигенам желудка, тонкой и толстой кишки, поджелудочной железы, может служить указанием на развитие аутоиммунного процесса при обострении ЯБДК у детей. Выработка аутоантител к тканям желудка при инфицировании H. pylori доказана и у взрослых. Усиление продукции АФК нейтрофилами у детей с ЯБДК указывает на участие секретируемых нейтрофилами токсических веществ в деструктивном процессе при ЯБДК [12].
Неблагоприятное течение может быть обусловлено такими дополнительными факторами как, нейроэндокринные — реализуются факторами APUD-системы (гастрин, бомбезин, соматостатин, секретин, холецистокинин, мотилин, энкефалины, ацетилхолин), мелатонин; нейропсихические — связаны с психотравмами, устойчивыми стрессами, в том числе конфликтами в семье. Выявляются особенности реагирования нервной системы больных с ЯБ (астенический и астеноневротический, ипохондрический, депрессивный синдромы), интраверсия и экстраверсия, эмоциональная неустойчивость, дистимические расстройства;
Этиологическая роль алиментарных факторов, ассоциированных с нерегулярным приёмом пищи, употреблением жареной, копченой пищи, продуктов с большим содержанием соли, экстрактивных веществ, ксенобиотиков (консервантов, усилителей вкуса и др.) хотя и обсуждается, однако в настоящее время не доказана.
Выделяется особая форма первичной ЯБ, называемая «идиопатической», развитие которой не ассоциировано с доказанным инфекционным процессом. Распространённость этой формы ЯБ по данным различных авторов колеблется от 39% до 73%. Причина развития язвенного процесса у этих больных до конца не выяснена и возможно связана с нарушением процессов нейро-гуморально-эндокринно-иммунной регуляции слизистой оболочки ЖКТ.
Таким образом, формирование ЯБ или возникновение рецидива заболевания может быть связано с течением H. pylori инфекции, у иммунокомпрометированных пациентов — персистированием герпетической инфекции, воздействием измененных сигнальных систем на местном и системном уровне, нарушением баланса между факторами агрессии и защиты слизистой оболочки ВОПТ. Наличие индивидуальных особенностей естественной резистентности слизистой оболочки, в том числе и к H. pylori, позволяет нейтрализовать или уменьшить «агрессивность» триггерных факторов развития ЯБ [13].
1.3 Эпидемиология заболевания или состояния (группы заболеваний или состояний)
По данным эпидемиологических исследований инфекция H. pylori в РФ обнаруживается у 65-92% взрослого населения. Инфицирование H. pylori среди детей РФ в возрасте 5-10 лет было выявлено у 29%, в возрасте 11-14 лет — у 56% [14, 15, 16, 17, 18].
По данным зарубежных авторов, риск развития ЯБДК или ЯБЖ у инфицированных H. pylori в течение жизни варьирует от 3% в США до 25% в Японии [10];
В Российской Федерации распространенность ЯБ у детей в последнее десятилетие снизилась в 1,5 раза и составляет 1,1-1,5 на 1000 детского населения [20]. ЯБЖ выявляется у 2 из 10 000 детей (в 8 раз реже, чем ЯБДПК). ЯБЖ и ЯБДК преимущественно встречаются у детей старше 7 лет. Единичные случаи обнаружения язв в дошкольном и раннем возрасте наиболее часто могут быть отнесены к симптоматическим язвам [3].
В то же время следует отметить, что, например, в США частота пептической язвы у детей снизилась в период 2000 г. — 2012 г. с 2,07 на 100 000 до 1,66 на 100 000 детского населения [21].
В структуре заболеваний ВОПТ ЯБ составляет 7-12%, встречается в 7 раз чаще в школьном возрасте и в 2 раза чаще среди жителей крупных городов. ЯБДПК диагностируется в 3-4 раза чаще, чем ЯБЖ. Дуоденальная локализация язвенного дефекта отмечается в 81-87% случаев (из них постбульбарная — в 2,4-2,8%), желудочная локализация — в 11-13%, двойная локализация — в 4-6% случаев [22].
Максимальная частота ЯДПК отмечается у девочек в 12-13 лет, а у мальчиков — в 14-15 лет. Половые различия в распространенности ЯБ у детей 4-8-летнего возраста отсутствуют, к 12-14 годам отмечается преобладание мальчиков над девочками 3:1, а к 18 годам оно составляет 5:1 [3, 23].
1.4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статической классификации болезней и проблем, связанных со здоровьем
Язва желудка (K25):
K25.0 — Острая с кровотечением
K25.1 — Острая с прободением
K25.2 — Острая с кровотечением и прободением
K25.3 — Острая без кровотечения или прободения
K25.4 — Хроническая или неуточненная с кровотечением
K25.5 — Хроническая или неуточненная с прободением
K25.6 — Хроническая или неуточненная с кровотечением и прободением
K25.7 — Хроническая без кровотечения или прободения
K25.9 — Не уточненная как острая или хроническая без кровотечения или прободения
Язва двенадцатиперстной кишки (K26):
K26.0 — Острая с кровотечением
K26.1 — Острая с прободением
K26.2 — Острая с кровотечением и прободением
K26.3 — Острая без кровотечения или прободения
K26.4 — Хроническая или неуточненная с кровотечением
K26.5 — Хроническая или неуточненная с прободением
K26.6 — Хроническая или неуточненная с кровотечением и прободением
K26.7 — Хроническая без кровотечения или прободения
K26.9 — Не уточненная как острая или хроническая без кровотечения или прободения
1.5 Классификация заболевания или состояния (группы заболеваний или состояний)
Общепринятой классификации ЯБ не существует.
В педиатрической практике наибольшее распространение получила классификация ЯБ по А.В. Мазурину, представленная в таблице 1.
Таблица 1. Классификация язвенной болезни
(по А.В. Мазурину 1984 г., с дополнениями В.Ф. Приворотского и Н.Е. Лупповой 2005 г., Цветковой Л.Н., 2009 г.)
| Фазы: 1. Обострение 2. Неполная клиническая ремиссия 3. Клиническая ремиссия | Локализация: — Желудок — Двенадцатиперстная кишка — Постбульбарные отделы — Двойная локализация | Форма: 1. Неосложнённая 2. Осложнённая — Кровотечение — Пенетрация — Перфорация — Стеноз привратника — Перивисцерит |
|---|---|---|
| Инфицирование H. pylori: 1. H. pylori — позитивная 2. H. pylori — негативная | ||
| Течение: 1. Впервые выявленная 2. Редко рецидивирующая (ремиссия более 3-х лет) 3. Непрерывно рецидивирующая (ремиссия менее 1 года) | ||
| Функциональная характеристика: Кислотность желудочного содержимого и моторика могут быть повышены, понижены или нормальными | ||
| Клинико-эндоскопические стадии язвенной болезни: 1 стадия — свежая язва 2 стадия — начало эпителизации язвенного дефекта 3 стадия — заживление язвенного дефекта при выраженном гастродуодените 4 стадия — клинико-эндоскопическая ремиссия | ||
| По клиническому течению: 1. Классическое 2. Атипичное 3. Бессимптомное | ||
| Сопутствующие заболевания: — Панкреатит — Эзофагит — Холецистохолангит | ||
Также различают ЯБ, которые возникают на фоне других заболеваний и связаны с особыми этиопатогенетическими факторами (Таблица 2)
Типы язв и их характеристика
| Типы язв | Причины | Клинические проявления |
|---|---|---|
| Стрессовые (вследствие ишемии слизистой оболочки) Локализация в желудке | Травма, в том числе черепно-мозговая (язвы Кушинга), при ожогах (язвы Курлинга), шоке, обморожениях и т.д. | Болевой синдром чаще отсутствует, первым признаком является остро возникшее кровотечение, реже — перфорация. |
| Медикаментозные (вследствие нарушения выработки простагландинов и слизи, снижения темпов регенерации) | Терапия НПВП, кортикостероидами системного действия Противоопухолевыми препаратами (цитостатиками) и др. | Чаще протекают бессимптомно, проявляются внезапно возникшим кровотечением. Иногда сопровождаются изжогой, болями в эпигастрии, тошнотой |
| Эндокринные | Сахарный диабет (изменяются сосуды подслизистого слоя по типу микроангиопатии, снижается уровень трофических процессов) | Локализуются в желудке, малосимптомны, иногда осложняются кровотечением. |
| Синдром Золлингера-Эллисона (выявляется выраженная гиперацидность, повышение гастрина в сыворотке крови) | Имеет крайне тяжёлое течение, множественная локализация язв, упорная диарея. | |
| Гиперпаратиреоз | Локализация чаще в ДПК, тяжелое течение с частыми рецидивами и склонностью к кровотечению и перфорации, характерны признаки повышенной функции паращитовидных желёз: мышечная слабость, боли в костях, чувство жажды, полиурия. | |
| Гепатогенные (нарушение кровотока в воротной вене, нарушение инактивации гистамина в печени, трофические и микроциркуляторные расстройства) | Цирроз печени, хронический гепатит | Локализуются чаще в желудке, реже в ДПК. Клиническая картина обычно стерта и атипична, язвы плохо поддаются терапии, отличаются торпидностью течения |
| Панкреатогенные (нарушение поступления бикарбонатов в кишечник при одновременном увеличении высвобождения кининов, гастрина) | Панкреатит | Локализуются обычно в ДПК. Для язв характерен выраженный болевой синдром, связь с приемом пищи. Течение язвенного процесса упорное, но осложнения наблюдаются редко. |
| Гипоксические (длительная гипоксия желудка) | Хронические заболевания легких и сердечно-сосудистой системы | Выраженная клиническая симптоматика, склонность к кровотечению |
По числу язвенных дефектов различают одиночные и множественные язвы; в зависимости от размеров язвенного дефекта выделяют язвы малых (до 0,5 см в диаметре), средних (0,6-1,9 см в диаметре) и больших (более 2,0 см в диаметре) размеров.
В диагнозе указывается стадия течения заболевания (обострения, заживления, рубцевания, ремиссия), а также наличие осложнений ЯБ (кровотечения, прободения, рубцово-язвенная деформация/стенозы желудка, двенадцатиперстной кишки.
1.6 Клиническая картина заболевания или состояния (группы заболеваний или состояний)
Клинические симптомы обострения ЯБ (боль в животе, диспептические расстройства и функциональные нарушения ВНС) не являются строго специфичными.
Наиболее частым, но наименее специфичным симптомом ЯБ является боль в животе. Только у 15-20% детей с болями в животе при обращении к врачам-гастроэнтерологам выявляются эрозивно-язвенные процессы.
Боль при типичном течении ЯБ достаточно интенсивная, локализуются в основном в эпигастральной и параумбиликальной области, возникает регулярно. Боль принимает ночной, «голодный» характер. Боль может быть ранней (возникает после приема пищи в течение 30-60 мин) и поздней (через 2-3 часа после еды). Возможна иррадиация боли в спину, правое плечо, лопатку, «мойнигановский» ритм боли: голод — боль — прием пищи — облегчение и т.д.
По характеру боли могут быть различными от ноющих до режущих и приступообразных, часто выявляется положительный симптом Менделя. Характер АБС зависит от возраста, индивидуальных особенностей больного, состояния его нервной и эндокринной систем, анатомических особенностей язвенного дефекта, степени выраженности функциональных нарушений ЖКТ. У 50% больных детей отсутствует параллелизм между эндоскопической стадией язвенного процесса и его клиническими проявлениями.
При атипичном течении заболевания (чаще в младшем возрасте) не определяется какая-либо закономерность возникновения и трансформации АБС, могут отсутствовать диспепсические жалобы, клиническая картина ЯБ протекает под «маской» болей в груди, холецистита, панкреатита, печеночной или почечной колики.
Согласно последним исследованиям, у 3% детей с впервые выявленной ЯБДК имеет место отсутствие АБС, что расценивается как первично безболевое течение заболевания, а у 27% детей отмечается вторично безболевое течение, когда на фоне повторного обострения язвенного процесса у детей, ранее получивших терапию, АБС отсутствует [12].
Желудочная диспепсия при ЯБ проявляется в виде рвоты, чувства тяжести или давления в подложечной области после еды, отрыжки, тошноты, жжения в эпигастрии и изжоги. В то же время следует отметить, что диспепсические расстройства у детей встречаются реже, чем у взрослых. С увеличением продолжительности заболевания частота симптомов диспепсии возрастает.
У части больных ЯБДК имеет место снижение аппетита, задержка физического развития, а также склонность к запорам или неустойчивый характер стула.
Прогрессирование заболевания так же, как и персистирование АБС сопровождается усилением эмоциональной лабильности, нарушением сна, повышенной утомляемостью и другими проявлениями астенического и депрессивного синдромов.
Рецидив ЯБДК проявляется аналогичной клинической картиной, однако самостоятельный АБС выявляется реже, а болезненность при пальпации живота отмечается примерно у 2/3 детей [13].
2. Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
Критерии установления диагноза/состояния
При постановке диагноза следует обратить внимание на:
1. анамнестические данные (характерные жалобы, рефрактерная к терапии железодефицитная анемия, семейный анамнез);
2. физикальное обследование (обнаружение болезненности с характерной локализацией, диспепсические расстройства, снижение веса);
инструментальным обследованием (обнаружение язвенного дефекта при эндоскопическом исследовании желудка и двенадцатиперстной кишки)
2.1 Жалобы и анамнез
См. раздел «Клиническая картина»
Клинические проявления ЯБ многообразны, типичная картина наблюдается не всегда, что значительно затрудняет диагностику. Так, у детей раннего возраста заболевание нередко протекает атипично. При этом, чем моложе ребенок, тем менее специфичны жалобы. В старшем возрасте симптоматика ЯБДПК сходна с таковой у взрослых, хотя может быть и более стертой.
Нередко отсутствует характерный «язвенный» анамнез, что объясняется отчасти тем, что дети быстро забывают боли, не умеют их дифференцировать, не могут указать их локализацию и причину, их вызвавшую. Увеличение числа нетипичных форм заболевания, отсутствие настороженности в формировании язвенного процесса, особенно у детей с отягощенной наследственностью по патологии ВОПТ, способствует росту процента пациентов с поздней диагностикой ЯБ, что приводит к более частому рецидивированию заболевания у этой категории пациентов и раннему формированию его осложнений, приводящих к снижению качества жизни детей с ЯБ.
2.2 Физикальное обследование
При осмотре следует обратить внимание на наличие белого налета на языке.
При пальпации следует обратить внимание на болезненность в пилородуоденальной зоне.
Независимо от локализации язвы у детей очень часто отмечается болезненность в эпигастральной области и в правом подреберье.
В фазе обострения ЯБ следует оценить наличие положительного симптома Менделя (локальная перкуторная болезненность в эпигастральной области) [1, 24, 25].
Комментарии: симптом мышечной защиты передней брюшной стенки выявляется редко, чаще во время сильных болей.
2.3 Лабораторные диагностические исследования
Патогномоничных для язвенной болезни лабораторных маркеров нет. Лабораторные исследования детям с ЯБ проводятся для исключения/подтверждения осложнений.
— Рекомендовано проведение всем пациентам с ЯБ общего (клинического) анализа крови развернутого с целью комплексной диагностики анемии (гемоглобин, гематокрит, эритроциты, тромбоциты) [26]
Комментарий: исследование проводится также в процессе динамического наблюдения — частота определяется клинической ситуацией.
— Пациентам с ЯБ с дефицитом железа/анемией рекомендовано проведение исследования кала на скрытую кровь с целью диагностики скрытого кровотечения [27, 58] (УУР — C; УДД — 5).
Комментарии: При интерпретации исследования кала на скрытую кровь необходимо учитывать, что положительная реакция может встречаться при многих других заболеваниях, приеме некоторых лекарственных препаратов, употреблении в пищу мяса, зеленых частей растений.
— При рефрактерном течении ЯБ с целью исключения синдрома Золлингера-Эллисона рекомендуется исследование уровня гастрина в сыворотке крови и внутрижелудочное определение концентрации водородных ионов (pH) в желудочном содержимом (тощакового гастрина в сыворотке крови и определение pH в желудочном содержимом) [27]
Комментарий: Синдром Золлингера-Эллисона характеризуется резким увеличением секреции соляной кислоты в результате развития у пациента гастринпродуцирующей опухоли, которая чаще всего локализуется, либо в проксимальной части 12-перстной кишки, либо в поджелудочной железе. В большинстве случаев синдром Золлингера-Эллисона ассоциируется с MEN-1 (синдромом Вермера) [28]. При синдроме Золлингера-Эллисона часто развиваются множественные язвы с локализацией не только в желудке и ДПК, но и в тощей кишке и пищеводе, протекающие с выраженным болевым синдромом и диареей. Обследование таких пациентов выявляет резкое повышение базального уровня желудочной секреции соляной кислоты и увеличение концентрации гастрина в сыворотке крови натощак в 10 раз и более относительно верхней границы нормы. Уровень тощакового гастрина 1000 пг/мл в сочетании с pH в желудке ниже 2 является диагностическим критерием для постановки диагноза [29].
— Всем пациентам с ЯБ для определения показаний к проведению эрадикационной терапии показано обследование на наличие инфицированности H. pylori с помощью дыхательного теста и/или определения антигена хеликобактера пилори в фекалиях или Иммунохроматографическое экспресс-исследование кала на геликобактер пилори (Helicobacter pylori), при одновременном проведении в ходе ЭГДС быстрого уреазного теста (БУТ). Для контроля успешности эрадикации через 4-6 недель после окончания лечения рекомендовано применение дыхательного теста или определение антигена хеликобактера пилори в фекалиях [11].
Комментарии: Чувствительность дыхательного теста по данным Кокрейновского обзора и метаанализа составляет 94% (95% ДИ: 0,89-0,97), а определение антигена H. pylori в кале — 83% (95% ДИ: 0,73-0,90) при фиксированной специфичности в 90% [30].
Следует помнить, что проведение дыхательного теста может дать ложноположительный результат у детей младше 6 лет из-за меньшего объема распределения и другой скорости продукции [31].
При использовании быстрого уреазного теста для диагностики H. pylori во время эндоскопического вмешательства необходимо осуществлять забор не менее 2 биоптатов: 1 — из тела и 1 — из антрального отдела желудка [32].
Использование микробиологического (культурального) исследования биоптатов стенки желудка на H. pylori с определением чувствительности к антибактериальным препаратам (в т.ч., при необходимости и возможности, молекулярно-биологическими методами (ПЦР) и методами флуоресцентной гибридизации) возможно в случае неэффективности эрадикационной терапии первой и второй линии [11]. Также при наличии возможности, следует сделать тесты для определения чувствительности или резистентности к кларитромицину (таблетки с 12 лет** и #гранулы для приготовления суспензии для приема внутрь**) и метронидазолу**. С этой целью при исследовании полученных в ходе ЭГДС биоптатов, могут быть использованы E-test, диско-диффузионный метод, ПЦР в реальном времени, FISH-тест [11, 33].
— Не рекомендуется применение серологических тестов для первичной диагностики H. pylori инфекции и контроля эрадикации у детей в связи с недостаточной информативностью [33, 34]
Комментарии: Клиническое применение теста ограничено тем, что он не позволяет дифференцировать факт инфицирования в анамнезе от наличия H. pylori в настоящий момент и контролировать эффективность эрадикации. Не все серологические тесты равноценны.
— У пациентов, которые получают ингибиторы протонного насоса (ИПН) и/или антибактериальные препараты системного действия, рекомендовано приостановить прием ИПН на 2 недели, а антибактериальных препаратов системного действия и препаратов висмута на 4 недели перед тестированием с помощью бактериологического, патолого-анатомического (гистологического) методов, быстрого уреазного теста, дыхательного теста или выявления антигена H. pylori в кале [11, 33, 35, 36]
— При наличии у пациента язвенного кровотечения для определения инфицированности H. pylori рекомендуется проведение дыхательного теста в связи с низкой чувствительностью БУТ и патолого-анатомического (гистологического) исследования биоптатов слизистой оболочки желудка [37, 38]
Комментарии: На фоне кровотечения чувствительность диагностики H. pylori снижается, поэтому при отрицательном результате теста рекомендуется обследование и лечение инфекции в период ремиссии.
2.4 Инструментальные диагностические исследования
— Всем пациентам с подозрением на ЯБ, при отсутствии противопоказаний, для подтверждения диагноза рекомендуется проведение эзофагогастродуоденоскопии (ЭГДС) [38, 39, 40].
Комментарии: ЭГДС позволяет достоверно диагностировать и охарактеризовать язвенный дефект, контролировать его локализацию, форму, размеры, глубину, состояние дна и краев язвы, заживление дефекта, позволяет выявить признаки пенетрации, рубцовой деформации и стенозирования просвета органа, проводить патолого-анатомическую (гистологическую) оценку морфологической структуры слизистой оболочки, исключать злокачественный характер изъязвления.
При локализации язвенного процесса в желудке рекомендуется проведение биопсий из краев язвенного дефекта с последующим патолого-анатомическим исследованием биопсийного материала, позволяющим исключить злокачественный характер язвенного поражения.
Контрольное эндоскопическое исследование со взятием биопсии по окончании курса консервативного лечения ЯБЖ проводится пациентам, у которых сохраняются симптомы язвенной болезни или этиологическая причина язвенного процесса остается недостаточно ясной.
Контрольное эндоскопическое исследование со взятием биопсии по окончании курса консервативного лечения ЯБЖ следует проводить при персистировании симптомов для исключения рефрактерной язвы, если этиология язвы не была установлена при первичном обследовании и в том случае, если язва была диагностирована рентгенологически, а лечение было назначено без проведения эндоскопии [41].
При локализации язвенного процесса в ДПК, выполнение биопсии из краев язвенного дефекта не рекомендуется, так как озлокачествление язв ДПК является редким. В то же время, проведение патолого-анатомического (гистологического) исследования обязательно при подозрении на наличие изъязвленных форм нейроэндокринных и субэпителиальных опухолей, прорастание в ДПК опухолей соседних органов.
Контрольное патолого-анатомическое (гистологическое) исследование при ЯБДПК рекомендуется выполнить для исключения рефрактерной язвенной болезни и непептической этиологии язвы, если в процессе лечения сохраняется клиническая симптоматика.
Эндоскопическая картина стадий язвенного поражения приводится в Приложении А3.3.
— Проведение ЭГДС пациентам с язвенным кровотечением с целью верификации источника кровотечения и выполнения эндоскопического гемостаза рекомендуется проводить в течение 24 часов после госпитализации и только после стабилизации гемодинамики (при наличии гемодинамических нарушений) [42] Более раннее проведение ЭГДС показано при отсутствии контроля над кровотечением на фоне консервативной терапии [43, 44].
— В случае невозможности выполнения эндоскопического исследования пациенту с подозрением на ЯБ, с целью подтверждения диагноза рекомендуется проведение рентгенографии желудка и двенадцатиперстной кишки с контрастом (Рентгенография желудка и двенадцатиперстной кишки, с двойным контрастированием) [34, 45]
Комментарии: Основным признаком ЯБ при проведении рентгенологического исследования является выявление «ниши» на контуре или на рельефе слизистой оболочки, а косвенными признаками являются: выявление местного циркулярного спазма мышечных волокон на контралатеральной по отношению к язвенному дефекту стенке желудка в виде «указующего перста», конвергенция складок слизистой оболочки к «нише», рубцово-язвенная деформация желудка и луковицы ДПК, гиперсекреция натощак, нарушения гастродуоденальной моторики. В то же время рентгенологическое исследование позволяет оценить выраженность сужения просвета кишки, нарушения моторики и эвакуации из желудка и ДПК.
— Для диагностики осложнений и при подозрении на перфорацию или пенетрацию язвы рекомендуется выполнение ультразвукового исследования брюшной полости комплексного (УЗИ) [48, 49]
Комментарии: По данным УЗИ обращается вниманием на наличие пузырьков газа над передней поверхностью печени, что свидетельствует о наличии перфорации. Основным признаком является также наличие свободной жидкости со взвесью в левом поддиафрагмальном пространстве, вокруг селезенки, в полости малого сальника (при перфорации задней стенки желудка) и в малом тазу. При подозрении на наличие перечисленных ультразвуковых признаков показано выполнение компьютерной томографии органов брюшной полости.
Чувствительность и специфичность ультразвуковой диагностики ниже таковых по сравнению с компьютерной томографией и во многом зависит от квалификации специалиста по ультразвуковой диагностике, однако данный метод является неинвазивным, не несет лучевую нагрузку и может применяться повторно [49].
— При подозрении на перфорацию язвы с целью подтверждения диагноза рекомендуется проведение компьютерной томографии органов брюшной полости [46, 47].
Комментарии: Компьютерная томография позволяет определить наличие и локализацию перфорационного отверстия, наличие свободного газа в брюшной полости, объем и характер выпота и других патологических изменений.
2.5 Иные диагностические исследования
2.5.1 Дифференциальная диагностика
Дифференциальная диагностика язвенной болезни с функциональными нарушениями желудочно-кишечного тракта, хроническим гастродуоденитом, хроническими заболеваниями печени, желчевыводящих путей и поджелудочной железы проводится по данным анамнеза, осмотра, результатов лабораторного, эндоскопического, рентгенологического и ультразвукового исследований.
Язвенную болезнь необходимо дифференцировать с симптоматическими язвами, патогенез которых связан с определёнными фоновыми заболеваниями или конкретными этиологическими факторами. Клиническая картина обострения этих язв стерта, отсутствует сезонность и периодичность заболевания.
Язвы желудка и 12-перстной кишки могут являться клиническими проявлениями болезни Крона и специфических заболеваний желудочно-кишечного тракта.
Это может быть как при изолированном поражении желудка, так и в сочетании с любыми другими локализациями поражения при болезни Крона
3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
3.1 Консервативное лечение
3.1.1 Диетотерапия
— С целью ускорения заживления язв всем пациентам с ЯБ рекомендуется диетотерапия [50, 51, 58].
Комментарии: Основные принципы диетического питания пациентов с язвенной болезнью включают частое (5-6 раз в сутки), дробного питания, механического термического и химического щажения. Из пищевого рациона необходимо исключить продукты, способные повышать секрецию пищеварительных ферментов и соляной кислоты и/или раздражающие слизистую оболочку: крепкие мясные и рыбные бульоны, жареную и копченую, соленую, маринованную пищу, продукты содержащие экстрактивные вещества (перец, горчица, приправы, специи, лук, чеснок).
Предпочтение необходимо отдавать продуктам, обладающим способностью связывать и нейтрализовать соляную кислоту (т.е. обладающим буферным действием): мясо и рыба (отварные или приготовленные на пару), яйца, молоко и молочные продукты. Разрешаются макаронные изделия, черствый белый хлеб, сухой бисквит и сухое печенье, молочные и вегетарианские супы, овощи (картофель, морковь, кабачки, цветная капуста), каши, кисели из сладких ягод, муссы, желе, сырые тертые и печеные яблоки, некрепкий чай. Предпочтительным способом приготовления пищи является варка, тушение, приготовление на пару.
3.1.2 Медикаментозная терапия
— Всем пациентам с обострением ЯБ с целью заживления язвенного дефекта рекомендуется проведение антисекреторной терапии ингибиторами протонного насоса (ИПН) [52, 53]
Комментарии: Предпочтение при выборе среди препаратов для лечения язвенной болезни желудка и двенадцатиперстной кишки и гастроэзофагеальной рефлюксной болезни (антисекреторных препаратов) группе ИПН в сравнении с блокаторами рецепторов объясняется более высокой эффективностью первых в устранении клинических симптомов и достижении рубцевания язв по данным рандомизированных сравнительных исследований (включая метаанализы) [53, 54].
— #рабепразол (0,5 мг/кг/сут в 2 приема, максимальная суточная доза 20 мга) [59];
— #омепразол** (капсулы разрешены к применению для детей с 2-х летнего возраста и массой тела не менее 20 кг; дозировка: дети весом 15-24 кг по 20 мг x 2 раза в сутки; 25-34 кг — по 30 мг x 2 раза в сут; >35 кг по 40 мг x 2 раза в сут)) [33] или доза 1 мг/кг/сут в 2 приема, максимальная суточная доза 40 мг [59];
— #лансопразол 1,5 мг/кг/сут в 2 приема (максимальная суточная доза 60 мг) [59]
Если язвенная болезнь ассоциирована с инфекцией Helicobacter pylori предпочтение следует отдавать #эзомепразолу** и #рабепразолу, поскольку эти препараты имеют более высокий синергетический эффект с антибиотиками и в меньшей степени зависят от часто встречающегося в европейской популяции усиливающего метаболизм фенотипа CYP2C19 (быстрые метаболизаторы) [33] Если #эзомепразол** и #рабепразол не доступны, могут быть назначены #омепразол** или #лансопразол. Высокие дозы ИПН лучше подавляют кислотопродукцию, увеличивая pH, что повышает эффективность наиболее часто назначаемых амоксициллина** и кларитромицина (таблетки с 12 лет** и #гранулы для приготовления суспензии для приема внутрь**) [60].
— При неосложненной язве луковицы 12-перстной кишки длительность назначения ИПН совпадает с длительностью антибактериальной терапии (14 дней). Для заживления язвенного дефекта нет необходимости в назначении более длительного курса антисекреторной терапии [61]. Более длительное назначение ИПН показано пациентам, у которых после завершения курса лечения инфекции H. pylori сохраняются диспептические симптомы [62].
— При неосложненной язве желудка длительность антисекреторной терапии должна составлять не менее 8 недель (2 недели вместе с антибиотиками и еще 6 недель) [62].
— При осложненной язве луковицы 12-перстной кишки и желудка продолжительность антисекреторной терапии должна составлять 8-12 недель (включая прием ИПН в составе антихеликобактерной терапии) [63]
— Не рекомендовано рутинное назначение блокаторов рецепторов, данные препараты могут применяться при язвенной болезни, не ассоциированной с H. pylori, при невозможности применения ИПН (или в комбинации с ними) с целью усиления антисекреторного действия [55]
Комментарий: Данные препараты утратили свои позиции и в настоящее время применяются редко.
— Рекомендовано проведение эрадикационной терапии при ЯБ, ассоциированной с H. pylori с лечебной целью [33, 55]
Комментарии: Проведение эрадикационной терапии H. pylori у инфицированных пациентов среди взрослого населения снижает риск рецидива ЯБДПК (ОР = 0,20; 95% ДИ: 0,15-0,26) и ЯБЖ (ОР = 0,29; 95% ДИ: 0,20-0,42) в сравнении с плацебо [57]. У детей подобные исследования не проводились.
При выборе схемы лечения инфекции H. pylori необходимо учитывать следующие факторы: наличие лекарственной аллергии (в частности, к пенициллинам), возраст, наличие/отсутствие данных о чувствительности/резистентности к антибиотикам у пациента, региональные особенности антибиотикорезистентности H. pylori, наличие факторов риска вторичной резистентности H. pylori [11, 33].
Следует выбирать схемы лечения, эффективность которых выше 90% [64, 65].
Продолжительность лечения инфекции H. pylori должна составлять 14 дней [11, 33].
Увеличение продолжительности эрадикационной терапии до 14 дней обеспечивает более высокую эффективность в сравнении с применяемой ранее 7-10-дневной терапией.
Наибольшей активностью в отношении инфекции H. pylori у детей обладают амоксициллин**, #метронидазол** (дозировка: дети весом 15-24 кг — 250 мг x 2 раза в сут; 25-34 кг — 500 мг утро — 250 мг вечер; >35 кг — по 500 мг x 2 раза в сутки), кларитромицин** (таблетки для детей с 12 лет и #гранулы для приготовления суспензии для приема внутрь**) (дозировка: дети весом 15-24 кг — 250 мг x 2 раза в сутки; 25-34 кг — 500 мг утро — 250 мг вечер (750 мг в сутки), либо 375 мг x 2 раза в сутки если доступна суспензия; >35 кг — по 500 мг x 2 раза в сутки), #тетрациклин (детям, начиная с 8-летнего возраста; дозировка: 25-50 мг/кг/сут, разделив на 4 приема (макс. доза 2000 мг)), #фуразолидон (30 кг — по 200 мг 2 раза в день или 6-10 мг/кг/сут, разделив на 4 приема) [33, 56].
Среди макролидов наибольшей активностью в отношении к H. pylori обладает кларитромицин** (таблетки с 12 лет** и #гранулы для приготовления суспензии для приема внутрь**), а наименьшей — джозамицин** [66, 67].
— Наибольшее влияние на эффективность лечения инфекции оказывает резистентность H. pylori к кларитромицину** (таблетки с 12 лет** и #гранулы для приготовления суспензии для приема внутрь**), #метронидазолу**, а также резистентность к обоим антибиотикам (двойная резистентность) [64].
— По данным метаанализа, включающим данные 11 исследований в 8 городах России, резистентность H. pylori к кларитромицину** (таблетки с 12 лет** и #гранулы для приготовления суспензии для приема внутрь**) у взрослых пациентов в Москве, Смоленске, Новосибирске, Казани, Ярославле и Владивостоке составляет менее 15%, что позволяет в этих городах включать данный антибиотик в схемы первой линии без предварительного тестирования. [68].
— У детей, проживающих в Санкт-Петербурге и Уфе, резистентность H. pylori к кларитромицину** (таблетки с 12 лет** и #гранулы для приготовления суспензии для приема внутрь**) превышает пороговые 15% [69], что при включении в схему этого препарата, не позволяет достичь целевой (>90%) эффективности лечения инфекции в этих городах [64].
— Преодолеть устойчивость к кларитромицину** (таблетки с 12 лет** и #гранулы для приготовления суспензии для приема внутрь**) не представляется возможным [64].
— Резистеность к #метронидазолу** во многих регионах России находится в диапазоне 15,3% — 55,6% [68, 70].
— Устойчивость к #метронидазолу** может быть преодолена с помощью назначения высоких доз препарата, включением в схему лечения #висмута трикалия дицитрата** и увеличением продолжительности лечения до 14 дней [71, 72].
— Риск вторичной устойчивости к кларитромицину** (таблетки с 12 лет** и #гранулы для приготовления суспензии для приема внутрь**) и #метронидазолу** существенно повышается в случае приема любых макролидов (эритромицина**, азитромицина**, джозамицина** и кларитромицина** (таблетки с 12 лет** и #гранулы для приготовления суспензии для приема внутрь**)) и/или производные имидазола в анамнезе [73, 74].
— Для выбора оптимальной схемы и снижения риска неудачного лечения инфекции H. pylori следует выяснить принимал ли пациент ранее макролиды и производные имидазола [75].
При наличии возможности, следует сделать тесты для определения чувствительности или резистентности к кларитромицину** (таблетки с 12 лет** и #гранулы для приготовления суспензии для приема внутрь**) и #метронидазолу**. С этой целью при исследовании полученных в ходе ЭГДС биоптатов, могут быть использованы E-test, диско-диффузионный метод, ПЦР в реальном времени, FISH-тест [33].
При отсутствии технической возможности проведения бактериологического исследования, ПЦР или FISH-теста, выбор схемы лечения должен быть основан на данных о распространенности устойчивых штаммов H. pylori в конкретном регионе [33, 65].
Резистентность к амоксициллину**, #тетрациклину, #фуразолидону встречается редко, что позволяет включать эти препараты в первую линию терапии, а также повторно их использовать в случае неудачи [76, 77, 78].
— В качестве терапии первой линии согласно рекомендациям V Маастрихтского соглашения (2016 г.), ESPGHAN/NASPGHAN (2016 г.), в большинстве случаев, можно без предварительного тестирования использовать стандартную тройную терапию в течение 14 дней: ИПН (#эзомепразол**, #рабепразол, #омепразол** и др.) + амоксициллин** + кларитромицин** (таблетки с 12 лет** и #гранулы для приготовления суспензии для приема внутрь**) или #метронидазол** Дозировки препаратов указаны в Приложении А3.4 [11].
— Добавление #висмута трикалия дицитрата** (дозировка 8 мг/кг/сут, разделив на 4 приема) к стандартной тройной терапии повышает ее эффективность. Схема #висмута трикалия дицитрат** + ИПН + амоксициллин** + кларитромицин** (таблетки с 12 лет** и #гранулы для приготовления суспензии для приема внутрь**) или #метронидазол** также рекомендуется в качестве терапии первой линии [58].
Комментарии: имеются данные по возможности применения джозамицина** в качестве альтернативы кларитромицину (таблетки с 12 лет** и #гранулы для приготовления суспензии для приема внутрь**), преимущественно у взрослых пациентов [79, 80], показания к применению при хеликобактерной инфекции у детей включены в инструкцию к препарату. Применение джозамицина** возможно, однако требуется проведение дальнейших исследований для уточнения места данного препарата в схемах антихеликобактерной терапии.
В регионах с высоким уровнем резистентности хеликобактера к кларитромицину** (таблетки с 12 лет** и #гранулы для приготовления суспензии для приема внутрь**) используются схемы без макролидов.
— При непереносимости Бета-лактамных антибактериальных препаратов: пенициллинов** в регионах с уровнем резистентности к кларитромицину** (таблетки с 12 лет** и #гранулы для приготовления суспензии для приема внутрь**) ниже порогового рекомендовано рассмотреть использование схемы ИПН + кларитромицин** (таблетки с 12 лет** и #гранулы для приготовления суспензии для приема внутрь**) + #метронидазол** [58].
Комментарии: учитывая высокую резистентность к метронидазолу** на территории Российской Федерации данная схема является альтернативной и должна применяться с осторожностью [81].
Возможно применение комбинации ИПН + #тетрациклин + #метронидазол**, ИПН + кларитромицин (таблетки с 12 лет ** и #гранулы для приготовления суспензии для приема внутрь**) + #тетрациклин, ИПН + #метронидазол** + #фуразолидон, в т.ч., в сочетании с #висмута трикалия дицитратом** (Приложение А3.4)
— Как вариант эрадикационной терапии (например, при непереносимости Бета-лактамных антибактериальных препаратов: пенициллинов** и при неэффективности стандартной тройной терапии) может быть назначена классическая четырехкомпонентная терапия на основе #висмута трикалия дицитрата** в комбинации с ИПН, #тетрациклином (разрешен детям с 8 лет) и #метронидазолом** (вторая линия терапии или альтернативный вариант первой линии терапии) [11, 81].
Комментарии: Квадротерапия с #висмута трикалия дицитратом** применяется так же, как основная схема терапии второй линии при неэффективности стандартной тройной терапии.
В случае плохой переносимости #тетрациклина у детей по рекомендациям российских экспертов как вариант эрадикационной терапии второй линии может быть рассмотрена для использования схема #висмута трикалия дицитрат** + ИПН + амоксициллин» + нифурател (30 мг/кг/сут) [82, 83, 84].
По данным немногочисленных исследований у взрослых и детей эффективность 3х-компонентных 10-14-дневных схем, включавших нифурател в комбинации с амоксициллином**, ИПН или #висмута трикалия дицитратом** составляет 82,9-86,0% (ITT) [84, 85, 86]. Учитывая небольшое количество пациентов, включенных в исследования, недостатки дизайна (отсутствие определения чувствительности H. pylori, контроль эффективности терапии одним тестом (а не двумя), а также показатель эффективности менее пороговых 90%, необходимо проведение более масштабных хорошо спланированных исследований для определения места нифуратела в лечении инфекции H. pylori [77].
#фуразолидон является недорогим и высоко эффективным в отношении H. pylori препаратом, к которому, практически не встречается ни первичная, ни вторичная резистентность [78]. #фуразолидон может быть включен в 4х-компонентные схемы вместо кларитромицина** (таблетки с 12 лет** и #гранулы для приготовления суспензии для приема внутрь**) и #тетрациклина в качестве терапии второй линии [87]. Эффективность 14-дневной 4х-компонентной схемы лечения, включающей #фуразолидон (ИПН + #висмута трикалия дицитрат** + амоксициллин** + #фуразолидон) составляет 90-99%, в том числе у пациентов с резистентностью штаммов H. pylori к #метронидазолу** и кларитромицину** (таблетки с 12 лет** и #гранулы для приготовления суспензии для приема внутрь**) [78]. Ограничивают широкое применение #фуразолидона частые побочные эффекты (тошнота, рвота и др.) [88, 89].
— При неэффективности эрадикационной терапии рекомендовано проводить индивидуальный подбор препарата на основе чувствительности H. pylori к антибактериальным препаратам — терапия третьей линии [55].
Комментарии: Неудачное лечение может быть связано с несоблюдением режима приема препаратов и развитием побочных эффектов [75]. Частота нежелательных эффектов эрадикационной терапии по результатам систематического обзора 43 исследований (6093 взрослых пациента) — 60%: диарея — 8%, изменение вкуса — 7%, тошнота и рвота — 5%, боль в эпигастрии — 5%, головная боль — 3%, стоматит — 2,5%, крапивница — 2% [57].
В ряде работ показана более высокая эффективность и безопасность антихеликобактерной терапии на фоне пребиотической или пробиотической терапии [90, 91]. Это, вероятно, связано со снижением частоты и выраженности побочных эффектов антибиотиков (диарея, тошнота, рвота, диспепсия, дисфагия) на фоне назначении Lactobacillus rhamnosus и Saccharomyces boulardii (p < 0,05) [11, 92, 93, 94]. Опубликован ряд метаанализов по данной теме [98, 99, 100, 101, 102].
Контроль эффективности эрадикации определяется не ранее чем через 4-6 нед. после окончания лечения антибактериальными препаратами системного действия и через 2 недели после окончания приема ИПН [33].
— Для оценки эффективности антихеликобактерной терапии у детей с ЯБ рекомендовано применять следующие неинвазивные тесты: дыхательный тест или определение антигенов Хеликобактер пилори в фекалиях (2х-этапный тест) [33]
— Не рекомендуется в большинстве случаев проведение эндоскопического контроля заживления язвенного дефекта у детей. Контрольная ЭГДС рекомендована в следующих ситуациях: персистирование симптомов после отмены ИПН (исключение рефрактерной язвы), осложненное течение язвы, неизвестна этиология язвы, язва была диагностирована рентгенологически (ЭГДС не проводили), есть подозрение на злокачественную природу язвы (чаще у взрослых) [34].
— В случае неэффективности терапии первой линии, при наличии возможности, рекомендуется повторить ЭГДС и биопсию с целью определения чувствительности H. pylori к антибиотикам. Если проведение тестов для определения чувствительности/резистентности H. pylori к антибиотикам не возможно, то при назначении терапии второй линии рекомендуется исходить из предположения о наличии у пациента устойчивости к макролидам и #метронидазолу** и отдавать предпочтение 14-дневным 4х-компонентным схемам на основе #висмута трикалия дицитрата**, высоких доз ИПН, высоких доз амоксициллина** и #метронидазола**, #тетрациклина и #фуразолидона [26, 78, 87].
Комментарий: После неудачной терапии инфекции H. pylori вторичная резистентность для кларитромицина (таблетки с 12 лет ** и #гранулы для приготовления суспензии для приема внутрь**) составляет 15-67%, а для #метронидазола** — 30-65% [76].
Для детей старше 8 лет наиболее эффективными схемами лечения являются:
— #Висмута трикалия дицитрат + ИПН + #Метронидазол ** + #Тетрациклин
— #Висмута трикалия дицитрат + ИПН + Амоксициллин ** + #Метронидазол**
Детям младше 8 лет могут быть назначены следующие схемы лечения:
— #Висмута трикалия дицитрат + ИПН + Амоксициллин ** + #Метронидазол**
— #Висмута трикалия дицитрат + ИПН + Амоксициллин ** + #Фуразолидон 1
— #Висмута трикалия дицитрат + ИПН + #Метронидазол** + #Фуразолидон 1
Дозировки препаратов см. Приложение А3.4 «Схемы лечения инфекции H. pylori и рекомендуемые дозы препаратов для антихеликобактерной терапии».
— В лечении НПВП-индуцированных язв рекомендовано применять ИПН в стандартных дозах. Если НПВП отменены, то продолжительность антисекреторной терапии составляет 4-8 недель. Если пациент вынужден длительно принимать нестероидные противовоспалительные препараты, то рекомендуется продолжить прием ИПН в течение всего курса НПВП [55].
— В лечении язв, не ассоциированных ни с H. pylori, ни с НПВП рекомендовано применять стандартные дозы ИПН [95]. Через 4-8 недель после начала антисекреторной терапии следует сделать повторную ЭГДС и еще раз проанализировать возможные причины ульцерогенеза (не выявленная инфекция H. pylori, прием ульцерогенных препаратов, мастоцитоз, болезнь Крона, эозинофильный гастрооэнтерит, васкулит, синдром Золлингера-Эллисона, цирроз, хроническая почечная недостаточность, диабет 1 типа, вирусные и грибковые инфекции у иммунокопрометированных пациентов). Если гастродуоденальные язвы являются вторичными или не удается выявить причину ульцерогенеза, то рекомендуется длительная антисекреторная терапия [96].
— С целью остановки кровотечения всем пациентам с лабораторно и эндоскопически подтвержденным язвенным кровотечением рекомендуется внутривенное введение ИПН (например, #омепразол**, #эзомепразол**, #рабепразол и др. — в дозе 1-3 мг/кг в течение 1 часа) [103, 104, 105] (УУР C; УДД — 5).
Комментарии: Внутривенное введение ИПН способствует значительному снижению риска повторных кровотечений (ОШ 2,24, 95% ДИ: 1,02-4,90). Доза ИПН, вводимая внутривенно болюсно аналогична таковой, рекомендуемой для перорального приема. Эрадикационная терапия проводится при переходе на пероральный прием препаратов.
3.2 Хирургическое лечение
— Рекомендовано проведение хирургического лечения язвенной болезни желудка при наличии осложнения болезни: перфорация язвы, декомпенсированный рубцово-язвенный стеноз привратника, сопровождающийся выраженными эвакуаторными нарушениями; профузные желудочно-кишечные кровотечения, которые не удается остановить консервативными методами, в том числе и с применением эндоскопического гемостаза [104, 106, 107, 108] (УУР B; УДД — 3).
Комментарии: Пациентам с осложненным течение ЯБ необходима госпитализация в хирургический стационар в экстренном порядке. При выборе метода хирургического лечения предпочтение отдают органосохраняющим операциям.
Эндоскопическая остановка кровотечения является «золотым стандартом» в лечении пациентов с язвенным кровотечением, позволяющим достичь устойчивого гемостаза в 82-92% случаев. Наиболее эффективным эндоскопическим способом остановки кровотечения является клипирование кроветочащего сосуда и аргоно-плазменная коагуляция. Другие методы эндоскопической остановки кровотечения, такие как нанесение препаратов для лечения язвенной болезни желудка и двенадцатиперстной кишки и гастроэзофагеальной рефлюксной болезни — пленкообразующих препаратов, использование полисахаридной гемостатической системы, электрокоагуляция, обкалывание язвы должны использоваться в комбинации с основными методами.
Случаи язвенных кровотечений у детей встречаются редко. По данным, основанным на взрослой популяции, факторами риска рецидива язвенного кровотечения являются:
— размер язвы более 1 см;
— расположение язвы на малой кривизне желудка;
— расположение язвы на задней стенке ДПК;
— нестабильная гемодинамика (снижение артериального давления во время кровотечения с последующим повышением на фоне восполнения объема циркулирующей крови [109].
— При неэффективности эндоскопического гемостаза, развитии перфорации, пенетрации язвы необходимо проведение экстренной операции [110]
4. Медицинская реабилитация, медицинские показания и противопоказания к применению методов реабилитации
В настоящее время убедительных доказательств того, что санаторно-курортное лечение, а также лечебная физкультура, улучшает прогноз или влияет на исходы нет.
Для окончательного вывода о необходимости данного лечения необходимо проведение более качественных исследований.
— Санаторно-курортное лечение рекомендуется рассмотреть после купирования обострения язвенного процесса, обычно через 2-3 месяца после обострения [111]
Комментарии: Продолжительность санаторно-курортного лечения — 14-21 день. В ранний период реабилитации предпочтение следует отдавать местным санаториям. Направление на курортное лечение в санатории, удаленные от места проживания возможно при формировании стойкой клинической ремиссии.
— Рекомендовано рассмотреть проведение лечебной физкультуры (ЛФК) (Лечебная физкультура при заболеваниях пищевода, желудка, двенадцатиперстной кишки) для улучшения крово- и лимфообращения в брюшной полости; нормализации моторики желудка и двенадцатиперстной кишки, секреторной и нейрогуморальной регуляции пищеварительных процессов; создания благоприятных условий для репаративных процессов в слизистой оболочке желудка и двенадцатиперстной кишки при отсутствии противопоказаний [111, 112, 113]
5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
5.1 Профилактика
— С целью профилактики обострения ЯБ всем пациентам с диагностированной хеликобактерной инфекцией рекомендуется проведение эрадикации H. pylori [11, 33, 114] (УУР C; УДД — 5).
Комментарии: Признание ведущей роли H. pylori в развитии и прогрессировании ЯБ делает эрадикацию основным методом профилактики данного заболевания.
5.2 Диспансерное наблюдение
— Рекомендуется проводить диспансерное наблюдение всех пациентов с ЯБ с целью профилактики обострений заболевания и своевременной терапии, снятие с диспансерного учета возможно при полной ремиссии в течение 5 лет от начала заболевания или обострения [24, 115, 116] (УУР — C; УДД — 5).
Комментарий: диспансерному учету подлежат даже пациенты с отсутствием морфологического субстрата язвы (клинико-эндоскопическая ремиссия).
Проводятся консультации врача-гастроэнтеролога, врача-педиатра или врача общей практики (семейного врача), в среднем, 1 раз в год, при необходимости — проводится обследование в соответствии с рекомендациями (см. раздел «Диагностика»)
6. Организация оказания медицинской помощи
Медицинская помощь детям с ЯБ может оказываться амбулаторно, в дневном стационаре, стационарно.
Виды медицинской помощи: плановая, неотложная, экстренная.
Дети с впервые выявленной ЯБ в фазе обострения должны пройти обследование и лечение в условиях отделений гастроэнтерологического или педиатрического профиля, при неосложненных язвах — амбулаторно, при наличии выявленных хирургических осложнений — в отделениях хирургического профиля [13].
Комментарии: Длительность пребывания в стационаре определяется индивидуально. Стационарное лечение пациентов с ЯБ в фазе ремиссии, как правило, нецелесообразно.
Дети с неосложнённым течением язвенной болезни подлежат консервативному лечению в амбулаторно-поликлинических условиях.
Дети в стадии ремиссии наблюдаются в амбулаторных условиях.
Детей с язвенной болезнью наблюдает врач-гастроэнтеролог или врач-педиатр, при необходимости осуществляется консультация/лечение врачом — детским хирургом.
Показания для стационарного лечения:
— ЯБ вне зависимости от фазы заболевания при наличии выраженных клинических проявлений обострения (выраженный болевой абдоминальный синдром, диспепсические жалобы); Осложненное и/или рецидивирующее течение ЯБ;
— Сочетание ЯБ с соматической патологией, в том числе желудочно-кишечного тракта;
— Необходимость проведения дифференциальной диагностики с доброкачественными и злокачественными новообразованиями.
7. Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
7.1 Исходы и прогноз
Прогноз благоприятный при неосложненной язвенной болезни. У большинства детей уже первый курс лечения в стационаре приводит к полному заживлению язвы и выздоровлению. В случае успешной эрадикации рецидивы язвенной болезни возникают у 6-7% пациентов. Прогноз ухудшается при большой давности заболевания в сочетании с частыми, длительными рецидивами, при осложнённых формах язвенной болезни.
7.2 Осложнения
Осложнения ЯБ в детском возрасте отмечаются у 7-10% пациентов. У мальчиков осложнения отмечаются чаще, чем у девочек в случае ЯБ ДПК (при изолированной ЯБДПК — в 2,3 раза, при сочетании ЯБ желудка и ДПК — в 8 раз). Удельный вес осложненных форм ЯБ наблюдается у детей всех возрастных групп с одинаковой частотой. В структуре осложнений преобладают кровотечения (80%), реже наблюдаются стенозы (11%), перфорации (8%) и пенетрации язвы (1,5%) [25, 116].
Кровотечение характеризуется кровью в рвотных массах (алая или рвота «кофейной гущей»), черным дегтеобразным стулом. При большой кровопотере характерны слабость, тошнота, бледность, тахикардия, снижение АД, иногда обморок. При скрытом кровотечении в кале определяется положительная реакция на скрытую кровь.
Стеноз пилоробульбарной зоны развивается обычно в процессе заживления язвы. В результате задержки пищи в желудке происходит его расширение с последующим развитием интоксикации, истощения. Клинически это проявляется рвотой пищей, съеденной накануне, усилением перистальтики желудка, особенно при пальпации и «шумом плеска», определяемого при толчкообразной пальпации брюшной стенки.
Пенетрация (проникновение язвы в соседние органы) возникает обычно на фоне длительного и тяжелого течения заболевания, неадекватной терапии. Сопровождается усилением болевого синдрома с иррадиацией в спину. Наблюдается рвота, не приносящая облегчения, возможна лихорадка.
Перфорация язвы в 2 раза чаще встречается при желудочной локализации язвы. Основной клинический признак перфорации — резкая внезапная («кинжальная») боль в эпигастральной области и в правом подреберье, часто сопровождающаяся шоковым состоянием. Отмечается слабый пульс, резкая болезненность в пилородуоденальной зоне, исчезновение печеночной тупости вследствие выхода воздуха в свободную брюшную полость. Наблюдается тошнота, рвота, задержка стула [25, 116].
Критерии оценки качества медицинской помощи
Таблица 1 — Критерии качества специализированной медицинской помощи детям при ЯБ
| N п/п | Критерии качества | Уровень достоверности доказательств | Уровень убедительности рекомендаций |
|---|---|---|---|
| 1. | Проведена ЭГДС всем пациентам с подозрением на язвенную болезнь (при отсутствии противопоказаний) | C | 5 |
| 2. | Выполнено определение инфицированности H. pylori при первичной диагностике — дыхательный тест или быстрый уреазный тест, или определение антигена H. pylori в фекалиях (Иммунохроматографическое экспресс-исследование кала на геликобактер пилори (Helicobacter pylori) или (при одновременном проведении ЭГДС) — с помощью быстрого уреазного теста (БУТ) и/или патолого-анатомическое (гистологическое) исследование биоптатов слизистой оболочки желудка | B | 2 |
| 3. | Проведена эрадикационная терапия (при выявлении Helicobacter pylori) | B | 2 |
| 4. | Выполнено лечение лекарственными препаратами группы ингибиторов протонного насоса (при отсутствии медицинских противопоказаний) | B | 2 |
Список литературы
1. Shay H., Sun D.C.H. Etiology and pathology of gastric and duodenal ulcer. In: Bockus H.L. Gastroenterology, Philadelphia — London: Saunders Elsevier, 1968: 420-465.
2. Guariso G., Gasparetto M. Update on Peptic Ulcers in the Pediatric Age. Hindawi Publishing Corporation. Ulcers, 2012. Article ID 896509, 9 pages. doi: 10.1155/2012/896509
3. Детская гастроэнтерология: руководство для врачей/под ред. проф. Н.П. Шабалова. — 3-е изд., перераб. и доп. — М.: МЕДпресс-информ, 2019. — 792 с: ил.
4. Shaymardanova E.K, Nurgalieva A.K, Khidiyativa I.M et al. Role of Allelic Genes of Matrix Metalloproteinases and Their Tissue Inhibitors in the Peptic Ulcer Disease Development. Genetika, 2016, 52(3): 364-75.
5. Yin Y.W., Hu A.M., Sun Q.Q. et al Association between interleukin-8 gene — 251T/A polymorphism and the risk of peptic ulcer disease: a meta-analysis. Hum Immunol, 2013, 74(1): 125-30. doi: 10.1016/j.humimm.2012.09.006
6. Trejo-de la O.A., Torres J., Sanchez-Zauco N. et al. Polimorphisms in TLR9 but not in TLR5 increase the risk for duodenal ulcer and after cytokine expression in the gastric mucosa. Innate Immun, 2015, 21(7): 706-13. doi: 10.1177/1753425915587130.
7. Macartur C., Saunders N., Feldman W. Helicobacter pylori, gastroduodenal disease and recurrent abdominal pain in children. JAMA. 1995; vol. 273: 729-734.
8. Rothenbacher D., Inceoglu J., Bode G. et al. Acquisition of Helicobacter pylori infection in a high-risk population occurs within the first 2 years of life. J Pediatr 2000; 136: 744-9.
9. B., Francavailla R. Helicobacter pylori Infection in Pediatrics. Helicobacter 2014; 19 (s1): 46-51. doi: 10.1111/hel.12158
10. Suerbaum S., Michetti P. Helicobacter pylori infection. N. Engl. J. Med. 2002; 347: 1175-86
11. Malfertheiner P., Megraud F., O′Morain C.A. et al. Management of Helicobacter pylori infection — the Maastricht V/Florence Consensus Report. Gut 2017; 66(1): 6-30.
12. Гуреев А.Н. Роль факторов иммунитета в развитии язвенной болезни двенадцатиперстной кишки у детей. Автореф. дисс. . канд. мед. наук., М.: 2007. 25 с.
13. Цветкова Л.Н. Язвенная болезнь у детей (алгоритм диагностики и лечебной тактики). ГОУ ВПО РГМУ Росздрава, 2009. 46 с.
14. Герман С.В. Распространенность инфекции H. pylori среди населения Москвы./С.В. Герман, И.Е. Зыкова, А.В. Модестова [и др.]//Российский журнал гастроэнтерологии, гепатологии, колопроктологии. — 2010. — Т. 20, N 2. — С. 25-30
15. Захарова Н.В. Распространенность хеликобактерной инфекции у пациентов гастроэнтерологического профиля в Санкт-Петербурге/Н.В. Захарова, В.И. Симаненков, О.А. Саблин [и др.]//Фарматека. — 2016. — N 5, Вып. 16. — С. 33-39
16. Ивашкин В.Т. Лечение инфекции Helicobacter pylori: Мейнстрим и новации/В.Т. Ивашкин, И.В. Маев, Т.Л. Лапина [и др.]//Российский журнал гастроэнтерологии, гепатологии, колопроктологии. — 2017. — Т. 27, N 4. — С. 4-21
17. Курилович С.А. Эпидемиология заболеваний органов пищеварения в Западной Сибири/С.А. Курилович, О.В. Решетников//Педиатрия. — 2002. — N 2. — С. 65-71
18. Щербаков П.Л. Эпидемиология инфекции Helicobacter pylori/П.Л. Щербаков//В кн. Ивашкин В.Т., Мегро Ф., Лапина Т.Л., ред. Helicobacter pylori: революция в гастроэнтерологии. — М.: Триада-X, 1999. — С. 14-20
19. Koletzko S., Richy F., Bontems P. et al. Prospective multicenter study on antibiotic resistance of Helicobacter pylori strains obtained from children living in Europe. Gut. 2006; 55(12): 1711-1716.
20. Корниенко Е.А., Шабалов Н.П., Эрман Л.В. Заболевания органов пищеварения/в кн.: Детские болезни: в 2 т. — 8-е изд. — СПб.: Питер, 2017. — Т. 1. — с. 585-796.
21. Munoz Abraham A.S., Osey H., Martino A., et al. Incidence and Outcomes of Perforated Peptic Ulcers in Children: Analysis of the Kid»s Inpatient Database and Report of Two Cases Treated by Laparoscopic Omental Patch Repair.//Journal of Laparoendoscopic & Advanced Surgical Techniques. — 2018. — Vol. 00. — p. 248-255. doi: 10.1089/lap.2018.0186
22. Мельникова И.Ю., Новикова В.П. Язвенная болезнь желудка и двенадцатиперстной кишки./в кн.: Детская гастроэнтерология: практическое руководство/под ред. И.Ю. Мельниковой. — М.: ГЭОТАР-Медиа, 2018. — с. 221-233
23. Цветкова Л.Н., Филин В.А., Нечаева Л.В., Горячева О.А., Гуреев А.Н. Язвенная болезнь у детей: особенности течения и выбора медикаментозной терапии на современном этапе//Рос вестн перинатол и педиат. 2008. N 5.
24. Авдеева Т.Г., Рябухин Ю.В., Парменова Л.П. и др. Детская гастроэнтерология. ГЭОТАР-Москва, 2009, С. 32-61
25. Гастроэнтерология детского возраста (под редакцией С.В. Бельмера и А.И. Хавкина) — Москва: ИД Медпрактика-М, 2011. — 420 с.
26. Tomizawa M., Shinozaki F., Hasegawa R. et al. Low haemoglobin levels are associated with upper gastrointestinal bleeding. Biomed Rep 2016; vol. 5(3): 349-352.
27. Romano C., Oliva S., Martellossi S., Miele E., Arrigo S., Graziani M.G., Cardile S., Gaiani F., de′Angelis G.L., Torroni F. Pediatric gastrointestinal bleeding: Perspectives from the Italian Society of Pediatric Gastroenterology. World J Gastroenterol. 2017 Feb 28; 23(8): 1328-1337 Kim H. Diagnostic and treatment approaches for refractory ulcers. Clin Endoscop 2015; vol. 48(4): 285-290.
28. Zhuang Z., Vortmeyer A.O., Pack S., et al. Somatic mutations of the MEN1 tumor suppressor gene in sporadic gastrinomas and insulinomas. Cancer Res. 1997 Nov 1; 57(21): 4682-6. PMID: 9354421.
29. Berna M.J., Hoffmann K.M., Serrano J., et al. Serum gastrin in Zollinger-Ellison syndrome: I. Prospective study of fasting serum gastrin in 309 patients from the National Institutes of Health and comparison with 2229 cases from the literature. Medicine (Baltimore). 2006 Nov; 85(6): 295-330. doi: 10.1097/01.md.0000236956.74128.76. PMID: 17108778
30. Best L.M., Takwoingi Y., Siddique S. et al. Non-invasive diagnostic tests for Helicobacter pylori infection. Cochrane Database Syst Rev 2018; vol. 3: CD012080
31. Leal Y.A., Flores L.L., Fuentes Panana E.M., Cedillo Rivera R., Torres J. 13C-urea breath test for the diagnosis of Helicobacter pylori infection in children: a systematic review and metaanalysis. Helicobacter. 2011; 16: 327-337
32. Moon S.W., Moon S.W., Kim T.H., et al. United rapid urease test is superior than separate test in detecting Helicobacter pylori at the gastric antrum and body specimens. Clin Endosc 2012; 45: 392-6.
33. Jones N.L., Koletzko S., Goodman K., Bontems P., Cadranel S., Casswall T., Czinn S., Gold B.D., Guarner J., Elitsur Y., Homan M., Kalach N., Kori M., Madrazo A., Megraud F., Papadopoulou A., Rowland M.; ESPGHAN, NASPGHAN. Joint ESPGHAN/NASPGHAN Guidelines for the Management of Helicobacter pylori in Children and Adolescents (Update 2016). J Pediatr Gastroenterol Nutr. 2017 Jun; 64(6): 991-1003
34. Bak-Romaniszyn L., S., Gil J., I. Choroba wrzodowa—etiopatogeneza, rozpoznawanie i leczenie [Peptic ulcer disease etiology, diagnosis and treatment]. Pol Merkur Lekarski. 2004; 17 Suppl 1: 128-32
35. Calvet X. Diagnosis of Helicobacter pylori infection in the proton pump inhibitor era. Gastroenterol Clin N Am. 2015; 44: 507-518
36. Peng C., Hu Y., Ge Z-M., Zou Q-M., Lyu N-H. Diagnosis and treatment of Helicobacter pylori infections in children and elderly populations. Chronic Diseases and Translational Medicine. 2019; 5: 243-251 https://doi.org/10.1016/j.cdtm.2019.12.003
37. Gisbert, J.P., Abraira V., Accuracy of Helicobacter pylori diagnostic tests in patients with bleeding peptic ulcer: a systematic review and meta-analysis. Am J Gastroenterol 2006; vol. 101(4): 848-863
38. Tam P.K., Saing H., Lau J.T. Diagnosis of peptic ulcer in children: the past and present. J Pediatr Surg. 1986 Jan; 21(1): 15-6
39. ASGE Standards of Practice Committee, Lightdale J.R., Acosta R., Shergill A.K., Chandrasekhara V., Chathadi K., Early D., Evans J.A., Fanelli R.D., Fisher D.A., Fonkalsrud L., Hwang J.H., Kashab M., Muthusamy V.R., Pasha S., Saltzman J.R., Cash B.D.; American Society for Gastrointestinal Endoscopy. Modifications in endoscopic practice for pediatric patients. Gastrointest Endosc. 2014 May; 79(5): 699-710.
40. Суринов В.А. Диагностические критерии язвенной болезни у детей//Пермский медицинский журнал. 2010. N 5. URL: https://cyberleninka.ru/article/n/diagnosticheskie-kriterii-yazvennoy-bolezni-u-detey (дата обращения: 28.06.2021).
41. ASGE Standards of Practice Committee, Banerjee S., Cash B.D., Dominitz J.A., Baron T.H., Anderson M.A., Ben-Menachem T., Fisher L., Fukami N., Harrison M.E., Ikenberry S.O., Khan K., Krinsky M.L., Maple J., Fanelli R.D., Strohmeyer L. The role of endoscopy in the management of patients with peptic ulcer disease. Gastrointest Endosc. 2010 Apr; 71(4): 663-8. doi: 10.1016/j.gie.2009.11.026. PMID: 20363407
42. Gralnek I.M., Stanley A.J., Morris A.J., et al. Endoscopic diagnosis and management of nonvariceal upper gastrointestinal hemorrhage (NVUGIH): European Society of Gastrointestinal Endoscopy (ESGE) Guideline — Update 2021. Endoscopy. 2021 Mar; 53(3): 300-332. doi: 10.1055/a-1369-5274. Epub 2021 Feb 10. PMID: 33567467
43. Thomson M., Belsha D. Endoscopic management of acute gastrointestinal bleeding in children: Time for a radical rethink. J Pediatr Surg. 2016 Feb; 51(2): 206-10.
44. Fox V.L. Gastrointestinal bleeding in infancy and childhood. Gastroenterol Clin North Am. 2000 Mar; 29(1): 37-66, v.
45. И.Н. Захарова, И.М. Османов, М.И. Пыков и др. Инструментальная диагностика функциональных нарушений желудочно-кишечного тракта в практике педиатра и детского гастроэнтеролога. Педиатрия (Прил. к журн. Consilium Medicum). 2018; 1: 79-89.
46. Ishiguro T., Kumagai Y., Baba H. et al. Predicting the amount of intraperitoneal fluid accumulation by computed tomography and its clinical use in patients with perforated peptic ulcer. Int Surg. 2014; vol. 99(6): 824-829
47. Baghdanian A.H., Baghdanian A.A., Puppala A.A. et al. Imaging manifestations of peptic ulcer disease on computed tomography. Semin Ultrasound CT MR 2018; vol. 39(2): 183-192.
48. Coppolino F., Gatta G., Di Grezia G. et al. Gastrointestinal perforation: ultrasonographic diagnosis. Crit Ultrasound J. 2013; vol. 5 (Suppl 1): S4
49. Picone D., Rusignuolo R., Midiri F. et al.. Imaging assessment of gastroduodenal perforations. Semin Ultrasound CT MR 2016; vol. 37(1), N 1: 16-22
50. Vomero M.D., Colpo E. Nutritional care in peptic ulcer. Arq Bras Cir Dig 2014; vol. 7(4): 298-302
51. Н.Н. Семенова, Т.Э. Боровик, Л.И. Дмитриенко Лечебное питание детей при заболеваниях желудка и двенадцатиперстной кишки. Медицинский совет. 2007; 3: 64-70.
52. Chan F.K.L., Lau J.Y.W. Peptic ulcer disease. In: Sleisenger and Fordtran′s Gastrointestinal and Liver Disease. 10th ed. Philadelphia: Saunders Elsevier; 2015: chap 14
53. Scally B., Emberson J.R., Spata E., et al. Effects of gastroprotectant drugs for the prevention and treatment of peptic ulcer disease and its complications: a meta-analysis of randomized trials//Lancet Gastroenterol Hepatol 2018; vol. 3(4): 231-241
54. Hu Z.H., Shi A.M., Hu D.M., Bao J.J. Efficacy of proton pump inhibitors for patients with duodenal ulcers: A pairwise and network meta-analysis of randomized controlled trial. Saudi J Gastroenterol 2017; vol. 23(1): 11-19
ва З.К.# Принципы лечения при язвенной болезни желудка у детей//Здоровье и образование в XXI веке. 2019. N 9
55. Бельмер С.В., Хавкин А.И. Гастроэнтерология детского возраста. Практическое руководства по детским болезням. Под ред. В.Ф. Коколиной, А.Г. Румянцева М: Медпрактика-М 2003; 2: 121-149
56. П.Л. Щербаков, А.С. Потапов, Е.С. Дублина, М.Ю. Щербакова, Г.А. Самсыгина, С.И. Эрдес, А.И. Логвинова, Л.В. Кудрявцева. Схема эрадикации штаммов Helicobacter pylori, резистентных к метронидазолу у детей. Вопросы современной педиатрии. 2007. Том 6. N 5
57. Ford A., Gurusamy K.S., Delaney B., Forman D., Moayyedi P. Eradication therapy for peptic ulcer disease in Helicobacter pylori-positive people. Cochrane Database of Systematic Reviews 2016. Issue 4. Art. No.: CD003840
58. Sierra D., Wood M., Kolli S., Felipez L.M. Pediatric Gastritis, Gastropathy, and Peptic Ulcer Disease. Pediatr Rev. 2018 Nov; 39(11): 542-549.
59. Kato S., Shimizu T., Toyoda S., et al; Japanese Society for Pediatric Gastroenterology, Hepatology and Nutrition. The updated JSPGHAN guidelines for the management of Helicobacter pylori infection in childhood. Pediatr Int. 2020 Dec; 62(12): 1315-1331.
60. Erah P.O., Goddard A.F., Barrett D.A., et al. The stability of amoxycillin, clarithromycin and metroni-dazole in gastric juice: relevance to the treatment of Helicobacter pylori infection. J Antimicrob Chemother 1997; 39: 5-12
61. Lam S.K., Ching C.K., Lai K.C., et al. Does treatment of Helicobacter pylori with antibiotics alone heal duodenal ulcer? A randomised double blind placebo controlled study. Gut. 1997 Jul; 41(1): 43-8. doi: 10.1136/gut.41.1.43. PMID: 9274470; PMCID: PMC1027226
62. Malfertheiner P., Megraud F., O»Morain C.A., et al; European Helicobacter Study Group. Management of Helicobacter pylori infection—the Maastricht IV/Florence Consensus Report. Gut. 2012 May; 61(5): 646-64. doi: 10.1136/gutjnl-2012-302084. PMID: 22491499
63. Vakil N.B. Peptic ulcer disease treatment and secondary prevention. UpToDate, April, 2020
64. Graham D.Y., Lee Y-C, Wu M-S. Rational Helicobacter pylori therapy: evidence-based medicine rather than medicine-based evidence. Clin Gastroenterol Hepatol 2014; 12: 177-86
65. Aguilera Matos I., Diaz Oliva S.E., Escobedo A.A., et al. Helicobacter pylori infection in children. BMJ Paediatr Open. 2020 Aug 3; 4(1): e000679. doi: 10.1136/bmjpo-2020-000679. PMID: 32818155; PMCID: PMC7402006
66. Дехнич Н.Н., Иванчик Н.В., Козлов Р.С. Сравнение in vitro активности различных макролидов в отношении Helicobacter pylori. Клиническая микробиология и антимикробная химиотерапия. 2018. Том 20, N 3; 192-197
67. Guslandi M. Review article: alternative antibacterial agents for Helicobacter pylori eradication. Aliment Pharmacol Ther. 2001 Oct; 15(10): 1543-7. doi: 10.1046/j.1365-2036.2001.01064.x. PMID: 11563992
68. Андреев Д.Н., Маев И.В., Кучерявый Ю.А. Резистентность Helicobacter pylori в Российской Федерации: метаанализ исследований за последние 10 лет. Терапевтический архив. 2020; 92(11): 24-30
69. Симаненков В.И., Захарова Н.В., Жебрун А.Б. и др. Резистентность Helicobacter pylori к антимикробным препаратам по результатам бактериологического тестирования Лечащий врач, 2015, окт
70. Кудрявцева Л.В. Биологические свойства Helicobacter pylori//Альманах клинической медицины, 2006 — T. XIV. — С. 39-46
71. Fischbach L., Evans E.L. Meta-analysis: the effect of antibiotic resistance status on the efficacy of triple and quadruple first-line therapies for Helicobacter pylori. Aliment Pharmacol Ther. 2007 Aug 1; 26(3): 343-57. doi: 10.1111/j.1365-2036.2007.03386.x. PMID: 17635369
72. Boltin D., Levi Z., Gingold-Belfer R., Gabay H., Shochat T., Schmilovitz-Weiss H., Dotan I., Birkenfeld S. Effect of Previous Nitroimidazole Treatment on Helicobacter pylori Eradication Success. J Clin Gastroenterol. 2020 Apr; 54(4): 333-337
73. McNulty C.A., Lasseter G., Shaw I. et al. Is Helicobacter pylori antibiotic resistance Surveillance needed and how can it be delivered? Aliment Pharmacol Ther. 2012; 35(10): 1221-1230
74. E., G.M., Szirtes I. et al. Primary and secondary clarithromycin resistance in Helicobacter pylori and mathematical modeling of the role of macrolides. Nat Commun 12, 2255 (2021)
75. Shah S.C., Iyer P.G., Moss S.F. AGA Clinical Practice Update on the Management of Refractory Helicobacter pylori Infection: Expert Review. Gastroenterology. 2021 Apr; 160(5): 1831-1841. doi: 10.1053/j.gastro.2020.11.059. Epub 2021 Jan 29. PMID: 33524402.
76. Savoldi A., Carrara E., Graham D.Y., et al. Prevalence of Antibiotic Resistance in Helicobacter pylori: A Systematic Review and Meta-analysis in World Health Organization Regions. Gastroenterology. 2018 Nov; 155(5): 1372-1382. e17. doi: 10.1053/j.gastro.2018.07.007. Epub 2018 Jul 7. PMID: 29990487; PMCID: PMC6905086
77. Nijevitch A.A., Idrisov B., Akhmadeeva E.N., Graham D.Y. Choosing optimal first-line Helicobacter pylori therapy: a view from a region with high rates of antibiotic resistance. Curr Pharm Des. 2014; 20(28): 4510-6. doi: 10.2174/13816128113196660728. PMID: 24180406; PMCID: PMC5314729
78. Lu H., Zhang W., Graham D.Y. Bismuth-containing quadruple therapy for Helicobacter pylori: lessons from China. Eur J Gastroenterol Hepatol. 2013 Oct; 25(10): 1134-40. doi: 10.1097/MEG.0b013e3283633b57. PMID: 23778309; PMCID: PMC3865448.
79. Liu W.Z., Xiao S.D., Hu P.J., et al. A new quadruple therapy for Helicobacter pylori using tripotassium dicitrato bismuthate, furazolidone, josamycin and famotidine. Aliment Pharmacol Ther. 2000 Nov; 14(11): 1519-22
80. Lazebnik L.B., Bordin D.S.; Research Group «Parad». [Management of patients with Helicobacter pylori-related illness in the ordinary clinical practice. Intermediate results of monitoring program]. Eksp Klin Gastroenterol. 2013; (5): 93-101
81. Бельмер С.В. Рекомендации по диагностике и лечению инфекции Helicobacter pylori: в поисках консенсуса для педиатров Лечащий врач; 2020 г.; N 3: 58-62
82. Стандарты диагностики и лечения кислотозависимых и ассоциированных с Helicobacter pylori заболеваний (четвертое Московское соглашение)/Методические рекомендации N 37 Департамента здравоохранения города Москвы. — М.: ЦНИИГ, 2010.
83. Nijevitch A.A., Shcherbakov P.L., Sataev V.U., et al. Helicobacter pylori eradication in childhood after failure of initial treatment: advantage of quadruple therapy with nifuratel to furazolidone. Aliment Pharmacol Ther. 2005 Nov 1; 22(9): 881-7
84. Nijevitch A.A., Sataev V.U., Akhmadeyeva E.N., et al. Nifuratel-containing initial anti-Helicobacter pylori triple therapy in children. Helicobacter. 2007 Apr; 12(2): 132-5
85. Дехнич Н.Н., Тряпышко А.А., Трушин И.В., и др. Нифурател в эрадикации инфекции Helicobacter pylori у взрослых: результаты рандомизированного сравнительного, клинического исследования. Клиническая микробиология и антимикробная химиотерапия. 2020; том 22, N 2, 119-127
86. Успенский Ю.П., Барышникова Н.В. Использование производных нитрофурана в схемах эрадикационной терапии первой линии. РМЖ, 2012, N 35, 1694
87. Cheng H., HU F.L. Furazolidone, amoxicillin, bismuth and rabeprazole quadruple rescue therapy for the eradication of Helicobacter pylori. World J Gastroenterol. 2009; 15: 860-64. doi: 10.3748/wjg.15.860
88. Graham D.Y., Lu H. Furazolidone in Helicobacter pylori therapy: misunderstood and often unfairly maligned drug told in a story of French bread. Saudi J Gastroenterol. 2012; 18: 1-2. doi: 10.4103/1319-3767.91724
89. Mohammadi M., Attaran B., Malekzadeh R., et al. Furazolidone, an Underutilized Drug for H. pylori Eradication: Lessons from Iran. Dig Dis Sci. 2017; 62(8): 1890-6. doi: 10.1007/s10620-017-4628-5
90. Boonyaritichaikij S., Kuwabara K., Nagano J., et al. Long-term administration of probiotics to asymptomatic pre-school children for either the eradication or the prevention of Helicobacter pylori infection. Helicobacter 2009; 14: 202-7
91. Fujimura S., Watanabe A., Kimura K., Kaji M. Probiotic mechanism of Lactobacillus gasseri OLL2716 strain against Helicobacter pylori. J. Clin. Microbiol. 2012; 50: 1134-6
92. Lu M., Yu S., Deng J et al. Efficacy of probiotic supplementation therapy for Helicobacter pylori eradication: a meta-analysis of randomized controlled trials. PLoS One 2016; 11: e0163743
93. Pacifico L., Osborn J.F., Bonci E., et al. Probiotics for the treatment of Helicobacter pylori infection in children. World J. Gastroenterol. 2014; 20: 673-83
94. Hurduc V., Plesca D., Dragomir D., Sajin M., Vandenplas Y. A randomized, open trial evaluating the effect of Saccharomyces boulardii on the eradication rate of Helicobacter pylori infection in children. Acta Paediatr. 2009; 98: 127-31
95. Chung C.S., Chiang T.H., Lee Y.C. A systematic approach for the diagnosis and treatment of idiopathic peptic ulcers. Korean J Intern Med. 2015 Sep; 30(5): 559-70. doi: 10.3904/kjim.2015.30.5.559. Epub 2015 Aug 27. PMID: 26354049; PMCID: PMC4578017
96. Chelimsky G., Czinn S. Peptic ulcer disease in children. Pediatr Rev. 2001 Oct; 22(10): 349-55
97. Горячева О.А. Особенности течения язвенной болезни детей на современном этапе. Автореф. дис. канд. мед. наук, Москва, 2009, 25 стр.
98. Li S., Huang X.L., Sui J.Z. et al. Meta-analysis of randomized controlled trials on the efficacy of probiotics in Helicobacter pylori eradication therapy in children. Eur J Pediatr 2014; 173: 153-61.
99. Losurdo G., Cubisino R., Barone M. et al. Probiotic monotherapy and Helicobacter pylori eradication: A systematic review with pooled-data analysis. World J Gastroenterol. 2018 Jan 7; 24(1): 139-149.
100. Zheng X., Lyu L., Mei Z. Lactobacillus-containing probiotic supplementation increases Helicobacter pylori eradication rate: evidence from a meta-analysis. Rev Esp Enferm Dig 2013; 105: 445-53
101. Zhu R., Chen K., Zheng Y.Y., et al. Meta-analysis of efficacy of probiotics in Helicobacter pylori edadication therapy. World J Gastroenterol. 2014; 20: 18013-18021
102. Bin Z., Ya-Zheng X., Zhao-Hui D., et al. The efficacy of Saccharomyces boulardii CNCM I-745 in addition to standard Helicobacter pylori eradication treatment in children. Pediatr Gastroenterol Hepatol Nutr. 2015; 18: 17-22
103. Romano C., Oliva S., Martellossi S., Miele E., Arrigo S., Graziani M.G., Cardile S., Gaiani F., de′′Angelis G.L., Torroni F. Pediatric gastrointestinal bleeding: Perspectives from the Italian Society of Pediatric Gastroenterology. World J Gastroenterol. 2017 Feb 28; 23(8): 1328-1337
104. Poddar U. Diagnostic and therapeutic approach to upper gastrointestinal bleeding. Paediatr Int Child Health. 2019 Feb; 39(1): 18-22.
105. Belei O., Olariu L., Puiu M. et al. Continuous esomeprazole infusion versus bolus administration and second look endoscopy for the prevention of rebleeding in children with a peptic ulcer. Rev Esp Enferm Dig. 2018 Jun; 110(6): 352-357.
106. Wong C.W., Chung P.H., Tam P.K. Et al. Laparoscopic versus open operation for perforated peptic ulcer in pediatric patients: A 10-year experience. J Pediatr Surg. 2015 Dec; 50(12): 2038-40
107. Edwards M.J., Kollenberg S.J., Brandt M.L. et al. Surgery for peptic ulcer disease in children in the post-histamine2-blocker era. J Pediatr Surg. 2005 May; 40(5): 850-4.
108. Gisbert J.P., Pajares J.M. Review article: Helicobacter pylori infection and gastric outlet obstruction — prevalence of the infection and role of antimicrobial treatment. Aliment Pharmacol Ther. 2002 Jul; 16(7): 1203-8.
109. Elmunzer B.J., Young S.D., Inadoni J.M. et al., Systematic review of the predictors of recurrent hemorrhage after endoscopic hemostatic therapy for bleeding peptic ulcers. Am J Gastroenterol 2008; vol. 103(10): 2625-2632; quiz 2633.
110. Neidich G.A., Cole S.R. Gastrointestinal bleeding. Pediatr Rev. 2014 Jun; 35(6): 243-53; quiz 254. doi: 10.1542/pir.35-6-243. Erratum in: Pediatr Rev. 2014 Aug; 35(8): 355. Erratum in: Pediatr Rev. 2014 Jul; 35(7): 317
111. Филимонов Р.М. Курортное лечение заболеваний органов пищеварения. Москва. 2012, 406 с.
112. Пархотик И.И. Физическая реабилитация при заболеваниях органов брюшной полости. Киев. Олимпийская литература. 2003, 223 с.
113. Физическая и реабилитационная медицина в педиатрии/Хан М.А., Разумов А.Н., Корчажкина Н.Б., Погонченкова И.В. — М.: ГЭОТАР-Медиа, 2018. — 408 с.
114. Kotilea K., Kalach N., Homan M. et al. Helicobacter pylori Infection in Pediatric Patients: Update on Diagnosis and Eradication Strategies. Paediatr Drugs. 2018 Aug; 20(4): 337-351.
115. Мельникова И.Ю., Новикова В.П. Диспансеризация детей и подростков с патологией пищеварительной системы. СпецЛит, Санкт-Петербург, 2011, С. 26-38
116. Клиника, диагностика и лечение заболеваний органов пищеварения у детей. Методическое пособие. Под ред. Л.Ф. Казначеевой. — Новосибирск, 2013. — 64 с.
117. Machado R.S., Silva M.R., Viriato A. Furazolidone, tetracycline and omeprazole: a low-cost alternative for Helicobacter pylori eradication in children. J Pediatr (Rio J). 2008 Mar-Apr; 84(2): 160-5. doi: 10.2223/JPED.1772
1 Комбинация с #Фуразолидоном — наименее желательный вариант в связи с не очень хорошей переносимостью данного препарата.
Состав рабочей группы по разработке и пересмотру клинических рекомендаций
Баранов А.А. академик РАН, д.м.н., почетный Президент Союза педиатров России, советник руководителя НИИ педиатрии и охраны здоровья детей ЦКБ РАН, главный внештатный специалист педиатр Минздрава России, профессор кафедры педиатрии и детской ревматологии Клинического института детского здоровья имени Н.Ф. Филатова ФГАОУ «Первый МГМУ им. И.М. Сеченова» Минздрава России (Сеченовский Университет)
Козлов Р.С., член-корреспондент РАН, профессор, д.м.н, ректор ФГБОУ ВО СГМУ Минздрава России, Главный внештатный специалист Минздрава России по клинической микробиологии и антимикробной резистентности, Президент МАКМАХ
Намазова-Баранова Л.С., академик РАН, профессор, д.м.н., Президент Союза педиатров России; паст-президент EPA/UNEPSA; руководитель НИИ педиатрии и охраны здоровья детей ЦКБ РАН, заведующая кафедрой факультетской педиатрии педиатрического факультета ФГБОУ ВО «РНИМУ им. Н.И. Пирогова» Минздрава России, главный внештатный детский специалист по профилактической медицине Минздрава России
Подкаменев А.В. (д.м.н., Санкт-Петербургский государственный педиатрический медицинский университет, доцент/проф. кафедры хирургических болезней детского возраста им. академика Г.А. Баирова), главный внештатный специалист — детский хирург Минздрава России
Аверкина Н.А. — к.м.н., главный специалист ФГБУ «Центральный научно-исследовательский институт организации и информатизации здравоохранения» Минздрава России, врач-гастроэнтеролог, член Союза педиатров России
Бабаян М.Л. кандидат медицинских наук, отделение гастроэнтерологии и эндоскопических методов исследования ОСП «Научно-исследовательский клинический институт педиатрии им. академика Ю.Е. Вельтищева» ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России) (участие в исходной версии документа)
Бельмер С.В. профессор, доктор медицинских наук профессор кафедры госпитальной педиатрии N 2 ПФ ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России (участие в исходной версии документа)
Блат С.Ф. кандидат медицинских наук, врач педиатр, гастроэнтеролог отделения гастроэнтерологии ОСП «Научно-исследовательский клинический институт педиатрии им. академика Ю.Е. Вельтищева» ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России ((участие в исходной версии документа))
Бордин Д.С. — д.м.н., Главный внештатный специалист гастроэнтеролог Департамента здравоохранения г. Москвы, зав. отделом патологии поджелудочной железы, желчных путей и верхних отделов пищеварительного тракта МКНЦ имени А.С. Логинова, профессор кафедры пропедевтики внутренних болезней и гастроэнтерологии, ФГБОУ ВО Московский государственный медико-стоматологический университет им. А.И. Евдокимова, профессор кафедры поликлинической терапии и семейной медицины ФПДО, ФГБОУ ВО Тверской государственный медицинский университет Минздрава России
Борзакова С.Н. кандидат медицинских наук, доцент кафедры педиатрии с инфекционными болезнями у детей Факультета дополнительного профессионального образования (ФДПО) Российского национального исследовательского медицинского университета (РНИМУ) им. Н.И. Пирогова, г. Москва, (участие в исходной версии документа)
Волынец Г.В. профессор, доктор медицинских наук, член Союза педиатров России, Российского общества детских гастроэнтерологов, гепатологов, нутрициологов, Российской гастроэнтерологической ассоциации, Научного общества гастроэнтерологов России, главный научный сотрудник, руководитель отдела гастроэнтерологии ОСП «Научно-исследовательский клинический институт педиатрии им. академика Ю.Е. Вельтищева» ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России (участие в исходной версии документа)
Горелов А.В. доктор медицинских наук, профессор, член-корр. РАН, заместитель директора по науке ФБУН Центральный научно-исследовательский институт эпидемиологии Росздравнадзора, профессор кафедры детских болезней ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет), член Союза педиатров России
Гундобина О.С. кандидат медицинских наук, в.н.с, врач-гастроэнтеролог НИИ педиатрии и охраны здоровья детей ЦКБ РАН член Союза педиатров России
Гуреев А.Н., кандидат медицинских наук, доцент кафедры госпитальной педиатрии N 2 ПФ ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России, член Союза педиатров России
Дехнич Н.Н. — д.м.н., доцент кафедры факультетской терапии, научный сотрудник НИИ антимикробной химиотерапии ФГБОУ ВО «Смоленский государственный медицинский университет» Минздрава России
Зокиров Н.З., д.м.н., заведующий кафедрой Академии последипломного образования ФГБУ ФНКЦ ФМБА России, ФГБУ «ФНКЦ детей и подростков ФМБА России», член Союза педиатров России
Ильенко Л.И., д.м.н., профессор, заведующий кафедрой госпитальной педиатрии N 2 ПФ ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России, заслуженный врач РФ
Кайтукова Е.В. кандидат медицинских наук, главный врач НИИ педиатрии и охраны здоровья детей ЦКБ РАН, доцент кафедры факультетской педиатрии педиатрического факультета ФГБОУ ВО «РНИМУ им. Н.И. Пирогова» Минздрава России член Союза педиатров России
Комарова Е.В. доктор медицинских наук, заместитель руководителя НИИ педиатрии и охраны здоровья детей ЦКБ РАН, врач-гастроэнтеролог, член Союза педиатров России
Комарова О.Н. кандидат медицинских наук врач педиатр, гастроэнтеролог отделения гастроэнтерологии ОСП «Научно-исследовательский клинический институт педиатрии им. академика Ю.Е. Вельтищева» ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России (участие в исходной версии документа)
Потапов А.С. профессор, доктор медицинских наук, г.н.с. ФГАУ «НМИЦ здоровья детей» Минздрава России, профессор кафедры педиатрии и детской ревматологии Клинического института детского здоровья имени Н.Ф. Филатова ФГАОУ «Первый МГМУ им. И.М. Сеченова» Минздрава России (Сеченовский Университет), член Союза педиатров России
Разумовский А.Ю. (член-корр. РАН, д.м.н., проф., заведующий кафедрой детской хирургии ФГАОУ ВО РНИМУ имени Н.И. Пирогова Минздрава России), руководитель ассоциации детских хирургов России
Сичинава И.В. доктор медицинских наук, доцент по кафедре, профессор кафедры детских болезней ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет), член Союза педиатров России
Смирнов А.Н., проф. д.м.н. Заведующий отделением неотложной и гнойной хирургии, врач — детский хирург ГБУЗ «Детская городская клиническая больница им. Н.Ф. Филатова Департамента здравоохранения города Москвы», профессор кафедры детской хирургии педиатрического факультета ФГБОУ ВО «РНИМУ им. Н.И. Пирогова» Минздрава России, член ассоциации детских хирургов России
Строкова Т.В. — д.м.н., профессор РАН, заведующая отделением педиатрической гастроэнтерологии, гепатологии и диетотерапии Клиники ФГБУН «ФИЦ питания и биотехнологии»
Сурков А.Н. доктор медицинских наук, заведующий отделением гастроэнтерологии ФГАУ «НМИЦ здоровья детей» Минздрава России, член Союза педиатров России
Ткаченко М.А., к.м.н., педиатр, гастроэнтеролог, главный внештатный гастроэнтеролог Комитета по Здравоохранению Ленинградской области, доцент кафедры поликлинической педиатрии имени академика А.Ф. Тура Санкт-Петербургского государственного педиатрического медицинского университета.
Хавкин А.И. профессор, доктор медицинских наук, заведующий отделением гастроэнтерологии и эндоскопических методов исследования Научно-исследовательского клинического института педиатрии (НИКИ педиатрии) имени академика Ю.Е. Вельтищева, г. Москва (участие в исходной версии документа)
Холостова В.В., д.м.н., врач — детский хирург отделения неотложной и гнойной хирургии ГБУЗ «Детская городская клиническая больница им. Н.Ф. Филатова Департамента здравоохранения города Москвы», член ассоциации детских хирургов России
Яблокова Е.А. кандидат медицинских наук, доцент кафедры детских болезней ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет), член Союза педиатров России
Авторы подтверждают отсутствие финансовой поддержки/конфликта интересов, который необходимо обнародовать.
Методология разработки клинических рекомендаций
Целевая аудитория данных клинических рекомендаций:
— Врачи общей врачебной практики (семейные врачи)
— Студенты медицинских ВУЗов
— Обучающиеся в ординатуре
Методы, используемые для сбора/селекции доказательств: поиск в электронных базах данных. Описание методов, использованных для оценки качества и силы доказательств: доказательной базой для рекомендаций являются публикации, вошедшие в Кохрейновскую библиотеку, базы данных EMBASE, MEDLINE и PubMed. Глубина поиска — 10 лет.
Методы, использованные для оценки качества и силы доказательств:
— оценка значимости в соответствии с рейтинговой схемой.
Таблица 1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
| УДД | Расшифровка |
|---|---|
| 1 | Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением метаанализа |
| 2 | Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением метаанализа |
| 3 | Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования |
| 4 | Несравнительные исследования, описание клинического случая |
| 5 | Имеется лишь обоснование механизма действия или мнение экспертов |
Таблица 2. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств)
| УДД | Расшифровка |
|---|---|
| 1 | Систематический обзор РКИ с применением метаанализа |
| 2 | Отдельные РКИ и систематические обзоры исследований любого дизайна, за исключением РКИ, с применением метаанализа |
| 3 | Нерандомизированные сравнительные исследования, в т.ч. когортные исследования |
| 4 | Несравнительные исследования, описание клинического случая или серии случаев, исследования «случай-контроль» |
| 5 | Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов |
Таблица 3. Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)
| УУР | Расшифровка |
|---|---|
| A | Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными) |
| B | Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными) |
| C | Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными) |
Методы, использованные для анализа доказательств:
— Обзоры опубликованных метаанализов;
— Систематические обзоры с таблицами доказательств.
Описание методов, использованных для анализа доказательств:
При отборе публикаций как потенциальных источников доказательств использованная в каждом исследовании методология изучается для того, чтобы убедиться в ее валидности. Результат изучения влияет на уровень доказательств, присваиваемый публикации, что, в свою очередь, влияет на силу вытекающих из нее рекомендаций.
На процессе оценки, несомненно, может сказываться и субъективный фактор. Для минимизации потенциальных ошибок каждое исследование оценивалось независимо, т.е. по меньшей мере двумя независимыми членами рабочей группы. Какие-либо различия в оценках обсуждались уже всей группой в полном составе. При невозможности достижения консенсуса привлекался независимый эксперт.
Таблицы доказательств заполнялись членами рабочей группы.
Методы, использованные для формулирования рекомендаций:
Анализ стоимости не проводился и публикации по фармакоэкономике не анализировались.
Метод валидизации рекомендаций:
— Внешняя экспертная оценка;
— Внутренняя экспертная оценка.
Описание метода валидизации рекомендаций:
Настоящие рекомендации в предварительной версии были рецензированы независимыми экспертами, которых попросили прокомментировать прежде всего то, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания.
Получены комментарии со стороны врачей первичного звена в отношении доходчивости изложения рекомендаций и их оценки важности рекомендаций как рабочего инструмента повседневной практики.
Предварительная версия была также направлена рецензенту, не имеющему медицинского образования, для получения комментариев с точки зрения перспектив пациентов.
Комментарии, полученные от экспертов, тщательно систематизировались и обсуждались председателем и членами рабочей группы. Каждый пункт обсуждался, и вносимые в результате этого изменения в рекомендации регистрировались. Если же изменения не вносились, то регистрировались причины отказа от внесения изменений.
Консультация и экспертная оценка:
Проект рекомендаций был рецензирован независимыми экспертами, которых попросили прокомментировать, прежде всего, доходчивость и точность интерпретации доказательной базы, лежащей в основе рекомендаций.
Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами рабочей группы, которые пришли к заключению, что все замечания и комментарии экспертов приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
Порядок обновления клинических рекомендаций.
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию — не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утвержденным КР, но не чаще 1 раза в 6 месяцев.
Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата
Документы и ресурсы, использованные при подготовке клинических рекомендаций
1. Государственный реестр лекарственных средств: https://grls.rosminzdrav.ru
2. Приказ МЗ РФ от 20 декабря 2012 г. N 1183н «Об утверждении номенклатуры должностей медицинских работников и фармацевтических работников».
3. Приказ МЗ РФ от 23 июля 2010 г. N 541н. Единый квалификационный справочник должностей руководителей, специалистов и служащих, раздел Квалификационные характеристики должностей работников в сфере здравоохранения.
4. Федеральный закон от 25.12.2018 N 489 489-ФЗ «О внесении изменений в статью 40 Федерального закона «Об обязательном медицинском страховании в Российской Федерации» и Федеральный закон «Об основах охраны здоровья граждан в Российской Федерации» по вопросам клинических рекомендаций».
5. Приказ Минздрава России N 103н от 28.02.2019 г. «Об утверждении порядка и сроков разработки клинических рекомендаций, их пересмотра, типовой формы клинических рекомендаций и требований к их структуре, составу и научной обоснованности включаемой в клинические рекомендации информации».
6. Приказ Минздрава России от 13.10.2017 N 804н «Об утверждении номенклатуры медицинских услуг».
7. Приказ Министерства здравоохранения РФ от 14 января 2019 г. N 4н «Об утверждении порядка назначения лекарственных препаратов, форм рецептурных бланков на лекарственные препараты, порядка оформления указанных бланков, их учета и хранения».
8. Приказ Министерства здравоохранения и социального развития РФ от 16 апреля 2012 г. N 366н «Об утверждении Порядка оказания педиатрической помощи».
9. Приказ Минздрава России 203н от 10 мая 2017 г. «Об утверждении критериев оценки качества медицинской помощи».
Примеры диагнозов
— Язвенная болезнь двенадцатиперстной кишки с локализацией в луковице, H. pylori. — позитивная, впервые выявленная, с повышенной кислотообразующей функцией, фаза обострения.
— Язвенная болезнь желудка, H. pylori — негативная, нормальная кислотообразующая функция желудка, часто рецидивирующее течение, фаза обострения, состоявшееся желудочное кровотечение.
При формулировке диагноза указывается локализация язвы (желудок, двенадцатиперстная кишка или двойное поражение), фаза заболевания (обострение, неполная клиническая ремиссия и клиническая ремиссия), эндоскопическая характеристика дефектов и стадия эволюции язвенного процесса, наличие H. pylori, осложнения.
Основной морфологический субстрат язвенной болезни в фазе обострения — язвенный дефект слизистой оболочки и сопряженный с ним активный гастродуоденит, а в фазе ремиссии — постязвенные рубцовые изменения и гастродуоденит.
Отражение в клиническом диагнозе локализации и исхода заживления язвенных дефектов весьма важно как для определения тактики лечения больных, так и для прогнозирования дальнейшего течения заболевания, планирования адекватной программы диспансерных мероприятий.
Эндоскопическая картина стадий язвенного поражения
I стадия — острая язва. На фоне выраженных воспалительных изменений СОЖ и ДПК — дефект (дефекты) округлой формы, окруженные воспалительным валом; выраженный отек. Дно язвы с наслоением фибрина.
II стадия — начало эпителизации. Уменьшается гиперемия, сглаживается воспалительный вал, края дефекта становятся неровными, дно язвы начинает очищаться от фибрина, намечается конвергенция складок к язве.
— Фаза неполной ремиссии:
III стадия — заживление язвы. На месте репарации — остатки грануляций, рубцы красного цвета разнообразной формы, с деформацией или без нее.
Полная эпителизация язвенного дефекта (или «спокойный» рубец), отсутствуют признаки сопутствующего гастродуоденита.
Схемы лечения инфекции H. pylori и рекомендуемые дозы препаратов для антихеликобактерной терапии (по 11, 33)
Таблица 1. Возможные схемы антихеликобактерной терапии
| Кларитромицин (таблетки с 12 лет** и #гранулы для приготовления суспензии для приема внутрь**) | #Метронидазол** | Рекомендуемая схема лечения (14 дней) |
|---|---|---|
| Пациенты без аллергии к пенициллинам | ||
| Чувствительность | Чувствительность | ИПН + Амоксициллин** + Кларитромицин (таблетки с 12 лет** и #гранулы для приготовления суспензии для приема внутрь**) |
| Резистентность | Чувствительность | ИПН + Амоксициллин** + #Метронидазол** |
| Чувствительность | Резистентность | ИПН + Амоксициллин** + Кларитромицин (таблетки с 12 лет** и #гранулы для приготовления суспензии для приема внутрь**) |
| Двойная резистентность или нет информации о чувствительности/резистентности | лет: #Висмута трикалия дицитрат**+ ИПН + #Метронидазол** + #Тетрациклин | |
| Пациенты с аллергией к пенициллинам | ||
| Чувствительность | Чувствительность | ИПН + #Метронидазол** + Кларитромицин (таблетки с 12 лет** и #гранулы для приготовления суспензии для приема внутрь**) |
| Резистентность | Чувствительность | лет: #Висмута трикалия дицитрат** + ИПН + #Метронидазол** + #Тетрациклин |
| Чувствительность | Резистентность | лет: #Висмута трикалия дицитрат** + ИПН + Кларитромицин (таблетки с 12 лет** и #гранулы для приготовления суспензии для приема внутрь**) + #Тетрациклин #Висмута трикалия дицитрат** + ИПН + #Метронидазол** 2 + #Тетрациклин |
| Двойная резистентность или нет информации о чувствительности/резистентности | лет: #Висмута трикалия дицитрат** + ИПН + #Метронидазол** + #Тетрациклин | |
1 Комбинация с #Фуразолидоном — наименее желательный вариант в связи с не очень хорошей переносимостью данного препарата.
2 Высокая суточная доза, разделенная на 3 приема.
Таблица 2. Дозы препаратов для лечения инфекции H. pylori у детей [33, 117]
| Препарат | Масса тела (кг) | Утренняя доза (мг) | Вечерняя доза (мг) |
|---|---|---|---|
| #Эзомепразол** или #омепразол** 1 , 2 | 15-24 | 20 | 20 |
| 25-34 | 30 | 30 | |
| >35 | 40 | 40 | |
| Амоксициллин** (стандартная доза) | 15-24 | 500 | 500 |
| 25-34 | 750 | 750 | |
| >35 | 1000 | 1000 | |
| Амоксициллин** (высокая доза) | 15-24 | 750 | 750 |
| 25-34 | 1000 | 1000 | |
| >35 | 1500 | 1500 | |
| Кларитромицин** (таблетки с 12 лет** и #гранулы для приготовления суспензии для приема внутрь**) | 15-24 | 250 | 250 |
| 25-34 | 500 (375 3 ) | 250 (375) | |
| >35 | 500 | 500 | |
| #Метронидазол** | 15-24 | 250 | 250 |
| 25-34 | 500 | 250 | |
| >35 | 500 | 500 | |
| #Тетрациклин | 25-50 мг/кг/сут, разделив на 4 приема (макс. доза 2000 мг) | ||
| #Фуразолидон | 30 кг — по 200 мг 2 раза в день или 6-10 мг/кг/сут, разделив на 4 приема | ||
| #Висмута трикалия дицитрат** | 8 мг/кг/сут, разделив на 4 приема | ||
1 Дозы других ИПН должны быть эквиваленты указанным дозам #эзомепразола** и #омепразола**.
2 Эзомепразол** в форме пеллет, покрытых кишечнорастворимой оболочкой, и гранул для приготовления суспензии для приема внутрь — при язвенной болезни двенадцатиперстной кишки — разрешен к применению детям с 4 лет согласно инструкции.
3 Если доступна суспензия, то суточную дозу нужно разделить на две равные дозы по 375 мг утром и вечером.
Таблица 3. Дозы ингибиторов протонного насоса для лечения инфекции H. pylori, возможные для использования у детей [59]
| Препарат | Доза мг/кг/сут (разделенная на 2 приема) | Максимальная суточная доза (мг/сут) |
|---|---|---|
| #Эзомепразол** 1 | лет Масса тела | 40 |
| #Рабепразол** | 0,5 мг/кг/сут (разделенная на 2 приема) | 20 |
| #Омепразол** | 1,0 мг/кг/сут (разделенная на 2 приема) | 40 |
| #Лансопразол | 1,5 мг/кг/сут (разделенная на 2 приема) | 60 |
1 Эзомепразол** в форме пеллет, покрытых кишечнорастворимой оболочкой, и гранул для приготовления суспензии для приема внутрь — при язвенной болезни двенадцатиперстной кишки — разрешен к применению детям с 4 лет согласно инструкции.
Расшифровка примечаний
** — лекарственный препарат, входящий в Перечень жизненно необходимых и важнейших лекарственных препаратов для медицинского применения на 2021 год (Распоряжение Правительства РФ от 12.10.2019 N 2406-р, от 23 ноября 2020 г. N 3073-р)
# — применение off-label — вне зарегистрированных в инструкции лекарственного средства показаний осуществляется по решению врачебной комиссии, с разрешения Локального этического комитета медицинской организации (при наличии), с условием подписанного информированного согласия родителей (законного представителя) и пациента в возрасте старше 15 лет
Алгоритмы действий врача
Информация для пациента
Язвенная болезнь желудка и 12-перстной кишки — хроническое рецидивирующее заболевание, опасное возможностью возникновения осложнений.
1. Возникновение и прогрессирование болезни, ее рецидивы обусловлены комплексом факторов, некоторые из которых (наследственность и др.) не зависят от пациента, другие же полностью или частично управляются пациентом и его семьей (образ жизни, рабочие стереотипы, семейные традиции питания и др.).
2. Язвы желудка часто являются побочным эффектом приема спазмолитиков в комбинации с анальгетиками (обезболивающих) и нестероидных противовоспалительных препаратов.
3. Алкоголь, пища, курение и эмоциональный стресс могут влиять на развитие язвенной болезни или на процесс ее излечения.
4. Боли в верхней части живота является наиболее распространенным симптомом язвы желудка, но многие язвы не вызывают никаких симптомов.
5. Язвы могут быть причиной кровотечения в желудочно-кишечном тракте, что проявляется черным цветом кала. Развитие язвенной болезни желудка может стать причиной непроходимости между желудком и тонкой кишкой, следствием которой являются частые сильные рвоты.
6. Язва желудка и ДПК почти всегда может быть успешно вылечена, как правило, без хирургического вмешательства. Во многих случаях язвенная болезнь может быть предотвращена.
7. Лекарства, которыми лечат язву желудка и двенадцатиперстной кишки, включают средства, нейтрализующие или уменьшающие секрецию кислоты желудочного сока и антибиотики, (при наличии хеликобактерной инфекции) а также препараты, улучшающие сопротивляемость желудка и двенадцатиперстной кишки.
Советы пациенту и его семье:
— В течение всего периода обострения — режим физического и психологического покоя.
— Исключается прием ряда лекарственных препаратов (при отсутствии абсолютных показаний, необходимо посоветоваться с врачом).
— Питание дробное, 4-5 раз в день, с исключением жареного, жирного, соленого, острого. В течение первых 4-5 дней пища, механически и химически щадящая, затем диета с достаточным содержанием белка. Предпочтение отдается вареным блюдам.
— Диета должна соблюдаться и в период ремиссии.
— Отказ от вредных привычек
Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Обзор документа
Минздрав представил клинические рекомендации по язвенной болезни желудка и/или двенадцатиперстной кишки у детей.
Рекомендации действуют до 2023 г.
Для просмотра актуального текста документа и получения полной информации о вступлении в силу, изменениях и порядке применения документа, воспользуйтесь поиском в Интернет-версии системы ГАРАНТ:
Источник https://diseases.medelement.com/disease/%D1%8F%D0%B7%D0%B2%D0%B5%D0%BD%D0%BD%D0%B0%D1%8F-%D0%B1%D0%BE%D0%BB%D0%B5%D0%B7%D0%BD%D1%8C-%D0%BA%D1%80-%D1%80%D1%84-2020/17160
Источник https://probolezny.ru/yazvennaya-bolezn-dvenadcatiperstnoy-kishki/
Источник https://www.garant.ru/products/ipo/prime/doc/402776269/