Инфаркт миокарда описание диагностика лечение по смр
МКБ 10: I21.0/I21.1/121.2/121.3/121.4/121.9/122.0/122.1/122.8/122.9/124.0/124.8
Год утверждения (частота пересмотра): 2016 (пересмотр каждые 3 года)
ID: КР157
- Общество специалистов по неотложной кардиологии
Ключевые слова
- острый коронарный синдром
- инфаркт миокарда
- инфаркт миокарда с подъемом сегмента ST
- реперфузионное лечение
- чрескожное коронарное вмешательство
- первичное чрескожное коронарное вмешательство
- спасающее чрескожное коронарное вмешательство
- тромболитическая терапия
- фармако-инвазивный подход
Список сокращений
АБ – атеросклеротическая бляшка
АВС – активированное время свертывания крови
АГ – артериальная гипертония
АД – артериальное давление
АСК – ацетилсалициловая кислота
АЧТВ – активированное частичное тромбопластиновое время
Блокаторы ГП IIb/IIIa рецепторов тромбоцитов – блокаторы гликопротеиновых рецепторов IIb/IIIa тромбоцитов
ВГН – верхняя граница нормы
ВСС – внезапная сердечная смерть
ЖТ – желудочковая тахикардия
Ингибиторы АПФ – ингибиторы ангиотензин-превращающего фермента
ИБС – ишемическая (коронарная)болезнь сердца
ИВЛ – искусственная вентиляция легких
ИМ – инфаркт миокарда
ИМпST – инфаркт миокарда со стойким подъемом сегмента ST ЭКГ
ИМТ – индекс массы тела
КА – коронарные артерии
КАГ – коронарная ангиография
КТ – компьютерная томография
КШ – коронарное шунтирование
ЛА – легочная артерия
ЛВП – липопротеины высокой плотности
ЛГ – легочная гипертония
ЛЖ – левый желудочек
ЛКА – левая коронарная артерия
ЛНП – липопротеины низкой плотности
ЛНПГ – левая ножка пучка Гиса
МВ КФК – МВ фракция креатинфосфокиназы
МЖП – межжелудочковая перегородка
МНО – международное нормализованное отношение
МРТ – магнитно-резонансная томография
МС – метаболический синдром
неQ-ИМ – ИМ без зубца Qна ЭКГ
НМГ – низкомолекулярный гепарин
НФГ – нефракционированный гепарин
ОКС – острый коронарный синдром
ОКСбпST – ОКС без подъема сегмента ST ЭКГ
ОКСпST – ОКС с подъемом сегмента ST ЭКГ
ПЖ – правый желудочек
ПНПГ – правая ножка пучка Гиса
ПЭТ – позитронная эмиссионная томография
РААС – ренин-ангиотензин-альдостероновая система
РФ – Российская Федерация
САД – систолическое АД
СД – сахарный диабет
СМП – скорая медицинская помощь
СН – сердечная недостаточность
ССЗ – сердечно-сосудистые заболевания
ТЛТ – тромболитическая (фибринолитическая) терапия
ТП – трепетание предсердий
ТФН – толерантность к физической нагрузке
ТЭЛА – ТЭ легочной артерии
УЗИ – ультразвуковое исследование
ФВ – фракция выброса ЛЖ
ФЖ – фибрилляция желудочков
ФК – функциональный класс
ФН – физическая нагрузка
ФП – фибрилляция предсердий
ФР – факторы риска
ХС ЛНП – холестерин ЛНП
ХСН – хроническая СН
ЧКВ – чрескожные коронарные вмешательства: лечебные вмешательства на коронарных артериях, осуществляемые с помощью вводимого чрескожно катетера (обычно выполняется транслюминальная баллонная ангиоплатикачаще с имплантацией стентов – стентирование).
ЭИТ – электроимпульсная терапия
ЭКГ – электрокардиография (-мма, -ческий, -ая, -ое)
ЭС – электрическая стимуляция сердца
BiPAP–bi-level positive pressuresupport (двухуровневая поддержка с положительным давлением)
HbA1c– гликозилированный гемоглобин
MDRD– Модификация диеты при заболеваниях почек
Q-ИМ – ИМ с зубцом Q на ЭКГ
Термины и определения
Голометаллический стент – стент, представляющий собой стальной каркас из биологически инертного материала.
Инфаркт миокарда без стойких подъемов сегментаST – инфаркт миокарда, при котором в ранние сроки заболевания отсутствуют стойкие (длительностью более 20 минут) подъемы сегмента ST на ЭКГ.
Инфаркт миокарда с зубцомQ – инфаркт миокарда с появлением патологических зубцов Q как минимум в двух смежных отведениях ЭКГ.
Инфаркт миокарда без зубцаQ – инфаркт миокарда, когда патологические зубцы Q на ЭКГ не сформировались.
Операция коронарного шунтирования – наложение обходного анастомоза, позволяющего улучшить кровоток дистальнее гемодинамически значимого стеноза в коронарной артерии. В зависимости от методики включает аортокоронарное, маммаро-коронарное и другие виды шунтирования.
Острый коронарный синдром – любая группа клинических признаков или симптомов, позволяющих заподозрить острый инфаркт миокарда или нестабильную стенокардию.
Острый коронарный синдром со стойкими подъемами сегментаST – недавно возникшие клинические признаки или симптомы ишемии миокарда в сочетании с наличием стойких (длительностью более 20 минут) подъемов сегмента ST как минимум в двух смежных отведениях ЭКГ. Включает инфаркт миокарда со стойкими подъемами сегмента ST и нестабильную стенокардию.
Острый инфаркт миокарда – признаки некроза кардиомиоцитов в клинических условиях, предполагающих наличие острой ишемии миокарда.
Острый некроз кардиомиоцитов – повышение и/или снижение содержания в крови биомаркеров некроза миокарда (предпочтительно сердечного тропонина), которое как минимум однократно превышает 99-й перцентиль значений у здоровых лиц.
Первичное чрескожное коронарное вмешательство – способ реперфузионного лечения острого коронарного синдрома со стойкими подъемами сегмента ST на ЭКГ, когда первым мероприятием по восстановлению проходимости коронарной артерии является чрескожное коронарное вмешательство.
“Подготовленное” чрескожное коронарное вмешательство – способ реперфузионного лечения острого коронарного синдрома со стойкими подъемами сегмента ST на ЭКГ, при котором перед первичным чрескожным коронарным вмешательством вводится полная или половинная доза фибринолитика, иногда в сочетании с блокатором гликопротеинов IIb/IIIa. В настоящее время не рекомендуется.
“Спасительное”(“ спасающее”) чрескожное коронарное вмешательство – срочное чрескожное коронарное вмешательство после неуспешной тромболитической терапии.
Стент, выделяющий лекарство — стент, с поверхности которого выделается антипролиферативное вещество, препятствующее образованию неоинтимы и за счет этого способствующее снижению выраженности процессов рестенозирования.
Тромболитическая терапия – способ реперфузионного лечения острого коронарного синдрома со стойкими подъемами сегмента ST на ЭКГ, когда осуществляется медикаментозное восстановление проходимости окклюзированной коронарной с помощью парентерального введения фибринолитического препарата, обычно в сочетании с антиагрегантами и антикоагулянтом.
Фармако-инвазивный подход – способ реперфузионного лечения острого коронарного синдрома со стойкими подъемами сегмента ST на ЭКГ, когда проводится тромболитическая терапия и в ближайшие сутки всем больным выполняется диагностическая коронарная ангиография с намерением осуществить стентирование инфаркт-связанного стеноза.
Чрескожное коронарное вмешательство – восстановление кровотока в стенозированном участке коронарной артерии с использованием чрескожного введения необходимых для этого устройств. Включает чрескожную баллонную ангиопластику, коронарное стентирование и другие, менее распространенные методики. Как правило, если не указано иное, под чрескожным коронарным вмешательством подразумевают коронарное стентирование.
1. Краткая информация
1.1. Определение
Острый коронарный синдром (ОКС) — термин, обозначающий период обострения ишемической болезни сердца (ИБС), когда любая группа клинических признаков или симптомов позволяет подозревать острый инфаркт миокарда (ИМ) или нестабильную стенокардию. Включает в себя понятия «острый ИМ», «ИМ с подъемом сегмента ST ЭКГ (ИМпST)», «ИМ без подъема сегмента ST ЭКГ (ИМбпST)», ИМ, диагностированный по изменениям ферментов, по другим биомаркерам, по поздним ЭКГ-признакам, и нестабильную стенокардию.
Термин “ОКС” был введен в клиническую практику, когда выяснилось, что вопрос о применении некоторых активных методов лечения, в частности ТЛТ, должен решаться быстро, нередко до окончательного диагноза ИМ. Установлено, что, во многом, характер и срочность вмешательства для восстановления коронарной перфузии определяется положением сегмента ST относительно изоэлектрической линии на ЭКГ – при смещении сегмента ST вверх (подъеме ST) – методом выбора восстановления коронарного кровотока является коронарная ангиопластика, но при невозможности ее проведения в соответствующие сроки эффективна и, соответственно, показана, ТЛТ. Восстановление коронарного кровотока при ОКСпST должно проводиться безотлагательно.
Подъем сегмента ST – как правило, следствие трансмуральной ишемии миокарда и возникает при наличии полной окклюзии одной из магистральных коронарных артерий КА. В этих случаях обычно развивается ИМ, который обозначается как ИМпST.
1.2. Этиология и патогенез
ОКСпST ЭКГ – как правило, следствие окклюзирующего тромбоза КА. Тромб возникает чаще всего на месте разрыва так называемой ранимой (нестабильной) атеросклеротической бляшки (А)Б с большим липидным ядром, богатой воспалительными элементами и истонченной покрышкой, однако возможно образование окклюзирующего тромба и на дефекте эндотелия (эрозии) КА над АБ. В большинстве случаев окклюзия развивается в месте гемодинамически незначимого стеноза КА.
В КА больных с ОКС обычно находят несколько ранимых АБ, в т.ч. имеющих надрывы. Из-за высокого риска возникновения повторных окклюзий КА при лечении этих больных локальные воздействия в области АБ, обусловившей развитие клинической картины ОКС, должны комбинироваться с общими лечебными мероприятиями, направленными на снижение вероятности тромбоза.
Тромб может быть источником эмболий в дистальное сосудистое русло сердца. Эмболизация микрососудов миокарда сама по себе может приводить к образованию мелких очагов некроза. Кроме того, мелкие эмболы препятствуют восстановлению кровоснабжения миокарда (реперфузии) после устранения окклюзии крупной КА.
Следствием ИМ является процесс ремоделирования сердца. Образование очага некроза в миокарде сопровождается изменение размера, формы и толщины стенки ЛЖ, а сохранившийся миокард испытывает повышенную нагрузку и подвергается гипертрофии. Насосная функция изменившего форму ЛЖ ухудшается, и это способствует развитию СН. Наиболее выраженная форма ремоделирования ЛЖ при обширных ИМ связана с образованием аневризмы стенки ЛЖ.
В последнее время предложено различать и другие типы ИМ, отличающиеся механизмами развития (Приложения Г1, Г2 и Г3).
1.3. Эпидемиология
Коды МКБ 10 не позволяют с уверенность выделять больных с ОКСпST и ИМпST. В частности, при трансмуральном ИМ не всегда (хотя и часто) в ранние сроки заболевания отмечаются стойкий подъем сегмента ST ЭКГ. Механизм возникновения и размеры повторного ИМ в МКБ 10 не учитываются. В разных странах частота ИМпST варьируется и по данным регистров с наиболее полным популяционным охватом в странах Европы и США составляют в настоящее время около 70 на 100000 населения в год. Хотя на фоне широкого внедрения современных подходов к ведению больных (прежде всего своевременного реперфузионного лечения) смертность при ИМпST снижается, по данным национальных регистров в Европе госпитальная летальность варьируется от 6 до 14%, смертность за 6 месяцев может превышать 12% и за 5 лет достигать 20%. У больных с тяжелыми проявлениями заболевания и выраженной сопутствующей патологией прогноз еще более неблагоприятен.
1.4. Кодирование по МКБ-10
Острый инфаркт миокарда (I21)
I21.0 – Острый трансмуральный инфаркт миокарда передней стенки
I21.1 – Острый трансмуральный инфаркт миокарда нижней стенки
I21.2 – Острый трансмуральный инфаркт миокарда других уточненных локализаций
I21.3 – Острый трансмуральный инфаркт миокарда неуточненной локализации
I21.4 – Острый субэндокардиальный инфаркт миокарда
I21.9 – Острый инфаркт миокарда неуточненный
Повторный инфаркт миокарда (I22)
I22.0 – Повторный инфаркт миокарда передней стенки
I22.1 – Повторный инфаркт миокарда нижней стенки
I22.8 – Повторный инфаркт миокарда другой уточненной локализации
I22.9 – Повторный инфаркт миокарда неуточненной локализации
Другие формы острой ишемической болезни сердца (I24)
I24.0 – Коронарный тромбоз, не приводящий к инфаркту миокарда
I24.8 – Другие формы острой ишемической болезни сердца
1.5. Классификация
ОКСпSTдиагностируют у больных с ангинозным приступом или другими неприятными ощущениями (дискомфортом) в грудной клетке и стойким (сохраняющимся не менее 20 мин) подъемом сегмента ST или «новой»( впервые возникшей) блокадой ЛНПГ на ЭКГ. Как правило, в тех случаях, когда у больных заболевание начинается как ОКСпST, позже наблюдаются признаки некроза миокарда. Появление признаков некроза означает, что у больного развился ИМ. Термин “ИМ” отражает гибель (некроз) клеток сердечной мышцы (кардиомиоцитов) в результате ишемии (приложения Г1, Г2) [1].
Термин “ОКС” используется, когда диагностическая информация еще недостаточна для окончательного суждения о наличии или отсутствии очагов некроза в миокарде. Соответственно, ОКС – это рабочий диагноз в первые часы и сутки заболевания, тогда как понятия “ИМ” и “нестабильная стенокардия”( ОКС, не закончившийся появлением признаков некроза миокарда) сохраняются для использования при формулировании окончательного диагноза.
Если признаки некроза миокарда обнаруживаются у больного с ОКС, у которого на начальных ЭКГ отмечены стойкие подъемы сегмента ST, это состояние обозначают как ИМпST. В дальнейшем зависимости от ЭКГ картины, пиковой активности ферментов, или/и данных методов, регистрирующих движения стенки сердца, ИМ может оказаться крупноочаговым, мелкоочаговым, с зубцами Q, без зубцов Q и т.д. При ИМ с глубокими зубцами Q, особенно при формировании зубцов QS, некроз обычно носит трансмуральный характер, захватывая на определенном участке всю толщу стенки ЛЖ. При ИМ без образования патологического зубца Q чаще находят поражение субэндокардиальных слоев стенки сердца. Обычно некроз при Q-ИМ имеет больший размер, чем при неQ-ИМ. В связи с этим неQ-ИМ иногда трактуют как «мелкоочаговый», а Q-ИМ как «крупноочаговый». Однако при патоморфологическом исследовании размер некроза при неQ-ИМ может оказаться сравнимым по размерам с Q-ИМ. Четких морфологических различий по размерам между «мелкоочаговым» и «крупноочаговым» ИМ не установлено.
ОКСпST ЭКГ чаще заканчивается появлением зубцов Q, чем ОКСбпST, особенно при естественном течении заболевания.
Таким образом, ОКС по своим ЭКГ характеристикам и морфологическим исходам весьма разнообразен. Изменения ЭКГ на начальном этапе не предопределяют окончательный диагноз. Однако они позволяют ответить на принципиально важный вопрос: показано ли в данном случае неотложное начало реперфузионной терапии?
Периодика ИМ. На основании клинических, морфологических и других признаков согласительный документ, принятый рядом международных кардиологических сообществ в 2007г., предлагает разделить течение ИМ на несколько периодов:
- развивающийся ИМ – от 0 до 6 часов;
- ОИМ – от 6 часов до 7 суток;
- заживающий (рубцующийся) ИМ – от 7 до 28 суток;
- заживший ИМ – начиная с 29 суток.
Относительность такого деления очевидна, однако оно может оказаться полезным для статистических и исследовательских целей.
Под повторным понимают ИМ, развившийся после 28 суток от предыдущего. Если же этот срок меньше, то речь идет о рецидивирующем ИМ.
2. Диагностика
- Рекомендуется в диагностике ОКСпST опираться на данные анамнеза, наличие факторов риска (ФР) ИБС, особенности острых проявлений заболевания, характер изменений на ЭКГ и в некоторых случаях данные о локальной сократительной функции желудочков сердца [2-4].
Уровень убедительности рекомендацийI (Уровень достоверности доказательств С).
Комментарии: Другие методы обследования требуются для подтверждения ишемии миокарда при недостаточной информативности ЭКГ, исключения заболеваний со схожей клинической симптоматикой, выявления ИМ и оценки (стратификации) риска неблагоприятного течения заболевания.
2.1. Жалобы и анамнез
- Рекомендуется в диагностике опираться на характерные клинические проявления, прежде всего – особенности болевого синдрома ( типично чувство сжатия или давления за грудиной; по характеру боль сходна с таковой при приступе стенокардии, но отличается по силе и продолжительности; характер болевых ощущений разнообразен – сжимающий, давящий, жгучий, иногда описываются как дискомфорт; в большинстве случаев она полностью не купируется приемом нитроглицерина, а иногда и повторными инъекциями наркотических анальгетиков; интенсивность болевого синдрома может быть различной – от незначительной до невыносимой; боль может носить волнообразный характер и продолжается от 20 мин до нескольких часов; может наблюдаться иррадиация боли в левую руку, левое плечо, горло, нижнюю челюсть, эпигастрий и т.д.) [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств С).
Комментарии: К атипичным формам ИМпSTотносят астматический вариант, абдоминальный вариант, аритмический вариант, цереброваскулярный вариант, а также малосимптомную (безболевую) форму.
2.2. Физикальное обследование.
- Рекомендуется физикальное обследование для выявления симптомов, позволяющих оценить наличие и тяжесть других заболеваний, провоцирующих или осложняющих течение ИМ и способных повлиять на выбор подходов к лечению, оценить наличие осложнений ИМ и помочь в дифференциальной диагностике [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств С).
2.3. Лабораторные методы исследования
- Рекомендуется определение уровня биохимических маркеров повреждения кардиомиоцитов в крови, предпочтительно сердечного тропонина Т или I [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств А).
Комментарии: Помимо сердечного тропонина клиническое значение сохраняет только определение массы МВ-КФК (ее уровень в крови после ИМ снижается быстрее, чем сердечный тропонин, что может позволить точнее судить о сроках повреждения миокарда и ранних рецидивах ИМ). Преходящее повышение уровня сердечного тропонина в крови свидетельствует о некрозе кардиомиоцитов вне зависимости от причины, которая может быть связана как с первичным ограничением коронарного кровотока, так и другими, в том числе внесердечными факторами (приложения Г1, Г2, Г3). Повышение уровня сердечного тропонина выше 99-го перцентиля здоровых лиц в условиях, указывающих на наличие ишемии миокарда, свидетельствует об остром ИМ.
- Рекомендуется забор крови в острой фазе заболевания на определение биохимических маркеров повреждения кардиомиоцитов. При этом не следует дожидаться результатов до начала реперфузионного лечения [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств С).
Комментарии: При ОКСпSTизменение уровня биомаркеров в крови используется выявления острого ИМ, но не влияет на принятие решения о проведении реперфузионной терапии.
2.4. Инструментальные методы исследования
- Рекомендуется регистрация ЭКГ как минимум в 12 отведениях в покое у всех больных с подозрением на ОКС [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств А).
Комментарий: Для ИМпST характерно возникновение подъема ST как минимум в двух последовательных отведениях, который оценивается на уровне точки J составляет³0,2 мВ у мужчин или³0,15 мВ у женщин в отведениях V2-V3 и/или³0,1 мВ в других отведениях (в случаях, когда нет блокады ЛНПГ и гипертрофии левого желудочка). Важный диагностический прием – сравнение с ЭКГ, зарегистрированной до наступления настоящего коронарного приступа. Поэтому следует приложить максимум усилий, чтобы предыдущая ЭКГ оказалась в Вашем распоряжении. Важно помнить, что подъемы сегмента ST могут наблюдаться, не только при ИМ, но и при синдроме ранней реполяризации, полной блокаде ЛНПГ, обширных рубцовых изменениях в миокарде (хронической аневризме ЛЖ), перикардите, синдроме Бругада и пр. (Приложение Г5). Поэтому диагноз ИМ должен основываться на комплексе признаков и всегда соотноситься с клинической картиной заболевания.
- Рекомендуется зарегистрировать ЭКГ в течение 10 мин на месте первого контакта с медицинским работником (как правило, догоспитально) и безотлагательно интерпретировать ее квалифицированным врачом [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств В).
- Рекомендуется у больных с подозрением на ИМ нижне-базальной локализации использование дополнительных отведений ЭКГ (V7-V9), при подозрении на ИМ правого желудочка (ПЖ) – V3R и V4R [2-4].
Уровень убедительности рекомендаций IIa (Уровень достоверности доказательств С).
Комментарий: Для отведений V7-V9 диагностичными являются подъемы ST³0,05 мВ (³0,1 мВ у мужчин моложе 40 лет). В сложных случаях возможно регистрация ЭКГ и в других отведениях (на 2 ребра выше и т.д.). Депрессия сегмента ST >0,1mV в 8 и более отведениях при подъеме сегмента ST в отведении aVR и/илиV1 предполагает поражение ствола левой КА или многососудистое поражение бассейна левой КА.
- Рекомендуется у больных с подозрением на ИМ нижне-базальной локализации рекомендовано использование дополнительных отведений ЭКГ V7-V9, при подозрении на ИМ правого желудочка – V3R и V4R [2-4].
Уровень убедительности рекомендаций IIa (Уровень достоверности доказательств С).
- Рекомендуется у больных с подозрением на ИМпST скорейшее начало мониторирования ЭКГ [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств В).
- Рекомендуется в неясных случаях для уточнения диагноза эхокардиография (ЭхоКГ), однако ее выполнение не должно задерживать транспортировку больного на коронарную ангиографию (КАГ) [2-4].
Уровень убедительности рекомендаций IIb (Уровень достоверности доказательств С).
Комментарий: Выявление локальных нарушений сократимости ЛЖ (а нередко и ПЖ) на фоне соответствующей клинической картины – важный признак очагового поражения миокарда. Вместе с тем локальные нарушения сократительной функции желудочков сердца могут наблюдаться и при тяжелой ишемии, не приведшей к развитию некроза, например, при нестабильной стенокардии, а также в случае рубцового поражения после ранее перенесенного ИМ. ЭхоКГ необходима для оценки функции и геометрии ЛЖ, а также для распознавания таких осложнений, как тромбоз полости, разрывы сердца, нарушение функции клапанов, в частности, митральная регургитация, ИМ ПЖ, перикардит. Существенна роль УЗИ в диагностике расслоения аорты и ТЭЛА. Оценка динамики локальной и глобальной функции сердца помогает уточнить эффективность лечения и прогноз.
Сцинтиграфия миокарда с 99mTc-пирофосфатом – дополнительный метод диагностики, который показан для верификации некроза миокарда преимущественно в тех случаях, когда имеются существенные затруднения в интерпретации изменений ЭКГ в связи с наличием блокады ножек пучка Гиса, пароксизмальных нарушений сердечного ритма или признаков перенесенного в прошлом ИМ.
Компьютерная томография не относится к числу стандартных методов обследования в остром периоде ИМ. Однако, она может оказаться полезной для дифференциальной диагностики, если другие методы недостаточно информативны (расслоение аорты, ТЭЛА, пневмоторакс, плеврит и пр.).
Магнитно-резонансная томография – лучший метод для уточнения локализации и объёма поражения даже при относительно небольших размерах очага (очагов) некроза. Он позволяет дифференцировать ишемическую или воспалительную (миокардиты) природу поражения, является эталонным методом трехмерной оценки морфологии и функции камер сердца, а также оценки клапанного аппарата. Дополнительное преимущество метода – отсутствие лучевой нагрузки. Однако технические сложности выполнения ограничивают его применение в самом остром периоде заболевания.
2.5. Стратификация риска
- Рекомендуется для стратификации риска неблагоприятного исхода осуществлять совокупную оценку анамнеза, клинических данных, ЭКГ, ЭхоКГ, результатов определения сердечного тропонина в крови, функции почек (расчетных значений клиренса креатинина или скорости клубочковой фильтрации) [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств А).
Комментарии: Наиболее проста для применения шкала оценки риска TIMI, однако более точно оценить прогноз заболевания позволяет шкала GRACE(Приложение Г6). Один из ее вариантов дает возможность осуществить стратификацию риска при госпитализации, другой — при выписке из стационара. Новая шкалаGRACE 2,0 характеризует прогноз заболевания на протяжении ближайших 3 лет без предварительного подсчета суммы баллов. Еще одной особенностью этой шкалы является возможность применения у больных с еще неизвестным уровнем креатинина в крови и классом поKillip. Для использования шкалыGRACE 2,0 необходим калькулятор, расположенный в сети Интернет по адресу http://www.gracescore.org/WebSite/default.aspx?ReturnUrl=%2f.
3. Лечение
3.1. Медикаментозное лечение
3.1.1. Обезболивание и устранение беспокойства
- Рекомендуется для обезболивания использовать внутривенное введение наркотического анальгетика, предпочтительно морфина ** [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств С).
Комментарии: Если ангинозный приступ не ослабевает через несколько минут после прекращения действия провоцирующего фактора (физическая нагрузка) или если он развился в покое, больному следует принять нитроглицерин ** в дозе 0,4-0,5 мг в виде таблеток под язык или аэрозоля (спрея). Если симптомы не исчезают через 5 мин, а препарат удовлетворительно переносится, рекомендуется использовать его повторно. Если боль в грудной клетке или дискомфорт, расцениваемый как ее эквивалент, сохраняются в течение 5 мин после повторного приема нитроглицерина, необходимо немедленно вызвать СМП и снова принять нитроглицерин. Исключение может быть сделано только для случаев, когда для купирования ангинозного приступа у данного больного обычно требуется прием нескольких доз нитроглицерина и при условии, что выраженность и продолжительность болевого синдрома не изменились.
Помимо обезболивания морфин способствует уменьшению страха, возбуждения, снижает симпатическую активность, увеличивает тонус блуждающего нерва, уменьшает работу дыхания, вызывает расширение периферических артерий и вен (последнее особенно важно при отеке легких). Доза, необходимая для адекватного обезболивания, зависит от индивидуальной чувствительности, возраста, размеров тела. Перед использованием 10 мг морфина гидрохлорида или сульфата разводят как минимум в 10 мл 0,9% раствора хлорида натрия или дистиллированной воды. Первоначально следует ввести в/в медленно 2-4 мг лекарственного вещества. При необходимости введение повторяют каждые 5-15 мин по 2-4 мг до купирования боли или возникновения побочных эффектов, не позволяющих увеличить дозу. Применять лекарственные средства для профилактики осложнений наркотических анальгетиков не следует.
- Рекомендуется использование транквилизатора у больных с признаками выраженного беспокойства и возбуждения [2-4].
Уровень убедительности рекомендаций IIa (Уровень достоверности доказательств С).
Комментарии: Для уменьшения страха обычно достаточно создать спокойную обстановку и ввести наркотический анальгетик. При выраженном возбуждении могут потребоваться транквилизаторы (например, диазепам ** в/в 2,5-10 мг). Важное значение для эмоционального комфорта больного имеет соответствующий стиль поведения персонала, разъяснение диагноза, прогноза и плана лечения. У больных с сохраняющимся беспокойством и нарушенным поведением, а также симптомами отмены при никотиновой зависимости разумно использовать транквилизаторы (минимальные дозы производных бензодиазепина на ограниченный период времени). При тяжелых симптомах, связанных с отменой никотина, может потребоваться заместительная терапия. При возбуждении и делирии достаточно эффективно и безопасно в/в введение галоперидола ** . Изменение восприятия, особенно после введения фибринолитика, подозрительно в отношении внутричерепного кровоизлияния, которое следует исключить до применения седативных препаратов.
3.1.2. Неантитромботическое лечение
Уровень убедительности рекомендаций I (Уровень достоверности доказательств С).
Комментарии: У больных без выраженной гипоксемии обычно достаточно дыхания кислородом через носовые катетеры со скоростью 2-8 л/мин. При тяжелой СН, отеке легких или механических осложнениях ИМпST для коррекции выраженной гипоксемии могут потребоваться различные способы поддержки дыхания, включая интубацию трахеи с ИВЛ. Убедительных свидетельств пользы от применения кислорода у больных с неосложненным ИМпST нет.
- Рекомендуется внутривенная инфузия нитратов в ранние сроки заболевания для симптоматического лечения больных с артериальной гипертензией (АГ), СН или возобновляющейся ишемией миокарда, если нет противопоказаний (артериальная гипотония, ИМ ПЖ, использование ингибиторов фосфодиэстеразы V в предшествующие 48 часов) [2-4].
Уровень убедительности рекомендаций IIa (Уровень достоверности доказательств С).
Комментарии: Критерий адекватно подобранной скорости введения (дозировки) при в/в инфузии нитратов – уровень систолического АД, который может быть снижен на 10-15% у нормотоников и на 25-30% у лиц с АГ, но не ниже 100 мм рт. ст. Обычная начальная скорость введения нитроглицерин ** а 10 мкг/мин. При ее неэффективности скорость инфузии увеличивается на 10-15 мкг/мин каждые 5-10 мин, пока не будет достигнут желаемый эффект. Если достичь целевого уровня снижения АД не удается, даже увеличив скорость инфузии нитроглицерина ** до 200 мкг/мин, от введения препарата следует отказаться. Убедительных свидетельств в пользу применения нитратов при неосложненном течении ИМпST нет. Если артериальная гипотония препятствует применению надлежащих доз бета-адреноблокаторов или иАПФ, от применения нитратов можно отказаться.
- Рекомендуется пероральный прием бета-адреноблокаторов всем больным с ИМпST, не имеющим противопоказаний [2-4].
Уровень убедительности рекомендаций IIa (Уровень достоверности доказательств В).
Комментарии: В ранние сроки ИМпST важнейшее значение имеет выбор приемлемой дозы препарата, которая не должна быть слишком большой при опасности возникновения осложнений (прежде всего – наличии СН). О достаточности дозы обычно судят по желаемой ЧСС. Она не должна быть ниже 44-46 ударов в 1 мин в ночные часы в покое. Абсолютные противопоказания к использованию бета-адреноблокаторов при ИМпST: кардиогенный шок, тяжелая обструктивная болезнь легких в стадии обострения, атриовентрикулярная (АВ) блокада II-III ст. у больных без функционирующего искусственного водителя ритма сердца, аллергия. Относительные противопоказания: клинические проявления СН, свидетельства наличия низкого сердечного выброса, систолическое АД 0,24 сек, обструктивная болезнь легких в анамнезе, наличие факторов риска возникновения кардиогенного шока. У больных с существенным нарушением сократимости ЛЖ начинать лечение следует с минимальных доз бета-адреноблокаторов. При наличии упорной тахикардии до начала использования β-адреноблокаторов желательно выполнить ЭхоКГ. При наличии противопоказаний к бета-адреноблокаторам в ранние сроки ИМпST возможность их назначения следует регулярно переоценивать. Титрование дозы препаратов для приема внутрь разумно начать через 24-48 ч после исчезновения выраженной брадикардии, артериальной гипотензии, выраженной СН, АВ блокады.
- Рекомендуется пероральный прием бета-адреноблокаторов при ИМпST больным с сердечной недостаточностью (СН) или сниженной фракцией выброса (ФВ) левого желудочка (ЛЖ) [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств А).
- Рекомендуется внутривенное введение бета-адреноблокаторов при ИМпST больным с высоким АД, тахикардией, не имеющим признаков СН [2-4].
Уровень убедительности рекомендаций IIa (Уровень достоверности доказательств В).
- Не рекомендуется внутривенное введение бета-адреноблокаторов при ИМпST не рекомендовано больным с артериальной гипотонией или СН [2-4].
Уровень убедительности рекомендаций III (Уровень достоверности доказательств В).
- Рекомендуется использовать верапамил ** при непереносимости бета-адреноблокаторов у больных без СН, сниженной ФВ ЛЖ и других противопоказаний для вторичной профилактики ИМ [2-4].
Уровень убедительности рекомендаций IIb (Уровень достоверности доказательств B).
Комментарии: Широкое применение блокаторов кальциевых каналов при ИМпST скорее ухудшает исходы заболевания и поэтому не рекомендуется. Верапамил или дилтиазем могут использоваться только в отсутствие симптомов СН, существенной сократительной дисфункции ЛЖ, нарушений синоатриальной и АВ проводимости и брадиаритмий. Если контролировать стенокардию или АГ другими средствами не удается, возможно применение длительно действующих производных дигидропиридина в дополнение к бета-адреноблокаторам.
- Рекомендуется начать титрование дозы ингибиторов АПФ в первые 24 часа ИМпST у больных с СН, сниженной ФВ ЛЖ, сахарным диабетом или ИМ передней локализации [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств А).
Комментарии: Общий принцип лечения – постепенно увеличивать (титровать) дозу до рекомендуемой (целевой), которая по данным клинических исследований обеспечивает положительное влияние на прогноз, а если это невозможно, до максимально переносимой (Приложение Г7). Противопоказания для начала использования ингибиторов АПФ: систолическое АД
- Рекомендуется использовать ингибиторы АПФ у всех больных ИМпST, не имеющих противопоказаний [2-4].
Уровень убедительности рекомендаций IIa (Уровень достоверности доказательств А).
- Рекомендуется использовать блокаторы рецептора ангиотензина, предпочтительно валсартан, вместо ингибиторов АПФ при ИМпST у больных с СН, сниженной ФВ ЛЖ или АГ, которые не переносят ингибиторы АПФ [2-4].
Комментарии: Начальная доза валсартана составляет 20 мг/сут; при хорошей переносимости дозу препарата постепенно увеличивают вплоть до 160 мг 2 раза в сутки.
Уровень убедительности рекомендаций I (Уровень достоверности доказательств В).
- Рекомендуется использовать блокаторы рецептора альдостерона, предпочтительно эплеренон, в добавление к бета-адреноблокаторам и ингибиторам АПФ у больных с ИМпST и ФВ ЛЖ ≤40% в сочетании с СН или сахарным диабетом при условии, что нет почечной недостаточности и гиперкалиемии [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств В).
Комментарии: В большинстве случаев титрование дозы можно начать на 3-14 сутки заболевания при условии, что уровень креатинина в крови у мужчин составлял
- Рекомендуется поддерживать концентрацию калия в крови в диапазоне 4,0±0,5 ммоль/л, магния >1 ммоль/л [2-4].
Уровень убедительности рекомендаций IIa (Уровень достоверности доказательств С).
Комментарии: Введение «поляризующих смесей», содержащих глюкозу, калий и инсулин, а также солей магния больным без гипомагниемии, не приносит пользы и не рекомендуется.
- Рекомендуется как можно быстрее определить уровень липидов в крови натощак, предпочтительно в первые 24 ч после госпитализации [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств С).
- Рекомендуется начать или продолжить лечение высокой дозой статинов (в частности, аторвастатином ** в суточной дозе 80 мг) вне зависимости от исходного уровня холестерина, если к ним нет противопоказаний и высокие дозы статинов хорошо переносятся [2-4].
Уровень убедительности рекомендацийI (Уровень достоверности доказательств А).
- Рекомендуется у больных с гипергликемией в острой фазе заболевания поддерживать концентрацию глюкозы в крови ≤11,0 ммоль/л (200 мг/дл), избегая гипогликемии (
Уровень убедительности рекомендацийIIa (Уровень достоверности доказательств В).
3.1.3. Антитромботическая терапия
- Рекомендуется неопределенно долгое использование АСК ** в дозе 75-100 мг 1 раз в сутки при отсутствии противопоказаний [2-4].
Уровень убедительности рекомендацийI (Уровень достоверности доказательств А).
Комментарии: Для достижения быстрого эффекта рекомендуется однократная нагрузочная доза АСК ** 250 мг. Для тех, кто не может проглотить таблетку, возможно внутривенное введение 150 мг АСК ** (эта доза эквивалентна 300 мг, даннымper os).
- Рекомендуется сочетание АСК ** с ингибитором Р2Y12-рецепторов тромбоцитов (двойная антитромбоцитарная терапия – ДАТТ), если не планируется срочная операция коронарного шунтирования (КШ) и нет противопоказаний (чрезмерный риск серьезных кровотечений) [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств А).
- Рекомендуется тикагрелор (нагрузочная доза 180 мг, поддерживающая — 90 мг 2 раза в сутки) при отсутствии противопоказаний (внутричерепное кровоизлияние в анамнезе, продолжающееся кровотечение) в добавление к АСК ** в случаях, когда планируется выполнить первичное ЧКВ [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств В).
Комментарии: Перейти на прием тикагрелора (дать нагрузочную дозу) можно и у больных, получивших клопидогрел. Прием тикагрелора не исключает возможность применение блокаторов ГП IIb/IIIa при выполнении ЧКВ. При одновременном применении АСК и тикагрелора перед операцией КШ и другими крупными хирургическими вмешательствами тикагрелор следует отменить за 5-7 суток, кроме случаев, когда опасность отказа от срочного вмешательства превосходит риск повышенной кровопотери.
- Рекомендуется клопидогрел ** (нагрузочная доза 300-600 мг, поддерживающая — 75 мг 1 раз в сутки) в добавление к АСК ** у больных, которые не могут получить тикагрелор или нуждаются в приеме пероральных антикоагулянтов [2-4].
Уровень убедительности рекомендацийI (Уровень достоверности доказательств А).
Комментарии: Обычная величина нагрузочной дозы составляет 300 мг; при планирующемся первичном ЧКВ ее следует увеличить до 600 мг. Оправданность применения нагрузочной дозы у лиц старше 75 лет, которым не предполагается проведение первичного ЧКВ, не установлена (рекомендуемая величина первой дозы клопидогрела ** в этих случаях – 75 мг). При одновременном применении АСК и клопидогрела ** перед операцией КШ и другими крупными хирургическими вмешательствами клопидогрел ** следует отменить за 5-7 суток, кроме случаев, когда опасность отказа от срочного вмешательства превосходит риск повышенной кровопотери. Клопидогрел ** может использоваться вместо АСК, когда ее применение невозможно из-за аллергии или выраженных желудочно-кишечных расстройств в ответ на прием препарата.
- Рекомендуется продолжать ДАТТ в течение 1 года вне зависимости от тактики лечения и типа установленного стента, если нет противопоказаний (в частности, чрезмерного риска кровотечений) [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств С).
- Рекомендуется использования ДАТТ более 1 года у отдельных больных с высоким риском тромботических осложнений и низким риском кровотечений [2-4].
Уровень убедительности рекомендаций IIb (Уровень достоверности доказательств А).
Комментарии: Имеются указания, что у больных высокого риска, переживших первый год лечения без осложнений, продление ДАТТ (сочетание АСК ** с тикагрелором в дозе 60 мг 2 раза в сутки или клопидогрелом ** в дозе 75 мг 1 раз в сутки) более 1 года существенно снижает количество ишемических событий. Однако при этом отмечено достоверное увеличение частоты крупных кровотечений.
- Рекомендуется минимальная длительность ДАТТ после установки голометаллических стентов (ГМС) 1 месяц [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств С).
- Рекомендуется минимальная длительность ДАТТ после установки стентов, выделяющих лекарства (СВЛ), 3-6 месяцев [2-4].
Уровень убедительности рекомендаций IIb (Уровень достоверности доказательств B).
- Рекомендуется назначение ингибиторов протонного насоса у больных, получающих ДАТТ, с высоким риском желудочно-кишечного кровотечения (кровотечение или язва ЖКТ в анамнезе, прием НПВС, антикоагулянтов, кортикостероидов, а также имеющие как минимум два из нижеперечисленных факторов риска: возраст ≥ 65 лет, диспепсия, гастроэзофагеальный рефлюкс, Helicobacter pylori, хроническое употребление алкоголя) [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств В).
- Рекомендуется использовать ингибиторы ГП IIb/IIIa-рецепторов тромбоцитов при ЧКВ и широком применении ДАТТ в случае возникновения тромботических осложнений или высокого, по мнению оператора, риска их развития (выраженный исходный внутрикоронарный тромбоз, феномен slow-reflow или no-reflow) [2-4].
Уровень убедительности рекомендаций IIa (Уровень достоверности доказательств C).
Комментарии: Одно из оснований для введения ингибиторы ГП IIb/IIIa-рецепторов тромбоцитов- отсутствиеуверенности, что к началу проведения ЧКВ удастся добиться нужного антиагрегантного действия с помощью ДАТТ. Основным осложнением, ограничивающим применение ингибиторы ГПIIb/IIIa-рецепторов тромбоцитов, являются кровотечения. Факторы, способствующие передозировке препаратов,— пожилой возраст, женский пол, почечная недостаточность, малая масса тела, сахарный диабет и ХСН. Применение ингибиторов ГПIIb/IIIa-рецепторов тромбоцитов может вызывать тромбоцитопению. Ингибиторы ГПIIb/IIIa-рецепторов тромбоцитов должны использоваться вместе с антиагрегантами и антикоагулянтами.
- Рекомендуется парентеральное введение антикоагулянтов [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств А).
- Рекомендуется при выборе парентерального антикоагулянта учитывать риск возможных ишемических осложнений и кровотечений [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств В).
- Рекомендуется использовать нефракционированный гепарин (НФГ) ** во время ЧКВ, при тромболитической терапии (ТЛТ), для профилактики и лечения артериальных или венозных тромбозов и тромбоэмболий (ТЭ) [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств C).
Комментарии: Во время ЧКВ НФГ вводят в/в болюсами, добиваясь поддержания определенных значений активированного времени свертывания крови АВС, в остальных случаях показана в/в инфузия под контролем активированного частичного тромбопластинового времени (АЧТВ). При отсутствии необходимости в применении более высоких доз антикоагулянтов, возможно подкожное введение низких доз НФГ ** для профилактики венозного тромбоза и тромбоэмболии легочных артерий (приложение Г7).
- Рекомендуется использовать эноксапарин натрия ** при ТЛТ, во время ЧКВ, для профилактики и лечения артериальных или венозных тромбозов и тромбоэмболий (ТЭ) [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств А).
Комментарии: Дозы препарата при его использовании в разных клинических ситуациях приведены в приложении Г7.
- Рекомендуется использовать фондапаринукс натрия при ТЛТ стрептокиназой, у больных, оставшихся без реперфузионного лечения, для профилактики и лечения венозного тромбоза и тромбоэмболии легочных артерий (ТЭЛА) [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств А).
Комментарии: Дозы препарата при его использовании в разных клинических ситуациях приведены в приложении Г7.
- Не рекомендуется использовать фондапаринукс натрия при первичном ЧКВ [2-4].
Уровень убедительности рекомендаций III (Уровень достоверности доказательств В).
Комментарии: Если ЧКВ выполняется у больных, получающих фондапаринкус натрия, во время процедуры необходимо вводить обычные дозы НФГ ** .
- Рекомендуется использовать бивалирудин при первичном ЧКВ в качестве альтернативы комбинации НФГ ** и антагонистов ГП IIb/IIIa-рецепторов тромбоцитов. Инфузию следует начинать одновременно с ЧКВ и продолжать до 4 ч после его завершения [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств В).
- Рекомендуется использовать прекратить введение антикоагулянтов после успешного завершения ЧКВ , если к ним нет иных показаний [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств С).
- Рекомендуется применение ривароксабана ** в дозе 2,5 мг 2 раза в сутки на срок до 1 года после прекращения лечения парентеральными антикоагулянтами у больных с ИМпST, получающих АСК ** и клопидогрел ** , не нуждающихся в длительном использовании антикоагулянтов, имеющих высокий риск ишемических осложнений и низкий риск кровотечений (как минимум без инсульта/транзиторной ишемической атаки в анамнезе)[2-4].
Уровень убедительности рекомендаций IIb (Уровень достоверности доказательств В).
- Рекомендуется тройная антитромботическая терапия, состоящая из АСК ** , клопидогрела ** и пероральных антикоагулянтов, после коронарного стентирования у больных, нуждающихся в длительном применении антикоагулянтов (фибрилляция предсердий [ФП], механические протезы клапанов сердца, тромбоз полости ЛЖ, недавние тромбоз глубоких вен или тромбоэмболия легочных артерий) [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств С).
Комментарии: Тройная антитромботическая терапия приводит к существенному увеличению риска кровотечений, поэтому ее длительность должна быть максимально сокращена. У больных с ФП для оценки риска инсульта и кровотечений рекомендуется использовать шкалы CHA2DS2-VAScиHAS-BLED.Доза антагонистов витамина К в составе тройной антитромботической терапии должна быть минимально эффективной (МНО 2,0-2,5). Применение пероральных антикоагулянтов прямого действия после ОКС малоизучено и их нельзя использовать у больных с механическими протезами клапанов сердца и при гемодинамически значимом митральном стенозе. Для защиты желудка при назначении тройной терапии разумно использовать ингибиторы протонного насоса. Алгоритм выбора антитромботической терапии у больных с ИМпST и фибрилляцией предсердий представлен в Приложении Г8.
- Рекомендуется продолжать лечение антикоагулянтами как минимум 3 месяца у больных с тромбом в полости ЛЖ [2-4].
Уровень убедительности рекомендаций IIa (Уровень достоверности доказательств В).
Комментарии: При тромбе в полости ЛЖ пероральные антикоагулянты прямого действия не изучены, поэтому препаратами выбора должны оставаться антагонисты витамина К.
- Не рекомендуется использовать тикагрелор в составе тройной антитромботической терапии [2-4].
Уровень убедительности рекомендаций III (Уровень достоверности доказательств C).
- Рекомендуется определять длительность и состав антитромботической у больных с с ФП, подвергнутых ЧКВ, терапии с учетом риска тромбоэмболических осложнений и кровотечений [2-4].
Уровень убедительности рекомендацийI (Уровень достоверности доказательств C).
Комментарии: Алгоритм выбора антитромботической терапии у больных с ИМпST и фибрилляцией предсердий представлен в Приложении Г8.
- Рекомендуется продолжать тройную антитромботическую терапию в течение 6 месяцев вне зависимости от типа установленного стента при условии низкого риска кровотечений. У больных с высоким риском кровотечений рекомендуется длительность тройной антитромботической терапии 1 месяц. В последующем вплоть до 1 года рекомендуется сочетание перорального антикоагулянта и одного антиагреганта (клопидогрела ** или АСК ** ) (рисунок 3) [2-4].
Уровень убедительности рекомендаций IIa (Уровень достоверности доказательств C).
- Рекомендуется сочетание перорального антикоагулянта и клопидогрела вместо тройной антитромботической терапии у отдельных больных с высоким риском кровотечений и низким риском ишемических осложнений ** [2-5].
Уровень убедительности рекомендаций IIb (Уровень достоверности доказательств В).
Уровень убедительности рекомендаций IIa (Уровень достоверности доказательств C).
Комментарии: У больных, получающих антагонисты витамина К, при более высоких значениях МНО парентерального введения антикоагулянты во время ЧКВ не требуется.
- Рекомендуется использовать лучевой доступ при КАГ и ЧКВ у больных, получающих пероральные антикоагулянты [2-5].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств A).
- Рекомендуется использовать СВЛ нового поколения у больных, получающих пероральные антикоагулянты [2-5].
Уровень убедительности рекомендаций IIa (Уровень достоверности доказательств B).
- Рекомендуется в течение года использовать сочетание антикоагулянта с одним антитромбоцитарным препаратом (клопидогрелом ** или АСК ** ) при консервативной тактике лечения больных, постоянно принимающим пероральные антикоагулянты [2-5].
Уровень убедительности рекомендаций IIa (Уровень достоверности доказательств C).
3.2. Хирургическое лечение
3.2.1. Показания к реперфузионной терапии
- Рекомендуется реперфузионная терапия всем больным с ОКСпST и длительностью симптомов
Уровень убедительности рекомендаций I (Уровень достоверности доказательств А).
Комментарии: ЭКГ критериями для начала реперфузионной терапии являются стойкие подъемы сегментаST≥0,1 мВ как минимум в двух смежных отведениях ЭКГ (≥ 0,25 мВ у мужчин до 40 лет/0,2 мВ у мужчин старше 40 лет и ≥0,15 мВ у женщин в отведенияхV2-V3) при отсутствии гипертрофии левого желудочка или (предположительно) остро возникшая блокада левой ножки пучка Гиса (особенно при конкордантных подъемах сегментаSTв отведениях с положительным комплексомQRS). При наличии депрессии сегментаST≥0,05 мВ в отведенияхV1-V3, особенно с позитивными зубцами Т, рекомендуется зарегистрировать ЭКГ в отведенияхV7-V9(выявление подъемовST≥0,05 мВ/≥0,01 мВ у мужчин моложе 40 лет является основанием для реперфузионного лечения). Сочетании депрессий сегментаST≥0,1 мВ во многих отведениях >0,1 мВ в сочетании с подъемами сегментаSTв отведенияхaVRи/или V1,свидетельствующих о многососудистом поражении или поражении ствола левой коронарной артерии. В этих случаях предпочтительна срочная КАГ для уточнения тактики лечения – ЧКВ или операция КШ.
- Рекомендуется реперфузионная терапия (предпочтительно первичное ЧКВ) больным с ИМпST при сохраняющейся ишемии миокарда и длительностью симптомов >12 часов [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств С).
- Рекомендуется первичное ЧКВ у стабильных больных с ИМпST через 12-24 часа от начала симптомов [2-4].
Уровень убедительности рекомендаций IIb (Уровень достоверности доказательств B).
3.2.2. Методы реперфузионного лечения
- Рекомендуется предпочесть первичное ЧКВ, ТЛТ в случаях, когда оно может быть выполнено опытной специалистов в первые 120 минут после контакта с медицинским работником [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств А).
Комментарии: При ЧКВ должно использоваться сочетание АСК ** , блокатора P2Y12 рецепторов тромбоцитов (тикагрелор или клопидогрел ** ) и парентеральнго введения антикоагулянта (Приложении Г8). В отдельных случаях показано введение блокатора ГПIIb/IIIaтромбоцитов.
- Рекомендуется предпочесть первичное ЧКВ, ТЛТ у больных с тяжелой острой СН, включая кардиогенный шок, за исключением случаев, когда задержка до инвазивного вмешательства слишком большая или больной обратился за помощью в очень ранние сроки заболевания [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств В).
- Рекомендуется в большинстве случаев при первичном ЧКВ ограничиться вмешательством на инфаркт-связанном сосуде, кроме больных с кардиогенным шоком и сохранения ишемии после вмешательства на стенозе, который представляется ответственным за ИМ [2-4,6].
Уровень убедительности рекомендаций IIa (Уровень достоверности доказательств В).
- Рекомендуется ЧКВ в не инфаркт-связанной артерии у отдельных гемодинамически стабильных больных с многососудистым поражением, либо во время первичного ЧКВ, либо в качестве плановой поэтапной процедуры [2-4,6].
Уровень убедительности рекомендаций IIb (Уровень достоверности доказательств В).
- Рекомендуется при первичном ЧКВ предпочесть коронарное стентирование баллонной ангиопластике [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств А).
- Рекомендуется при наличии соответствующего опыта при первичном ЧКВ предпочесть лучевой доступ бедренному [2-4].
Уровень убедительности рекомендаций IIa (Уровень достоверности доказательств B).
- Рекомендуется использовать СВЛ (предпочтительно второго поколения), а не ГМС, у больных с ожидаемой хорошей приверженностью к лечению, не имеющих противопоказаний к длительной ДАТТ и не нуждающихся в длительном использовании антикоагулянтов [2-4].
Уровень убедительности рекомендаций IIa (Уровень достоверности доказательств А).
Комментарий: Не исключено, чтосовременные СВЛ предпочтительнее ГМС и при непродолжительной ДАТТ.
- Не рекомендуется рутинное выполнение аспирации тромба [2-4,6].
Уровень убедительности рекомендаций III (Уровень достоверности доказательств А).
- Рекомендуется начинать ТЛТ в первые 30 минут после контакта с медицинским работником, если у больного нет противопоказаний [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств В).
Комментарии: Абсолютные противопоказания к ТЛТ — ранее перенесенный геморрагический инсульт или нарушение мозгового кровообращения неизвестной этиологии; ишемический инсульт в предшествующие 6 месяцев; повреждения ЦНС или ее новообразования или артериовенозные мальформации; недавняя серьезная травма/хирургическое вмешательство/травма головы (в течение предыдущих 3-х недель); желудочно-кишечное кровотечение (в течение последнего месяца); геморрагический диатез (кроме menses); расслоение аорты; пункция некомпрессируемых сосудов (биопсия печени, спинно-мозговая пункция) в течение предыдущих 24 часов. Относительные противопоказания к ТЛТ — транзиторная ишемическая атака в предыдущие 6 месяцев; наличие плохо контролируемой АГ (в момент госпитализации – систолическое АД >180 мм рт.ст. и/или ДАД>110 мм рт.ст.); тяжелое заболевание печени; инфекционный эндокардит; травматичная или длительная (>10 мин) сердечно-легочная реанимация; для стрептокиназы – введение стрептокиназы, в т.ч. модифицированной, более 5 суток назад или известная аллергия на нее; беременность и 1-я неделя после родов; обострение язвенной болезни; прием антагонистов витамина К (чем выше МНО, тем выше риск кровотечения). Помимо фибринолитика при ТЛТ должны использоваться сочетание АСК ** , клопидогрела ** и парентерального введения антикоагулянта (Приложении Г8).
- Рекомендуется начать ТЛТ на догоспитальном этапе [2-4].
Уровень убедительности рекомендаций IIa (Уровень достоверности доказательств А).
- Рекомендуется при ТЛТ предпочесть фибрин-специфичный фибринолитик [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств В).
- Рекомендуется после ТЛТ транспортировать больных в медицинское учреждение, выполняющее неотложные ЧКВ [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств А).
Уровень убедительности рекомендаций I (Уровень достоверности доказательств А).
- Рекомендуется при возобновлении ишемии миокарда или свидетельствах реокклюзии после первоначально успешной ТЛТ срочное ЧКВ [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств В).
- Рекомендуется немедленная коронарная ангиография (КАГ) с намерением выполнить реваскуляризацию миокарда у больных с СН, включая кардиогенный шок [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств А).
- Рекомендуется КАГ с намерением выполнить ЧКВ в инфаркт-связанной артерии после успешной ТЛТ [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств А).
- Рекомендуется задержка до КАГ с намерением выполнить ЧКВ в инфаркт-связанной артерии составляет 3-24 часа у стабильных больных после успешной ТЛТ в качестве оптимальной [2-4].
Уровень убедительности рекомендаций IIа (Уровень достоверности доказательств А).
3.2.3. Осложнения ИМ
3.2.3.1. Застой в малом круге кровообращения. Отек легких
- Рекомендуется ранняя реваскуляризация миокарда. Выбор между ЧКВ и операцией КШ определяется особенностями поражения коронарного русла [2-4].
Уровень убедительности рекомендацийI (Уровень достоверности доказательств С).
Комментарий: ЧКВ предпочтительнее ТЛТ.
- Рекомендуется срочно выполнить ЭхоКГ для оценки выраженности сократительной дисфункции и поиска механических осложнений ИМ у больных с застоем в легких и особенно с отеком легких [2-4].
Уровень убедительности рекомендацийI (Уровень достоверности доказательств С).
Уровень убедительности рекомендацийI (Уровень достоверности доказательств С).
- Рекомендуется в/в введение 20-40 мг фуросемида ** , при необходимости повторно с интервалом в 1-4 часа [2-4].
Уровень убедительности рекомендацийI (Уровень достоверности доказательств С).
Комментарии: У больных с выраженной задержкой жидкости, недостаточным ответом на введение препарата могут применяться более высокие дозы фуросемида.
- Рекомендуется в/в введение морфина при отеке легких [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств С).
- Рекомендуется в/в инфузия нитратов у больных без артериальной гипотонии [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств С).
- Рекомендуются ингибиторы АПФ при отсутствии артериальной гипотонии, гиповолемии и выраженной почечной недостаточности [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств А).
- Рекомендуются блокаторы рецептора ангиотензина (предпочтительно валсартан) при непереносимости ингибиторов АПФ [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств B).
- Рекомендуется блокатор рецептора альдостерона (предпочтительно эплеренон) у больных с ФВ ЛЖ ≤40% при отсутствии выраженной почечной недостаточности и гиперкалиемии [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств B).
- Рекомендуется краткосрочная инфузия кардиотонических лекарственных средств (добутамина, допамина) при рефрактерном отеке легких, особенно в сочетании с артериальной гипотонией, которая не связана с гиповолемией [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств С).
- Рекомендуется краткосрочная инфузия левосимендана, при рефрактерном отеке легких у больных без артериальной гипотонии и гиповолемии, особенно если отек легких развился на фоне продолжающегося приема бета-адреноблокаторов [2-4].
Уровень убедительности рекомендаций IIb (Уровень достоверности доказательств C).
- Рекомендуется рассмотреть целесообразность использования различных способов поддержки кровообращения в наиболее тяжелых рефрактерных случаях, при механических осложнениях ИМ [2-4].
Уровень убедительности рекомендаций IIb (Уровень достоверности доказательств C).
3.2.3.2. Кардиогенный шок
- Рекомендуется максимально полная реваскуляризация миокарда с использованием ЧКВ или операции КШ вне зависимости от сроков начала заболевания [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств В).
- Рекомендуется тромболитическая терапия при недоступности реваскуляризации миокарда [2-4].
Уровень убедительности рекомендаций IIa (Уровень достоверности доказательств С).
- Рекомендуется срочно выполнить ЭхоКГ для оценки выраженности сократительной дисфункции и поиска механических осложнений ИМ [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств С).
- Рекомендуется оксигенотерапи, при необходимости поддержка дыхания, включая интубацию трахеи с механической ИВЛ [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств С).
- Рекомендуется убедиться в отсутствии гиповолемии [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств С).
Комментарии: У больных без признаков застоя в малом круге кровообращения можно оценить эффективность быстрого внутривенного введения жидкости. В сложных случаях может быть оправдана установка в легочную артерию плавающего катетера для контроля давления заполнения камер сердца.
- Рекомендуется инотропная поддержка с использованием внутривенной инфузии допмина, добутамина [2-4].
Уровень убедительности рекомендаций IIa (Уровень достоверности доказательств С).
- Рекомендуется внутривенная инфузия норэпинефрина при выраженной артериальной гипотонии, который в этой ситуации предпочтительнее допмина [2-4].
Уровень убедительности рекомендаций IIв (Уровень достоверности доказательств В).
- Рекомендуется рассмотреть использование различных способов поддержки кровообращения в наиболее тяжелых рефрактерных случаях, при механических осложнениях ИМ [2-4].
Уровень убедительности рекомендаций IIb (Уровень достоверности доказательств C).
3.2.3.3. Нарушения ритма и проводимости сердца
- Рекомендуется восстановление синусового ритма при возникновении фибрилляции предсердий (ФП) в случаях, когда провоцирующий фактор или причина могут быть устранены (например, ишемия миокарда) [2-4].
Уровень убедительности рекомендаций IIа (Уровень достоверности доказательств C).
- Рекомендовано в/в введение бета-адреноблокаторов, дилтиазема или верапамила для уменьшения ЧСС у больных с сохраняющейся ФП, не имеющих проявлений острой СН,. При необходимости в дальнейшем возможен переход на пероральный прием этих лекарственных средств [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств А).
Комментарий: Бета-адреноблокаторы, верапамил и дилтиазем неэффективны в восстановлении синусового ритма и применяются для урежения ЧСС при сохраняющейся ФП.
- Рекомендуется в/в введение амиодарона или дигоксина для уменьшения ЧСС у больных с сохраняющейся ФП в сочетании с острой СН, артериальной гипотонией [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств В).
- Рекомендуется немедленная электрическая кардиоверсия при невозможности адекватного контроля ЧСС с помощью медикаментозной терапии у больных с сохраняющейся ФП в сочетании с ишемией миокарда, артериальной гипотонией, выраженной СН [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств С).
Комментарии: Энергии электрического разряда приведены в Приложении Г10.
- Рекомендуется в/в введение амиодарона при недавно возникшей ФП у стабильных больных со структурной болезнью сердца для восстановления синусового ритма.
Уровень убедительности рекомендаций I (Уровень достоверности доказательств А).
- Рекомендуется электричеркая кардиоверсия/дефибрилляция у больных с устойчивой желудочковой тахикардией или фибрилляцией желудочков [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств С).
- Рекомендуется в/в введение амиодарона у больных с рецидивирующей или рефрактерной к электрической кардиоверсии мономорфной желудочковой тахикардией [2-4].
Уровень убедительности рекомендаций IIa (Уровень достоверности доказательств С).
- Рекомендуется в/в введение лидокаина у больных с рецидивирующей или рефрактерной к электрической кардиоверсии мономорфной желудочковой тахикардией [2-4].
Уровень убедительности рекомендаций IIb (Уровень достоверности доказательств С).
- Рекомендуется трансвенозная стимуляция у больных рефрактерной к электрической кардиоверсии или часто рецидивирующей на фоне медикаментозного лечения мономорфной желудочковой тахикардией для устранения аритмии [2-4].
Уровень убедительности рекомендаций IIа (Уровень достоверности доказательств С).
- Рекомендуется в/в введение бета-адреноблокаторов или амиодарона у больных с полиморфной желудочковой тахикардией [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств В для бета-адреноблокаторов, С для амиодарона).
- Рекомендуется срочная КАГ с намерением выполнить реваскуляризацию миокарда у больных с полиморфной желудочковой тахикардией в случаях, когда нельзя исключать ишемию миокарда [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств С).
- Рекомендуется в/в введение лидокаина у больных с полиморфной желудочковой тахикардией [2-4].
Уровень убедительности рекомендаций IIb (Уровень достоверности доказательств С).
- Рекомендуется выявление и устранение электролитных нарушений, а также возможное введение магния у больных с полиморфной желудочковой тахикардией [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств С).
- Рекомендуется подавляющая электрическая кардиостимуляция через катетер в правом делудочке или в/в инфузия изопреналина у больных с полиморфной желудочковой тахикардией [2-4].
Уровень убедительности рекомендаций IIa (Уровень достоверности доказательств С).
- Рекомендуется в/в введение атропина у больных с синусовой брадикардией, сопровождающейся артериальной гипотонией, АВ блокадой II степени типа Мобитц II или АВ блокадой III степени с брадикардией, которая вызывает артериальную гипотонию или СН. При его неэффективности рекомендована временная электрическая кардиостимуляция [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств С).
- Рекомендуется срочная КАГ с намерением выполнить реваскуляризацию миокарда у больных с синусовой брадикардией, сопровождающейся артериальной гипотонией, АВ блокадой II степени типа Мобитц II или АВ блокадой III степени с брадикардией, которая вызывает артериальную гипотонию или СН, не получивших реперфузионной терапии.
Уровень убедительности рекомендаций I (Уровень достоверности доказательств С).
- Рекомендуется оценить ФВ ЛЖ с помощью ЭхоКГ как минимум через 40 дней после ИМ у больных с ФВ ЛЖ ≤40% для оценки риска внезапной сердечной смерти и целесообразности имплантации кардиовертера-дефибриллятора [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств А).
4. Реабилитация
- Рекомендуется включение больных в программы по вторичной профилактике и реабилитации [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств А).
Комментарий: Правильно построенная программа физической и психологической реабилитацииспособствует повышению приверженности к медикаментозному лечению и мероприятиям по изменению образа жизни, включающим диету, регулярные физические нагрузки и отказ от курения. После определения индивидуальной переносимости физической нагрузки и оценки связанного с ней риска рекомендуется разработать программу реабилитации, при возможности включающую регулярные аэробные физические нагрузки (тренировки) как минимум 3 раза в неделю продолжительностью как минимум по 30 мин. Больных с малоподвижным образом жизни следует активно стимулировать к началу программ физической реабилитации с нагрузками небольшой интенсивности.
- Рекомендуется использование программ реабилитации, основанных на регулярной физической активности [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств В).
5. Профилактика
- Рекомендуется модификация факторов риска и изменение стиля жизни (диета, адекватная физическая нагрузка), отказ от курения и неопределенно долгое (при отсутствии побочных эффектов фактически пожизненное) использование несколько групп лекарственных средств [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств А).
Комментарии: Подходы к вторичной профилактике представлены в Приложении Г11.
6. Дополнительная информация, влияющая на течение и исход заболевания
Организация системы оказания помощи
- Рекомендуется оказание догоспитальной помощи бригадой Скорой медицинской помощи со специально обученным персоналом, оснащенная электрокардиографом (и при необходимости телеметрией), способная начать необходимое лечение, включая тромболитическеую терапию [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств B).
Комментарии: Особенности догоспитального лечения ИМпSTизложены в приложении Г8.
- Рекомендуется создание региональной системы оказания медицинской помощи, обеспечивающей быстрое и эффективное реперфузионное лечение ИМпST, организованное таким образом, чтобы максимальному числу больных было доступно первичное ЧКВ [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств B).
- Рекомендовано наличие в лечебных учреждениях, выполняющих первичное ЧКВ, службы, работающей 24 часа 7 дней в неделю и позволяющей начать вмешательство как можно быстрее, в пределах 60 минут после первого контакта больного с медицинским работником [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств B).
- Рекомендуется, чтобы все подразделения, вовлеченные в лечение ИМпST, имели письменно изложенный протокол лечения заболевания, согласованный с региональной структурой оказания помощи подобным больным [2-4].
Уровень убедительности рекомендаций I (Уровень достоверности доказательств С).
- Рекомендуется, чтобы больные, поступившие для первичного ЧКВ, доставлялись напрямую в ангиографическую лабораторию, минуя все другие подразделения стационара [2-4].
Уровень убедительности рекомендаций IIa (Уровень достоверности доказательств В).
Критерии оценки качества медицинской помощи
Критерий качества
Уровень достоверности доказательств
Уровень убедительности рекомендаций
Выполнено ЭКГ в течение 10 мин на месте первого контакта с медицинским работником
Выполнена определение уровня биохимических маркеров повреждения кардиомиоцитов в крови
Проведена стратификации риска неблагоприятного исхода на этапе диагностики
Проведен учет временных интервалов от момента обращения за медицинской помощью до начала реперфузионного лечения
Выполнено первичное ЧКВ в первые 120 мин после контакта с медицинским работником
Выполнена ТЛТ в первые 30 мин после контакта с медицинским работником
Выполнена реперфузионная терапия в первые 12 часов от начала симптомов
Выполнено лечение АСК **
Проведено лечение пероральным ингибитором Р2Y12-рецепторов тромбоцитов (тикагрелор или клопилогрел ** )
Выполнено использование антикоагулянта
Выполнено лечение ингибиторами АПФ или блокаторами ангиотензиновых рецепторов у больных с ФВ ЛЖ ФВ ≤40% или с клиническими проявлениями СН
Выполнено лечение бета-адреноблокаторами у больных с ФВ ЛЖ ФВ ≤40% или с клиническими проявлениями СН
Проведено лечение высокой доза статина
Выполнено ультразвуковое исследование сердца с оценкой ФВ ЛЖ до выписки из стационара
Выполнено включение больных в программу по вторичной профилактике и реабилитации
Список литературы
- Thygesen K, Alpert JS, Jaffe AS et al. ESC Committee for Practice Guidelines (CPG). Third universal definition of myocardial infarction. Eur Heart J 2012; 33: 2551—2567.
- Руда М.Я., Аверков О.В., Голицын С.П., Грацианский Н.А., Комаров А.Л., Панченко Е.П., Певзнер Д.В., Явелов И.С. Диагностика и лечение больных острым инфарктом миокарда с подъемами сегмента ST электрокардиограммы. Клинические рекомендации. Разработаны по поручению Минздрава России, утверждены Обществом специалистов по неотложной кардиологии и профильной комиссией по кардиологии. Кардиологический вестник 2014, том IX, №4: 3-60.
- Steg PG, James SK, Atar D et al. ESC Guidelines for the management of acute myocardial infarction in patients presenting with ST-segment elevation. The Task Force on the management of ST-segment elevation acute myocardial infarction of the European Society of Cardiology (ESC). Eur Heart J 2012; 33: 2569—2619.
- O»Gara P.T., Kushner F.G., Ascheim D.D., et al. 2013 ACCF/AHA Guideline for the Management of ST-elevation Myocardial Infarction. A Report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. JACC 2013; 61: 485—510.
- Roffi M., Patrono C., Collet J.P., et al. 2015 ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation: Task Force for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation of the European Society of Cardiology (ESC). Eur Heart J 2016; 37: 267—315.
- Levine G.N., Bates E.R., Blankenship J.C., et al. 2015 ACC/AHA/SCAI Focused Update on Primary Percutaneous Coronary Intervention for Patients With ST-Elevation Myocardial Infarction: An Update of the 2011 ACCF/AHA/SCAI Guideline for Percutaneous Coronary Intervention and the 2013 ACCF/AHA Guideline for the Management of ST-Elevation Myocardial Infarction: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines and the Society for Cardiovascular Angiography and Interventions. Circulation 2016; 133: 1135-1147.
Приложение А1. Состав рабочей группы
Авторы (рабочая группа по подготовке текста рекомендаций)
Руда М.Я. (председатель), проф., руководитель отдела неотложной кардиологии ФГБУ “Российский кардиологический научно-производственный комплекс” Министерства здравоохранения Российской Федерации, Лауреат Госпремии России, Президент Общества специалистов по неотложной кардиологии.
Аверков О.В., д.м.н., руководитель сосудистого центра, заместитель главного врача, ГКБ им. О. М. Филатова (г. Москва).
Голицын С.П., проф., руководитель отдела клинической электрофизиологии и рентгенохирургических методов лечения нарушений ритма сердца, ФГБУ “Российский кардиологический научно-производственный комплекс” Министерства здравоохранения Российской Федерации.
Грацианский Н.А., проф., руководитель лаборатории клинической кардиологии ФГБУ “Федеральный научно-клинический центр физико-химической медицины Федерального медико-биологического агентства”.
Комаров А.Л., д.м.н., ведущий научный сотрудник лаборатории клинических проблем атеротромбоза, ФГБУ «Российский кардиологический научно-производственный комплекс» Министерства здравоохранения Российской Федерации.
Панченко Е.П., проф., руководитель лаборатории клинических проблем атеротромбоза, ФГБУ «Российский кардиологический научно-производственный комплекс» Министерства здравоохранения Российской Федерации.
Певзнер Д.В., к.м.н., врач-кардиолог отдела неотложной кардиологии, ФГБУ “Российский кардиологический научно-производственный комплекс” Министерства здравоохранения Российской Федерации.
Явелов И.С., д.м.н., ведущий научный сотрудник отдела клинической кардиологии и молекулярной генетики, ФГБУ «ГНИЦ профилактической медицины» Министерства Здравоохранения Российской Федерации; профессор кафедры клинической фармакологии РНИМУ им. Н.И. Пирогова.
Комитет экспертов
д.м.н. Аверков О.В. (Москва), академик РАМН, проф. Алекян Б.Г. (Москва), проф. Аронов Д.М. (Москва), проф. Архипов М.В. (Екатеринбург), член-корр. РАН, проф. Барбараш О.Л. (Кемерово), проф. Белялов Ф.И. (Иркутск), проф. Болдуева С.А. (Санкт-Петербург), член-корр. РАН, проф. Бойцов С.А. (Москва), проф. Васильева Е.Ю. (Москва), проф. Габинский Я.Л. (Екатеринбург), проф. Галявич А.С. (Казань), проф. Говорин А.В. (Чита), проф. Гиляревский С.Р. (Москва), проф. Голицын С.П. (Москва), проф. Грацианский Н.А. (Москва), проф. Гринштейн Ю.И. (Красноярск), проф. Довгалевский П.Я. (Саратов), к.м.н. Ерегин С.Я. (Ярославль), проф. Затейщиков Д.А. (Москва), академик РАМН, проф. Карпов Р.С. (Томск), проф. Карпов Ю.А. (Москва), д.м.н. Комаров А.Л. (Москва), проф. Космачева Е.Д. (Краснодар), проф. Коц Я.И. (Оренбург), проф.Куимов А.Д. (Новосибирск), проф. Лопатин Ю.М. (Волгоград), проф. Марков В.А. (Томск), академик РАМН, проф. Мартынов А.И. (Москва), академик РАМН, проф. Моисеев В.С. (Москва), академик РАМН, проф. Оганов Р.Г. (Москва), проф. Панченко Е.П. (Москва), к.м.н. Певзнер Д.В. (Москва), проф. Перепеч Н.Б. (Санкт-Петербург), проф. Репин А.Н. (Томск), проф. Руда М.Я. (Москва), проф. Самко А.Н. (Москва), проф. Синицын В.Е. (Москва), д.м.н. Староверов И.И. (Москва), проф. Сулимов В.А. (Москва), проф. Сыркин А.Л. (Москва), проф. Терещенко С.Н. (Москва), проф. Туев А.В. (Пермь), д.м.н. Хрипун А.В. (Ростов-на-Дону), проф. Хрусталев О.А. (Ярославль), академик РАН, проф. Чазов Е.И. (Москва), академик РАН, проф. Чазова И.Е. (Москва), проф. Шалаев С.В. (Тюмень), проф. Шальнова С.А. (Москва), проф. Шпектор А.В. (Москва), д.м.н. Явелов И.С. (Москва), к.м.н. Яковлев А.Н. (Санкт-Петербург). проф. Якушин С.С. (Рязань).
Члены рабочей группы не имеют конфликта интересов.
Приложение А2. Методология разработки клинических рекомендаций
В основе рекомендаций лежат не только достижения отечественной медицины, но и результаты крупных международных кооперативных клинических исследований, метаанализов, регистров, которые являются основой и для других национальных и международных рекомендаций. Там, где это возможно, авторы пытались сделать отечественные рекомендации как можно более близкими к международным. Вместе с тем авторы старались учесть некоторые отличия и особенности практики оказания помощи больным с ОКС в нашей стране. Это касается и использования некоторых препаратов, и оценки эффективности методов лечения.
Целевая аудитория данных клинических рекомендаций:
- Врач кардиолог;
- Врач анестезиолог-реаниматолог;
- Врач скорой медицинской помощи;
- Врач терапевт;
- Врач общей практики.
Таблица П1.Уровни убедительностирекомендаций
Данные и/или всеобщее согласие, что конкретный метод лечения или процедура полезна, эффективна, имеет преимущества
Противоречивые данные и/или расхождение мнений о пользе/эффективности конкретного метода лечения или процедуры
Большинство данных/мнений говорит о пользе/эффективности
Данные/мнения о пользе/эффективности противоречивы
Данные и/или всеобщее согласие, что конкретный метод лечения или процедура не являются полезной или эффективной, а в некоторых случаях могут приносить вред
Таблица П2. Уровни достоверности доказательств
Данные многочисленных рандомизированных клинических исследований или мета-анализов
Данные одного рандомизированного клинического исследования или крупных нерандомизированных исследований
Согласованное мнение экспертов и/или небольшие исследования, ретроспективные исследования, регистры
Порядок обновления клинических рекомендаций.
Рекомендации обновляются рабочей группой при появлении существенных изменений в подходах к ведению больных ИМпST, но не реже 1 раза в 3 года.
Приложение А3. Связанные документы
- Приказ Министерства здравоохранения РФ от 1 июля 2015 г. № 405ан «Об утверждении стандарта специализированной медицинской помощи при остром инфаркте миокарда (с подъемом сегмента ST электрокардиограммы)».
- Приказ Минздрава России от 05.07.2016 N 457н «Об утверждении стандарта скорой медицинской помощи при остром трансмуральном инфаркте миокарда» (Зарегистрировано в Минюсте России 22.07.2016 N 42959).
Приложение Б. Алгоритмы ведения пациента
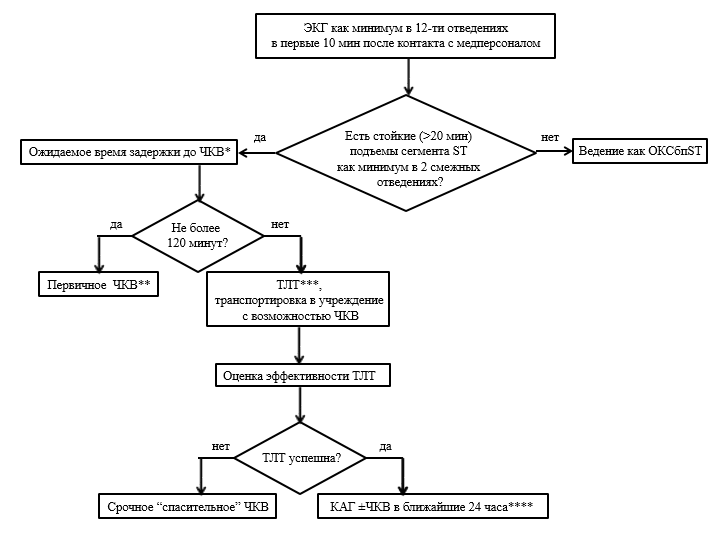
Примечания: КАГ – коронарная ангиография; ТЛТ – тромболитическая терапия; ЧКВ – чрескожное коронарное вмешательство (как правило со стентированием).
* от первого контакта с медицинским работником;
** предпочтительно в первые 60 мин и максимум в первые 90 мин от первого контакта с медицинским работником, предпочтительно в учреждениях с программой выполнения первичного ЧКВ 24 часа 7 дней в неделю;
*** предпочтительно на догоспитальном этапе, в течение 30 мин от первого контакта с медицинским работником;
****у стабильных больных предпочтительно через 3-24 часа после успешной ТЛТ.
Приложение В. Информация для пациентов
Инфаркт миокарда – гибель участка сердечной мышцы из-за недостаточной доставки к ней кислорода. В большинстве случаев это происходит из-за внезапно возникшей закупорки крупной коронарной артерии тромбом, который обычно возникает на поверхности разорвавшейся атеросклеротической бляшки. В ранние сроки инфаркта миокарда высока вероятность возникновения серьезных и угрожающих жизни осложнений. Кроме того, при быстром и качественном восстановлении просвета коронарной артерии удается спасти существенную часть сердечной мышцы и за счет этого уменьшить опасность неблагоприятного течения заболевания в будущем. Поэтому важнейшее значение имеет быстрое выявление признаков развивающегося инфаркта миокарда и своевременное обращение за медицинской помощью. На практике это означает, что при появлении определенных симптомов необходимо срочно вызвать бригаду Скорой медицинской помощи. Для инфаркта миокарда характерного возникновение боли или дискомфорта за грудиной, которые не проходят в покое и после приема нитроглицерина. Эти ощущения могут распространяться на шею, нижнюю челюсть, левую руку, под левую лопатку, в верхние отделы живота. Разобраться в ситуации и решить, что делать дальше, может специально обученный медицинский работник. Он зарегистрирует электрокардиограмму и, если результат укажет на прекращение кровотока по крупной коронарной артерии, выберет способ его восстановления. Это может быть, как немедленное введение лекарственного средства, разрушающего тромбы, так и срочная транспортировка в лечебное учреждение, где проходимость коронарной артерии будет восстановлена механическим способом и в сосуд установят специально разработанный каркас (стент). В любом случае из-за опасности серьезных осложнений лечение острого инфаркта миокарда проводится в специально созданных подразделениях лечебных учреждений.
Инфаркт миокарда – как правило проявление прогрессирования атеросклероза, которые развивается во всех артериях человека. Поэтому после выписки повышенная угроза повторного возникновения осложнений, связанных с нарушением целостности атеросклеротических бляшек, приводящим к тромбозу, будет сохраняться долго. Поэтому очень важно не прекращать лечение, начатое в стационаре, и сосредоточить усилия на устранении факторов, способствующих прогрессированию атеросклероза (бросить курить, обеспечить регулярную физическую активность, соблюдение диеты, разработанной для таких случаев, избавиться от избыточной массы тела, поддерживать низкие значения холестерина в крови с помощью статинов, обеспечить стойкую нормализацию АД при наличии артериальной гипертонии, поддерживать нормальный уровень сахара в крови при наличии сахарного диабета). Кроме того, при обширном поражении сердечной мышцы и/или осложнениях инфаркта миокарда требуется дополнительное лечение. Известно, что преждевременное прекращение приема необходимых препаратов существенно увеличивает риск возникновения повторного инфаркта миокарда и смерти от ишемической болезни сердца. Соответственно, этого делать нельзя, не посоветовавшись с врачом.
Приложение Г.
Приложение Г1. Критерии ОИМ
Термин «инфаркт миокарда» используется при присутствии признаков некроза миокарда в клинической ситуации, указывающей на наличие ишемии миокарда. При этом для диагностики ИМ достаточно одного из следующих критериев.
1. Повышение и/или снижение уровня биохимического маркера некроза миокарда в крови (предпочтительно сердечного тропонина, определенного высокочувствительным методом), если его концентрация как минимум в одной пробе крови превышает верхнюю границу нормы (ВГН), принятую в данной лаборатории (99-й перцентиль значений показателя в контрольной группе здоровых лиц при условии, что коэффициент вариации лабораторных определений не превышает 10%; при определении предела нормальных значений МВ КФК следует учитывать пол), и имеется как минимум одно из следующих свидетельств ишемии миокарда:
- клиническая картина ишемии миокарда;
- изменения ЭКГ, указывающие на появление ишемии миокарда (возникновение смещений ST—T, блокады ЛНПГ);
- появление патологических зубцов Q на ЭКГ;
- появление признаков потери жизнеспособного миокарда или нарушений локальной сократимости при использовании методик, позволяющих визуализировать сердце;
- выявление тромба в коронарной артерии при КАГ или патологоанатомическом исследовании.
2. Сердечная смерть на фоне симптомов, позволяющих заподозрить ишемию миокарда, у больных с предположительно остро возникшим подъемом сегмента ST или остро возникшей блокадой ЛНПГ, в случаях, когда летальный исход наступил до появления возможности забора образцов крови или раньше, чем отмечается повышение уровня биохимических маркеров некроза в крови.
3. По соглашению наличие ОИМ при ЧКВ констатируется при повышении сердечного тропонина >5 раз от ВГН у больных с исходно нормальными значениями этого показателя или при его повышении >20% от исходного, когда исходный уровень сердечного тропонина был повышен и стабилен или снижался, в сочетании как минимум с одним из следующих признаков: симптомы, предполагающие ишемию миокарда; новые ишемические изменения или новая блокада ЛНПГ на ЭКГ; ангиографическая потеря проходимости крупной коронарной артерии или боковой ветви, или феномен slow-/no-flow, или эмболизация; новая потеря жизнеспособного миокарда или новые зоны нарушения сократимости, выявленные при использовании методик, позволяющих визуализировать сердце.
4. Тромбоз стента, приведший к ИМ, диагностируется при наличии соответствующих свидетельств при КАГ или патологоанатомическом исследовании при наличии ишемии миокарда в сочетании с подъемом и/или снижением уровня маркеров некроза миокарда в крови, когда как минимум одно значение превышает ВГН.
5. По соглашению наличие ОИМ при операции КШ констатируется при повышении сердечного тропонина >10 раз от ВГН у больных с исходно нормальными значениями этого показателя в сочетании как минимум с одним из следующих признаков: новые патологические зубцы Q или новая блокада ЛНПГ на ЭКГ; ангиографически документированная новая окклюзия шунта или коронарной артерии; новая потеря жизнеспособного миокарда или новые зоны нарушения сократимости, выявленные при использовании методик, позволяющих визуализировать сердце.
Критерии ранее перенесенного ИМ
- Появление патологических зубцов Q на ЭКГ. Больной может помнить или не помнить предшествующие симптомы. Биохимические маркеры некроза миокарда могут нормализоваться в зависимости от времени, прошедшего после начала ИМ.
- Полученные с помощью визуализирующих методов свидетельства потери жизнеспособного миокарда в виде участка истончения стенки с нарушением локальной сократимости при отсутствии указаний на их неишемическую природу.
- Признаки перенесенного ИМ, выявленные при патологоанатомическом исследовании.
Приложение Г2. Особенности биохимической диагностики ИМ.
Для диагностики ИМ следует использовать сердечные тропонины Т или I (предпочтительны высокочувствительные методы определения), а при их недоступности — определение массы МВ КФК. На активность МВ КФК или общую КФК можно ориентироваться только в случаях, когда определение сердечных тропонинов или массы МВ КФК недоступно.
Использование методов определения сердечного тропонина «обычной» чувствительности. Первое определение должно быть выполнено при поступлении в стационар; при отсутствии клинически значимого повышения необходимо повторное определение через 6—9 ч, а при нормальных значениях у больных с сохраняющимся клиническим подозрением на ОКС — повторно через 12—24 ч.
Использование высокочувствительных методов определения сердечного тропонина. Определение должно быть выполнено при поступлении в стационар, через 3—6 ч после появления симптомов (или после первого определения, если нет точных сведений о времени появления симптомов), а при нормальных значениях у больных с сохраняющимся клиническим подозрением на ОКС и в более поздние сроки заболевания. Предложены алгоритмы диагностики и/или исключения острого ИМ на основании двух определений с интервалом в 1 и 3 ч. Уровень сердечного тропонина в крови и величина его изменения при повторном определении, достаточные для диагностики острого ИМ, зависят от метода определения.
Если уровень сердечного тропонина в крови остается повышенными после недавно перенесенного ИМ, диагноз повторного ИМ выставляют при подъеме сердечного тропонина не менее чем на 20% от уровня, отмеченного сразу после ангинозного приступа (при условии, что временной интервал до повторного забора крови составляет как минимум 3—6 ч).
Приложение Г3. Клиническая классификация типов ИМ.
Тип 1. ИМ, развившийся без видимых причин (спонтанно), в результате первичного нарушения коронарного кровотока, обусловленного образованием эрозии, разрыва, трещины или диссекции АБ с появлением тромба в просвете коронарной артерии.
Тип 2. ИМ, развившийся в результате ишемии, связанной с повышением потребности миокарда в кислороде и/или уменьшения его доставки к миокарду, например, при спазме или эмболии КА, анемии, нарушениях ритма сердца, анемии, дыхательной недостаточности, АГ или гипотензии.
Тип 3. Сердечная смерть на фоне симптомов, позволяющих заподозрить ишемию миокарда, у больных с предположительно остро возникшим подъемом сегмента ST или остро возникшей блокадой ЛНПГ, в случаях, когда летальный исход наступил до появления возможности забора образцов крови или раньше, чем отмечается повышение уровня биохимических маркеров некроза в крови.
Тип 4а. ИМ, связанный с процедурой ЧКВ.
Тип4б. ИМ, связанный с тромбозом коронарного стента, документированным при КАГ или патологоанатомическом исследовании.
Тип 5. ИМ, связанный с операцией КШ.
Приложение Г4. Причины повышения уровня сердечных тропонинов в крови.
Повреждение кардиомиоцитов, связанное с первичным (спонтанным) острым нарушением коронарного кровотока
- Разрыв атеросклеротической бляшки
- Образование тромба в просвете коронарной артерии
Повреждение кардиомиоцитов, связанное с ишемией миокарда, возникшей из-за повышения потребности миокарда в кислороде и/или уменьшения его доставки к миокарду
- Тахи- или брадиаритмии, блокада сердца.
- Расслоение аорты или тяжелый порок аортального клапана.
- Гипертрофическая кардиомиопатия.
- Кардиогенный, гиповолемический или септический шок.
- Тяжелая дыхательная недостаточность.
- Выраженная анемия.
- АГ
- Спазм коронарной артерии.
- Эмболия в коронарную артерию или васкулит.
- Дисфункция эндотелия коронарных артерий без существенного обструктивного коронарного атеросклероза.
Повреждение кардиомиоцитов, не связанное с ишемией миокарда
- Травма сердца (контузия, операция, абляция, ЭС, разряды дефибриллятора и пр.).
- Воспалительные заболевания (миокардит, вовлечение миокарда при эндокардите или перикардите).
- Кардитоксическое воздействие лекарств и токсинов.
Повреждение миокарда вследствие нескольких причин или неустановленной этиологии
- СН (острая и хроническая).
- Стрессорная кардиомиопатия (Такоцубо).
- Тяжелая ТЭЛА или ЛГ.
- Сепсис и крайне тяжелое состояние больного.
- Почечная недостаточность.
- Тяжелое острое неврологическое заболевание (например, инсульт, субарахноидальное кровоизлияние).
- Инфильтративное заболевание (амилоидоз, гемохроматоз, саркоидоз, склеродермия).
- Обширные ожоги.
- Очень интенсивная ФН.
Приложение Г5. Заболевания и состояния, затрудняющие ЭКГ диагностику ИМпST.
- Синдром ранней реполяризации желудочков сердца.
- Блокада ЛНПГ.
- Возбуждение желудочков сердца по дополнительному проводящему пути.
- ГЛЖ.
- Синдром Бругада.
- Перикардит, миокардит.
- ТЭЛА.
- Субарахноидальное кровоизлияние.
- Метаболические нарушения (например, гиперкалиемия).
- Кардиомиопатия.
- Холецистит.
- Сохраняющиеся изменения ЭКГ, свойственные молодому возрасту.
- Неправильное наложение электродов.
- ИМ в анамнезе с формированием патологических зубцов Q и/или сохраняющимся подъемом ST (например, хроническая аневризма ЛЖ).
- Ритм сердца, навязанный с помощью ЭС желудочков.
Приложение Г6. Оценка прогноза больного ИМпST в ранние сроки заболевания.
Таблица 1. Оценка риска смерти в стационаре по критериям группы TIMI
Фактор риска
Число баллов
Диагностика острого инфаркта миокарда
Инфаркт миокарда (ИМ) — одна из основных причин смертности работоспособного населения во всем мире. Главное предусловие летального исхода этой болезни связано с поздней диагностикой и отсутствием профилактических мероприятий у пациентов из группы риска. Своевременное установление диагноза подразумевает комплексную оценку общего состояния больного, результаты лабораторных и инструментальных методов исследования.
Опрос больного
Обращение пациента кардиологического профиля к врачу с жалобами на загрудинную боль всегда должны настораживать специалиста. Подробный расспрос с детализацией жалоб и течения патологии помогает установить направление диагностического поиска.
Основные моменты, которые указывают на возможность инфаркта у пациента:
- наличие ишемической болезни сердца (стабильная стенокардия, диффузный кардиосклероз, перенесенный ИМ);
- факторы риска: курение, ожирение, гипертоническая болезнь, атеросклероз, сахарный диабет;
- провоцирующие факторы: чрезмерная физическая нагрузка, инфекционное заболевание, психоэмоциональное напряжение;
- жалобы: загрудинная боль сдавливающего или жгущего характера, которая длится более 30 минут и не купируется «Нитроглицерином».
Кроме того, ряд пациентов отмечают за 2-3 дня до катастрофы «ауру» (подробнее о ней в статье «Предынфарктное состояние»):
- общая слабость, немотивированная усталость, обмороки, головокружение ;
- усиленное потоотделение;
- приступы сердцебиения.
Осмотр
Физикальное (общее) исследование пациента проводится в кабинете доктора с использованием методов перкуссии (поколачивания), пальпации и аускультации («выслушивания» сердечных тонов с помощью фонендоскопа).
Инфаркт миокарда — патология, которая не отличается специфическими клиническими признаками, позволяющими поставить диагноз без использования дополнительных методов. Физикальное исследование применяется для оценки состояния сердечно-сосудистой системы и определения степени нарушения гемодинамики (кровообращения) на догоспитальном этапе.
Частые клинические признаки инфаркта и его осложнений:
- бледность и высокая влажность кожных покровов;
- цианоз (синюшность) кожи и слизистых оболочек, холодные пальцы рук и ног — свидетельствуют о развитии острой сердечной недостаточности;
- расширение границ сердца (перкуторное явление) — говорит об аневризме (истончение и выпячивание стенки миокарда);
- прекардиальная пульсация характеризуется видимым биением сердца на передней грудной стенке;
- аускультативная картина — приглушенные тоны (из-за сниженной сократительной способности мышцы), систолический шум на верхушке (при развитии относительной недостаточности клапана при расширении полости пораженного желудочка);
- тахикардия (учащенное сердцебиение) и гипертензия (повышенные показатели артериального давления) вызываются активацией симпатоадреналовой системы.
Более редкие явления — брадикардия и гипотензия — характерны для инфаркта задней стенки.
Изменения в других органах регистрируются нечасто и связаны преимущественно с развитием острой недостаточности кровообращения. Например, отек легких, который аускультативно характеризуется влажными хрипами в нижних сегментах.
Изменение формулы крови и температура тела
Измерение температуры тела и развернутый анализ крови — общедоступные методы оценки состояния пациента для исключения острых воспалительных процессов.
В случае инфаркта миокарда возможно повышение температуры до 38,0 °С на 1—2 дня, состояние сохраняется в течение 4—5 суток. Однако гипертермия встречается при крупноочаговом некрозе мышцы с выделением медиаторов воспаления. Для мелкоочаговых инфарктов повышенная температура нехарактерна.
Наиболее характерные изменения в развернутом анализе крови при ИМ:
- лейкоцитоз — повышение уровня белых клеток крови до 12—15*10 9 /л (норма — 4—9*10 9 /л);
- палочкоядерный сдвиг влево: увеличение количества палочек (в норме — до 6 %), юных форм и нейтрофилов;
- анэозинофилия — отсутствие эозинофилов (норма — 0—5 %);
- скорость оседания эритроцитов (СОЭ) возрастает до 20—25 мм/час к концу первой недели (норма — 6—12 мм/час).
Сочетание перечисленных признаков с высоким лейкоцитозом (до 20*10 9 /л и больше) свидетельствуют о неблагоприятном прогнозе для пациента.
Коронарография
Согласно современным стандартам, пациент с подозрением на инфаркт миокарда подлежит экстренному выполнению коронарографии (введение контраста в сосудистое русло и с последующим рентгеновским исследованием проходимости сосудов сердца). Подробнее об этом обследовании и особенностях его выполнения можно прочесть тут.
Электрокардиография
Электрокардиография (ЭКГ) по-прежнему считается основным методом диагностики острого инфаркта миокарда.
Метод ЭКГ позволяет не только поставить диагноз ИМ, но и установить стадию процесса (острая, подострая или рубец) и локализацию повреждений.
Международные рекомендации Европейского общества кардиологов выделяют следующие критерии инфаркта миокарда на пленке:
- Острый инфаркт миокарда (при отсутствии гипертрофии левого желудочка и блокады левой ножки пучка Гисса):
- Повышение (подъем) сегмента ST выше изолинии: >1 мм (>0,1 мВ) в двух и более отведениях. Для V2-V3 критерии >2 мм (0,2 мВ) у мужчин и >1,5 мм (0,15 мВ) у женщин.
- Депрессия сегмента ST >0,05 мВ в двух и более отведениях.
- Инверсия («переворот» относительно изолинии) зубца Т более 0,1 мВ в двух последовательных отведениях.
- Выпуклый R и соотношение R:S>1.
- Ранее перенесенный ИМ:
- Зубец Q длительностью более 0,02 с в отведениях V2-V3; более 0,03 с и 0,1мВ в I, II, aVL, aVF, V4-V6.
- Комплекс QS в V2-V
- R >0,04 c в V1-V2, соотношение R:S>1 и положительный зубец Т в этих отведениях без признаков нарушения ритма.
Определение локализации нарушений по ЭКГ представлено в таблице ниже.
| Пораженный участок | Отвечающие отведения |
|---|---|
| Передняя стенка левого желудочка | I, II, aVL |
| Задняя стенка («нижний», «диафрагмальный инфаркт») | II, III, aVF |
| Межжелудочковая перегородка | V1-V2 |
| Верхушка сердца | V3 |
| Боковая стенка левого желудочка | V4-V6 |
Аритмический вариант инфаркта протекает без характерной загрудинной боли, но с нарушениями ритма, которые регистрируются на ЭКГ.
Биохимические анализы на маркеры некроза сердечной мышцы
«Золотым стандартом» подтверждения диагноза ИМ в первые часы от начала приступа боли является определение биохимических маркеров.
Лабораторная диагностика инфаркта миокарда с помощью ферментов включает:
- тропонины (фракции І, Т и С) — белки, которые находятся внутри волокон кардиомиоцитов и попадают в кровь при разрушении миокарда (о том, как выполнить тест, читайте здесь;
- креатинфосфокиназа, сердечная фракция (КФК-МВ);
- белок, связывающий жирные кислоты (БСЖК).
Также лаборанты определяют менее специфические показатели: аспартатаминотрансфераза (АСТ, является также маркером поражения печени) и лактатдегидрогеназа (ЛДГ1-2).
Время появления и динамика концентрации сердечных маркеров представлены в таблице ниже.
Согласно приведенным выше данным, для диагностики рецидива инфаркта (в первые 28 дней) целесообразно определять КФК-МВ или БСЖК, концентрация которых снижается в течение 1—2 дней после приступа.
Забор крови на сердечные маркеры проводится в зависимости от времени начала приступа и специфики изменения концентраций ферментов: не стоит ожидать высоких значений КФК-МВ в первые 2 часа.
Неотложная помощь пациентам оказывается вне зависимости от результатов лабораторной диагностики, на основании клинических и электрокардиографических данных.
Рентгенография органов грудной клетки
Рентгенологические методы нечасто используются в практике кардиологов для диагностики инфаркта миокарда.
Согласно протоколам, рентгенография органов грудной клетки показана при:
- подозрении на отек легких (одышка и влажные хрипы в нижних отделах);
- острой аневризме сердца (расширение границ сердечной тупости, перикардиальная пульсация).
УЗИ сердца (эхокардиография)
Комплексная диагностика острого инфаркта миокарда подразумевает раннее ультразвуковое исследование сердечной мышцы. Метод эхокардиографии (ЭхоКГ) информативен уже в первые сутки, когда определяются:
- снижение сократительной способности миокарда (зоны гипокинезии), что позволяет установить топический (по локализации) диагноз;
- падение фракции выброса (ФВ) — относительный объем, который попадает в систему кровообращения при одном сокращении;
- острая аневризма сердца — расширение полости с формированием кровяного сгустка в нефункционирующих участках.
Кроме того, метод используется для выявления осложнений ИМ: клапанной регургитрации (недостаточности), перикардита, наличия тромбов в камерах.
Радиоизотопные методы
Диагностика инфаркта миокарда при наличии сомнительной ЭКГ-картины (например, при блокаде левой ножки пучка Гисса, пароксизмальных аритмиях) подразумевает использование радионуклидных методов.
Наиболее распространенный вариант — сцинтиграфия с использованием пирофосфата технеция (99mTc), который накапливается в некротизированных участках миокарда. При сканировании такой области зона инфаркта обретает наиболее интенсивный окрас. Исследование информативно с 12 часов после начала болевого приступа и до 14 дней.

Изображение сцинтиграфии миокарда
МРТ и мультиспиральная компьютерная томография
КТ и МРТ в диагностике инфаркта используются сравнительно редко из-за технической сложности исследования и невысокой информативности.
Компьютерная томография наиболее показательна для дифференциальной диагностики ИМ с тромбоэмболией легочной артерии, расслоения аневризмы грудной аорты и других патологий сердца и магистральных сосудов.
Магнитно-резонансная томография сердца отличается высокой безопасностью и информативностью в определении этиологии поражения миокарда: ишемическое (при инфаркте), воспалительное или травматическое. Однако длительность процедуры и особенности проведения (необходимо неподвижное состояние пациента) не позволяют проводить МРТ в острый период ИМ.
Дифференциальная диагностика
Наиболее опасные для жизни патологии, которые необходимо отличать от ИМ, их признаки и используемые исследования представлены в таблице ниже.
- внезапная боль за грудиной;
- одышка;
- цианоз шеи, лица и верхней половины туловища;
- кровохарканье;
- тахикардия (учащенное сердцебиение)
- коагулограмма (повышение свертываемости крови);
- увеличение концентрации D-димера (более 0,5 нм/л)
- рентгенография органов грудной клетки (дискообразные ателектазы, расширение корня легкого и конуса верхней полой вены);
- ЭКГ: глубокие Q в V3 и S в V1, высокий Т в V3;
- КТ органов грудной полости: ателектаз пораженного сегмента;
- ЭхоКГ: визуализация тромба в просвете легочного ствола;
- ангиопульмонография (рентгенологический метод с внутрисосудистым введением контраста) — «блок» участка
- сильная боль в груди с иррадиацией в спину, шею и плечо;
- головная боль, отек лица (из-за сдавливания верхней полой вены);
- одышка;
- охриплость голоса;
- синдром Бернара-Горнера: птоз, миоз, энофтальм (опущенные веки, суженные зрачки, глубоко посаженные глаза)
- рентгенография органов грудной клетки: расширение тени средостения;
- на УЗИ и КТ: два контура и два просвета аорты;
- ангиография — двойной контур расслаивающей аневризмы;
- ЭхоКГ — недостаточность аортального клапана, расширение устья сосуда
- кашель;
- одышка;
- высокая температура тела;
- боли в груди, которые усиливаются на вдохе
- рентгенография органов грудной клетки: участки затемнения с вовлечением в процесс плевры;
- КТ-симптомы «матового стекла» и «дерева в почках»
Для подготовки материала использовались следующие источники информации.
Инфаркт миокарда и нестабильная стенокардия

Инфаркт миокарда – неотложное заболевание сердца, которое чаще всего вызывается внезапной закупоркой коронарной артерии тромбом. Подозрение на инфаркт миокарда кардиологи называют — острым коронарным синдромом (ОКС). По данным электрокардиографии (ЭКГ) выделяют ОКС с повреждением сердечной мышцы, либо начальная фаза без гибели сердечной мышцы, которая называется нестабильной стенокардией. Восстановление кровообращения в коронарной артерии при инфаркте миокарда в течение ближайших 6 часов устраняет последствия и такой подход очень эффективен, потому что даёт надежду на полное выздоровление. Первые признаки инфаркта миокарда должны стать поводом для экстренной госпитализации в специализированный центр.
Подход к лечению в Инновационном сосудистом центре
Современная технология лечения ОКС и нестабильной стенокардии подразумевает коронарографию, ангиопластику и стентирование поражённой артерии. Эта тактика с успехом применяется у нас в клинике. В нашей клинике есть чёткое понимание того, что спасение жизни при инфаркте зависит от времени, когда было восстановлено коронарное кровоснабжение. Поэтому принимая машины скорой помощи, мы организуем экспресс-диагностику и подготовку больного к коронарографии в течение 5 минут. Среднее время восстановления коронарного кровотока после поступления больного в клинику составляет менее 20 минут. Отличительные особенности, подготовка наших специалистов и организация работы клиники позволяет сохранять очень низкий уровень летальности при инфаркте миокарда.
Причины инфаркта миокарда
Сердце требует своего постоянного снабжения кислородом и питательными веществами, как и любая мышца в организме. Для обеспечения этой потребности необходима хорошая проходимость двух крупных артерий и их ветвей, которые доставляют обогащённую кислородом кровь к сердечной мышце. Это система правой и левой коронарных артерий. Если одна из этих артерий или ветвей внезапно блокируются, то часть сердца испытывает недостаток кислорода. Это состояние называется «ишемией миокарда». Если ишемия продолжается долго, то может возникнуть гибель мышечной ткани сердца. Это сердечный приступ, известный как инфаркт миокарда — буквально «смерть сердечной мышцы».
Атеросклероз коронарных артерий (ишемическая болезнь сердца) является фоновым состоянием для большинства инфарктов миокарда . Непосредственной причиной возникновения инфаркта миокарда обычно бывает тромб, образующийся в суженом участке сосуда и полностью перекрывающий кровоток.
Инфаркт миокарда — классификация причин :
Тип 1 – спонтанный, вследствие первичного коронарного события, такого как разрыв, растрескивание или расслоение атеросклеротической бляшки
Тип 2 – инфаркт развивается вследствие уменьшения кровообращения сердца вследствие вторичных причин, таких как спазм коронарной артерии, коронарной эмболия, анемия, аритмия, гипертензия или гипотензия.
Тип 3 – внезапная неожиданная сердечная смерть, включая остановку сердца, часто с симптомами ишемии миокарда. Только патологоанатом может ответить на вопрос, как и отчего происходит развитие массивного инфаркта миокарда при внезапной смерти.
Тип 4 – связанный с коронарной ангиопластикой или стентированием:
Тип 4а – развитие инфаркта миокарда вследствие чрескожного коронарного вмешательства.
Тип 4б – инфаркт, связанный с тромбозом стента.
Тип 5 – развитие инфаркта миокарда, связанного с аортокоронарным шунтированием.
Клинические синдромы при инфаркте
- Сердечная недостаточность, когда сердце не справляется с перекачиванием необходимого объёма крови из гибели части мышечных клеток.
- Аритмии или другие нарушения сердечного ритма из-за гибели проводящих путей.
- Внезапная сердечная смерть, когда сердце перестаёт биться из-за блокады проводящих путей.
- Кардиогенный шок — рефлекторная реакция организма с низким артериальным давлением, которая может привести к повреждению почек, печени и головного мозга.
Атипичные формы инфаркта
Помимо характерной для инфаркта сдавливающей боли за грудиной, выделяют ещё несколько форм инфаркта, которые могут напоминать другие заболевания или протекать бессимптомно. К ним относятся:
- Гастритический инфаркт. Начинается болью в верхней половине живота похожей на обострение гастрита. Нередко при ощупывании живота, отмечается болезненность и напряжённость мышц передней брюшной стенки. Иногда симптоматика напоминает прободную язву.
- Астматический инфаркт. Симптоматика напоминает приступ бронхиальной астмы. Она проявляется надсадным сухим кашлем, чувством заложенности в груди, одышкой. Бывает при поражении передней стенки левого желудочка.
- Безболевой вариант инфаркта, который может проявиться ощущением неопределённого дискомфорта в грудной клетке, потоотделением и общей слабостью.
Классификация инфаркта
По ЭКГ обычно выделяют на два варианта: с подъёмом сегмента ST (ЅТEMI) и без подъёма сегмента ST (NSTEMI). Подъём сегмента ST на электрокардиограмме и последующим изменением специфических лабораторных показателей свидетельствует о формировании очага гибели сердечной мышцы. Термин «Острый коронарный синдром» часто используется для определения тактики первичной врачебной помощи и включает в себя все варианты острого нарушения коронарного кровообращения.
Осложнения
Осложнения инфаркта связаны с повреждением участков сердца, проводящих путей, тромбозами полостей сердца. Развитие инфаркта значит гибель того или иного структурного элемента сердца.
Примерно у 90% больных отмечаются различные формы нарушений сердечного ритма (аритмии) во время или сразу после события. У 25% пациентов, нарушение ритма проявляются в течение первых 24 часов. В этой группе больных риск серьёзных аритмий, таких как фибрилляция желудочков, является наибольшим в течение первого часа, а затем постепенно сокращается. Врач должен правильно оценивать эти аритмии, так как некоторые из них могут привести к остановке сердца, поэтому необходим постоянный мониторинг ЭКГ у больных с ишемией миокарда.
- Повреждения миокарда и структуры сердца.
Гибель ткани сердца вследствие прекращения кровоснабжения может привести к распаду этой ткани и повреждению структуры сердца. Чаще всего наблюдаются 3 основных механических осложнений инфаркта:
- Спонтанный разрыв стенки желудочка.
- Разрыв межжелудочковой перегородки значит, что развивается нарушение внутрисердечных потоков крови и гемодинамики.
- Отрыв сосочковой мышцы разрыв с развитием впоследствии тяжёлой недостаточности митрального клапана.
- Постинфарктные аневризмы левого желудочка.
Аневризма левого желудочка это локализованный участок миокарда с аномальными выпячиванием и деформацией во время систолы и диастолы, который появляется вследствие замещения миокарда рубцовой тканью. Аневризма опасна скоплением тромботических масс в её просвете с последующей эмболией (переносом) их с током крови в другие органы. При аневризме увеличивается объём левого желудочка, а значит проявляется его относительная функциональная недостаточность.
- Тромботические осложнения
При инфаркте в левом желудочке нередко возникает пристеночный тромб, особенно часто он развивается после инфарктов, произошедших в области передней стенки левого желудочка. Частота этого осложнения при инфаркте составляет 20-60 %, что приводит к высокому риску отрыва и переноса тромба с током крови (эмболии). Антикоагулянтная терапия может существенно уменьшить риск развития тромбоза и эмболии.
Клинические синдромы, связанные с повреждением миокарда после инфаркта
- Перикардит
Воспаление околосердечной сумки (перикарда) наблюдается примерно у 10% пациентов после перенесённого инфаркта со значительным повреждением миокарда. Перикардит обычно лечится противовоспалительными препаратами или при большом скоплении жидкости может проводится пункция перикарда для облегчения состояния пациента.
- Постинфарктный аутоиммунный синдром (синдром Дресслера)
До эпохи тромболизиса и коронарной ангиопластики этот синдром возникал у 5 % больных после сердечного приступа. С внедрением реперфузии развитие синдрома Дресслера происходит реже. Отличительные клинические признаки включают лихорадку, боль в груди и симптомы перикардита возникают через 2-3 недели после лечения инфаркта миокарда . Лечение включает в себя противовоспалительные препараты и гормоны. Клинические проявления синдрома обуславливают значимую сердечную недостаточность, развивающуюся после инфаркта.
Прогноз
Острый инфаркт миокарда приводит в результате к 30% смертности, а половина смертей происходят до прибытия в больницу. В течение первого года после острого сердечного приступа умирают 5-10% выживших. Приблизительно половина всех пациентов подвергаются повторной госпитализации в течение 1 года после предыдущего события. Большое значение для прогноза имеет объём поражённой ткани миокарда. Он сильно варьирует и во многом зависит от степени инфаркта, остаточной функции левого желудочка, и будет ли проведено восстановление кровообращения в миокарде.
Лучший прогноз связан со следующими факторами:
- Успешная ранняя реперфузия (с подъёмом сегмента ST с помощью тромболизиса или чрескожное коронарное вмешательство (ангиопластика и стентирование) в течение 90 минут.
- Сохранилась функция левого желудочка в результате быстрого восстановления кровоснабжения миокарда.
- Адекватная терапия с бета-адреноблокаторами, аспирином, клопидогрелем и ингибиторами АПФ в остром периоде.
Неблагоприятный прогноз связан со следующими факторами:
- Преклонный возраст
- Сахарный диабет
- Поражения в других бассейнах (сонные и периферические артерии)
- Задержка или неудачное коронарное вмешательство.
- Плохо сохранилась функция левого желудочка
Лечение проводится в клиниках:
Преимущества лечения в клинике
Безотлагательная помощь при инфаркте
Лучшие стенты с лекарственными покрытиями
Лечение по полису ОМС
Диагностика
 Симптомы инфаркта миокарда
Симптомы инфаркта миокарда
Стенокардия (пациент испытывает сжимающие боли за грудиной): самый первый признак поражения коронарных артерий и симптом грядущего инфаркта миокарда. Большинство пациентов отмечают предшествующие приступы стенокардии, которая даёт аналогичную боль в груди. Разница в основном в продолжительности болевого синдрома: при стенокардии кровообращение восстанавливается, боль отступает в течение нескольких минут, а миокард не повреждается.
При инфаркте поток крови критически снижен или полностью заблокирован, боль длится дольше и сердечная мышца может погибнуть в ближайшие часы. Затянувшийся приступ стенокардии должен заставить срочно вызвать скорую помощь! Около 25% всех инфарктов происходит без предшествующей стенокардии, но могут сопровождаться снижением давления и появлением одышки.
Для выявления проблем с кровообращением миокарда необходимо выполнить электрокардиографию (ЭКГ). Так как инфаркт — это гибель участков ткани сердца и его проводящих путей, то развиваются нарушения его функции.
Основные симптомы инфаркта миокарда связаны с болью и острой сердечной недостаточностью :
- Боль в груди, чувство наполнения и/или сдавливания в груди.
- Боль в челюсти, зубная, головная боль.
- Нехватка дыхания, которую больной чувствует из-за отёка лёгких.
- Тошнота, рвота, общее ощущение давления под ложечкой (вверху в центре живота).
- Потливость, одышка .
- Изжога и/или расстройство пищеварения, кишечника.
- Боль в руке (наиболее часто в левой, но может и в правой руке).
- Боль в верхней части спины, которую пациент испытывает при заднем инфаркте.
- Общее болезненное ощущение (неясное ощущение недомогания) и нарушения сердцебиения.
Диагностика инфаркта складывается из методов определения характера инфаркта и формы повреждения миокарда и определения причин этого повреждения. Для диагностики используются следующие методы:
- Электрокардиограмма (ЭКГ).
Электрическая активность сердца регистрируется с помощью электродов, прикреплённых к коже. Определённые отклонения в электрической активности сердца могут помочь специалистам определить зоны ишемии миокарда и уточнить диагноз.
Это ультразвуковое исследование сердца. Она позволяет выявить зоны нефункционирующего миокарда при его гибели и в результате определить функциональный резерв сердца — фракцию выброса.
Контрастное вещество вводится в кровеносные сосуды сердца. Затем рентгеновский аппарат делает серию снимков (ангиография), показывая проходимость этих коронарных артерий. Это исследование позволяет определить причину ишемии миокарда и принять меры для нормализации кровотока по коронарным артериям.
- Лабораторная диагностика.
Наиболее чувствительным и специфичным маркёром гибели клеток миокарда является повышение концентрации тропонинов I и Т. В норме эти тропонины в крови не определяются. Возникновение некроза кардиомиоцитов сопровождается сравнительно быстрым и значительным увеличением концентрации тропонинов I и Т уже через 2–6 ч после сердечного приступа.
- Консультация кардиолога
- Коронарография
- Электрокардиография
- Эхокардиография
Лечение

Лечение ишемии миокарда предполагает улучшение притока крови к сердечной мышце. Консервативная терапия инфаркта миокарда малоэффективна, чтобы открыть заблокированные коронарные артерии может быть использован внутривенный тромболизис.
Своевременное эндоваскулярное вмешательство — коронарная ангиопластика и стентирование восстанавливают проходимость коронарных сосудов и предотвращают развитие инфаркта, снижая летальность при ОКС до 2% с 40% при обычном лечении. Улучшение непосредственных и отдалённых исходов является отличительной чертой эндоваскулярных вмешательств по сравнению с консервативной терапией.
Большинство инфарктов развивается в течение нескольких часов, поэтому не стоит ждать, чтобы появились все признаки и последствия сердечного приступа. Чаще всего сердечный приступ сопровождается болью в грудной клетке, которая не проходит после приёма нитроглицерина, однако бывают и безболевые формы, особенно у больных с сахарным диабетом. Инфаркт требует немедленной медицинской помощи. Для того чтобы максимально сохранить жизнеспособную сердечную мышцу и предотвратить дальнейшее ухудшение пациенту надо дать аспирин и нитроглицерин.
Если через 15 минут после нитроглицерина и получаса после возникновения боль в грудной клетке не отступила, то необходимо срочно вызывать скорую помощь. В зависимости от вида инфаркта проводятся различные лечебные мероприятия.
- Лечение инфаркта миокарда с подъёмом ЅТ (STEMI)
Основное лечение для инфаркта с подъёмом сегмента ST может включать тромболизис или чрескожное коронарное вмешательство (ЧКВ). Первичное чрескожное коронарное вмешательство является методом выбора для лечения инфаркта с подъёмом ЅТ, если оно может быть выполнено своевременно. Если ЧКВ не может быть выполнено в течение 90 до 120 минут, то с целью оказания первой помощи рекомендуется проведение тромболизиса. Если пациент имеет симптомы инфаркта в течение от 12 до 24 часов, то показаний для тромболизиса меньше, позже тромболизис не рекомендуется.
ЧКВ — главный метод лечения острого инфаркта миокарда, позволяющий восстановить кровоток в инфаркт-связанной артерии. Чем раньше будет проведена ангиопластика и стентирование закрытой коронарной артерии, тем больше шансов на благоприятный исход.
- Инфаркт миокарда без подъёма сегмента ST
При отсутствии подъёма сегмента ST, диагноз уточняется с помощью анализа крови на тропонин. Положительный тест на тропонин может появиться через 3-6 часов после развития острого коронарного синдрома и свидетельствует о том, что имеется очаг некроза миокарда. Такой инфаркт называется «острый коронарный синдром без подъёма сегмента ST (NSTEMI). В этом случае у врача есть время, чтобы специалисты провели дополнительные обследования больного, которые определят необходимость вмешательства на коронарных артериях. Если принято решение о необходимости реваскуляризации, то коронарография проводится в ближайшие часы после поступления пациента. Если принято решение о консервативном лечении, то применяются дезагреганты (клопидогрель, тромбо асс) и патогенетическая лекарственная терапия, отказ от вредных привычек, изменение образа жизни и режима физической активности.
Источник https://library.mededtech.ru/rest/documents/cr_135/
Источник https://cardiograf.com/diagnostika/shemy/diagnostika-infarkta-miokarda.html
Источник https://angioclinic.ru/zabolevaniya/infarkt-miokarda/