Руководство по обследованию и лечению гирсутизма у женщин в предклимактерическом периоде (Journal of Clinical Endocrinology & Metabolism, март 2018)

В журнале Journal of Clinical Endocrinology & Metabolism 07 марта 2018 г. Endocrine Society опубликовала руководство по обследованию и лечению гирсутизма у женщин в предклимактерическом периоде.
1.0. Диагностика гирсутизма.
1.1 Рекомендуется тестирование на предмет повышенного уровня андрогенов у всех женщин с патологическим результатом по шкале гирсутизма. В случаях, когда результат уровня общего сывороточного тестостерона нормален и имеется умеренный-выраженный рост волос половой зоны, либо рост волос половой зоны незначителен, но имеются клинические данные гиперандрогенного эндокринного расстройства (таких как менструальные нарушения или прогрессирование несмотря на лечение), то рекомендуется измерение утреннего общего и свободного тестостерона специальными методами тестирования.
1.2. Рекомендуется проведение скрининга у женщин с гиперандрогенемией на предмет неклассической формы врожденной гиперплазии коры надпочечников (НВГКН) вследствие недостаточности 21-гидроксилазы путем измерения утреннего уровня 17-Гидроксипрогестерона в фолликулярную фазу, либо в произвольный день у женщин с аменореей или нечастыми месячными. У пациенток с повышенным оволосением с высоким риском врожденной гиперплазии коры надпочечников (положительный семейный анамнез, представители этнических групп с высоким риском), рекомендуется проведение данного скрининга даже если имеется нормальный результат сывороточного общего и свободного тестостерона.
1.3. Не рекомендуется проведение тестирования на наличие повышенного уровня андрогена у женщин с нормальным менструальным циклом (эуменорея) с нежелательным местным ростом волос (например при отсутствии патологического результата по шкале гирсутизма) ввиду низкой вероятности выявления медицинской патологии, которая сможет повлиять на лечение или исходы.
2.0. Лечение гирсутизма у женщин в предклимактерическом периоде.
2.1. Для большинства женщин со значимым для них гирсутизмом несмотря на косметологические меры, рекомендуется фармакологическое лечение. Для тех женщин, которые в последующем изъявляют желание дополнительного косметологического эффекта, рекомендуется добавление методов прямого удаления волос. Однако, для женщин с легким гирсутизмом и без данных за наличие эндокринного заболевания, рекомендуется любой из этих подходов.
2.2. Для женщин с гирсутизмом и с ожирением, включая с синдромом поликистоза яичников, также рекомендуется изменение образа жизни.
3.0. Фармакологическое лечение.
Изначальное лечение:
3.1. Для большинства женщин с гирсутизмом, которые не планируют беременность, рекомендуются пер-оральные контрацептивы как исходная терапия для лечения значимого для пациентки гирсутизма.
3.2. Для большинства женщин с гирсутизмом не рекомендуется изначальная анти-андрогенная монотерапия (ввиду потенциального тератогенного эффекта данных препаратов), только если женщина не применяет адекватную контрацепцию. Однако, для женщин, не ведущих активную половую жизнь, для женщин, которые прошли окончательную стерилизацию, либо применяют долгосрочную обратимую контрацепцию, рекомендуется применение либо пер-оральных контрацептивов, либо анти-андрогенных препаратов для исходной терапии. Выбор между данными двумя методами зависит от предпочтений пациентки в эффективности, побочных эффектах и стоимости препаратов.
3.3. Для большинства женщин не отдается предпочтений какому либо пер-оральному контрацептиву над другим при исходном лечении, так как все пер-оральные контрацептивы имеют равную эффективность при гирсутизме, и риск побочных эффектов низок.
3.4. Для женщин с гирсутизмом с более высоким риском венозной тромбоэмболии (например с ожирением, либо старше 39 лет) рекомендуется изначальное лечение пер-оральным контрацептивом, содержащим наименьшую эффективную дозу этинилэстрадиола (обычно 20 микрограмм) и прогестин низкого риска (смотрите Таблицу 2 в статье).
3.5. Если значимый для пациентки гирсутизм сохраняется несмотря на монотерапию пер-оральным контрацептивом в течение 6 месяцев, рекомендуется добавление анти-андрогена.
3.6. Не отдается предпочтений какому либо анти-андрогену над другим. Однако, не рекомендуется применение Флутамида ввиду потенциальной гепатотоксичности.
3.7. Для всех фармакологических препаратов от гирсутизма рекомендуется пробное лечение в течение как минимум 6 месяцев до принятия решения по изменении дозы, смены на другой препарат, либо принятия решения по добавлению другого препарата.
3.8. У пациенток с тяжелым гирсутизмом с эмоциональным стрессом, и/или у женщин, которые уже применяли пер-оральные контрацептивы и не отметили достаточного улучшения, рекомендуется назначение комбинированного лечения с пер-оральным контрацептивом и анти-андрогеном. Однако, не рекомендуется применение комбинированного лечения как стандартное лечение первой линии.
Другие виды лекарственной терапии:
3.9. Не рекомендуется применение препаратов, снижающих инсулин, для исключительно лечения гирсутизма.
3.10. Не рекомендуется применение агонистов гонадотропин-рилизинг-гормона, кроме женщин с тяжелой формой гиперандрогенемии (таких как гипертекоз яичников) с неоптимальным ответом на пер-оральные контрацептивы и анти-андрогены.
3.11. Не рекомендуется применение местных анти-андрогенных препаратов для лечения гирсутизма.
4.0. Методы прямого удаления волос.
4.1. Для женщин, выбравших лечение путем удаления волос, рекомендуется фотоэпиляция нежелательных волос тёмно-рыжего, коричневого и черного цвета, и рекомендуется электролиз седых волос и у блондинок.
4.2. Для женщин не-европеоидной этнической принадлежности, выбравших фотоэпиляцию, рекомендуется применение длинно-волнового, долго-импульсного источника света, такого как Nd:YAG лазер или диодный лазер с надлежащим охлаждением кожи. Врачу необходимо предупреждать средиземноморских женщин и женщин с Ближнего Востока с лицевым гирсутизмом об повышенном риске развития парадоксального гипертрихоза от фотоэпиляции. Рекомендуется местное лечение или электролиз у данной категории женщин.
4.3. Для женщин, желающих более быстрый ответ на фотоэпиляцию, рекомендуется добавлять крем Эфлорнитин для местного применения во время лечения.
4.4. У женщин с гиперандрогенемией, выбравших лечение путем удаления волос, рекомендуется назначение фармакологического лечения для снижения повторного роста волос.
Подробнее смотрите в прикрепленном файле .
Посмотреть другие обзоры
Автор обзора
Автор обзоров мировой медицинской периодики на портале MedElement — врач общей практики, хирург Талант Иманалиевич Кадыров.
Закончил Киргизский Государственный медицинский институт (красный диплом), в совершенстве владеет английским языком. Имеет опыт работы хирургом в Чуйской областной больнице; в настоящий момент ведет частную практику.
Регулярное повышение квалификации: курсы Advanced Cardiac Life Support, International Trauma Life Support, Family Practice Review and Update Course (Англия, США, Канада).
Прикреплённые файлы
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement и в мобильных приложениях «MedElement (МедЭлемент)», «Lekar Pro», «Dariger Pro», «Заболевания: справочник терапевта», не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement и мобильные приложения «MedElement (МедЭлемент)», «Lekar Pro», «Dariger Pro», «Заболевания: справочник терапевта» являются исключительно информационно-справочными ресурсами. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.
Гирсутизм у девочек и подростков

В статье представлены современные данные о физиологии формирования и роста волос. Освещены механизмы андрогенной регуляции кожи и волосяного покрова в норме и при патологии, вызывающей гирсутизм у девочек и подростков. Приводятся особенности клинической к
2017-03-13 11:25
88494 прочтения
Hirsutism in girls and adolescents
The article presents modern data on the physiology of the formation and growth of hair. We covered the mechanisms of androgen regulation of skin and hair in normal and pathological conditions, causing hirsutism in girls and adolescents. We give characteristics of clinical picture, diagnostic methods and treatment approaches.
Под гирсутизмом понимают чрезмерный рост волос у лиц женского пола по мужскому типу, т. е. появление терминальных волос на верхней губе, подбородке, в области грудины, верхней части спины, срединной линии живота, на крестце, ягодицах, внутренней поверхности бедер. Гирсутизм является не только косметической проблемой, но и нередко симптомом серьезных заболеваний.
Физиология оволосения
На теле человека около 50 миллионов волосяных фолликулов и только малая часть (100–150 тыс.) расположены на волосистой части головы. Свободны от волос только ладони, стопы, губы. Основная часть волосяных фолликулов формируется из экто- и мезодермы в пренатальном периоде. Эти элементы тесно контактируют в течение всей жизни волосяного фолликула.
Первые волосы появляются у человека в конце 3-го месяца внутриутробной жизни, а на 7-м месяце — пушковые волосы (лануго), которые покрывают все части тела за исключением ладоней, подошв, грудных сосков. Лануго — это мягкие, нежные, тонкие волосы, не имеющие мозгового вещества, около 2 мм в длину, умеренно пигментированы. По мере развития плода количество их уменьшается, а к четвертому месяцу жизни ребенка они полностью выпадают.
Перед рождением они меняются на детский волосяной покров. Терминальный волосяной покров образуется к началу полового созревания — это густые волосы на лобке и подмышечных впадинах, а у мужчин на лице, животе, конечностях.
Рост волос во многом связан с полом. У мужчин волос больше и растут они быстрее. Это вызвано наличием в их организме большой концентрации андрогенов. С увеличением этого гормона больше появляется волос на теле.
Выделяют три фазы роста волоса. Активная фаза — анаген, за которой следует фаза инволюции (катаген), в которой волосы перестают расти, а волосяная луковица уменьшается в размере, и, наконец, фаза телогена, в которой старый волос сменяется на новый. Продолжительность катагена и телогена составляет в среднем от 2–3 недель до 3–4 месяцев соответственно. Соотношение числа волос в фазе анагена к телогену используется для определения активности роста волос, более высокое соотношение указывает на активный рост. Частота и расположение волосяных луковиц в коже является индивидуальной особенностью организма [1].
Каждый волос состоит из стержня и корня. Весь корень волоса заключен в волосяном мешочке — фолликуле. Клетки сосочкового слоя дермы андрогензависимых областей имеют большое количество андрогеновых рецепторов по сравнению с другими областями кожи.
Все андрогены являются С19-стероидами, производными андростана, и имеют разную биологическую активность. Основными источниками продукции андрогенов в женском организме являются тека-клетки яичников, сетчатый слой коры надпочечников, периферическая конвертация из предшественников стероидных гормонов (андростендион, дегидроэпиандростерон (ДГЭА)) в печени, мышцах, коже и жировой ткани.
В циркуляции наряду с тестостероном определяются 5-андростендион, 4-андростендион, андростерон и ДГЭА, обладающие незначительной биологической активностью. Они являются предшественниками или продуктами метаболизма тестостерона.
В клетках-мишенях (коже, мышцах, жировой ткани) тестостерон подвергается воздействию тканевого фермента 5α-редуктазы, превращаясь в 5α-дигидротестостерон (ДГТ), обладающий максимальной андрогеновой активностью. Свободные фракции тестостерона обладают большей биологической активностью. Проникая в клетку-мишень, они связываются с ядерным рецептором. В физиологических условиях андрогены выполняют роль анаболических факторов [2].
Половые гормоны, главным образом андрогены, переносятся специфическим белком — сексстероидсвязывающим глобулином (СССГ). В свободном состоянии циркулирует 1–3% андрогенов, которые оказывают биологическое действие на клетки. Уровень его снижается под влиянием андрогенов, глюкокортикоидов, соматотропного гормона, тиреоидных гормонов, избытка массы тела.
Инактивация половых стероидов происходит в основном в печени за счет процессов конъюгирования с глюкоуроновой кислотой и сульфирования. Концентрация стероидов в крови обусловлена взаимодействием активности биосинтеза и деградации.
Половое оволосение зависит от уровня андрогенов. До периода полового созревания волосы нежные (небольшой длины, прямые, светлые), сальные железы кожи мало активны. В ответ на повышение уровня андрогенов в период полового созревания в гормонозависимых областях детские волосы трансформируются в жесткие терминальные (более темные, завитые). Высокий уровень андрогенов необходим для роста волос в подмышечной и лобковых областях. На других участках кожи, таких как лоб, например, этот же уровень андрогенов увеличивает активность сальных желез, но не вызывает дифференцировки пушковых волос. Причины этого в настоящее время не до конца ясны [3].
На периферии активность 5α-редуктазы увеличивается под действием местных факторов роста и циркулирующих андрогенов. В организме дигидротестостерон стимулирует: выработку кожного сала, дифференцировку волосяного фолликула из пушкового волоса в осевой, продлевает фазу анагена. В результате чего волосы утолщаются.
Этническое происхождение значительно влияет на рост терминальных волос на теле. Считается, что различия между уровнем оволосения у людей связаны с чувствительностью фолликула волоса к ферменту 5α-редуктазы, а также с полиморфизмом андрогеновых рецепторов. У северных народов наименьшее количество терминальных волос, в то время как в Южной Европе и у темнокожих средиземноморских женщин их много.
Патогенез гирсутизма
Гирсутизм — это результат дисбаланса между уровнем гормонов и чувствительностью волосяных фолликулов к андрогенам. Он является важным симптомом андрогензависимой дерматопатии. Выраженность этого признака зависит от многих факторов: этнической принадлежности женщины, длительности и глубины патологического процесса, спектра и уровня секретированных андрогенов, дающих различный вирилизирующий эффект.
В популяции большинство девушек, у которых уровень андрогенов в крови в 2 раза выше средней нормы, имеют умеренную степень гирсутизма. Тем не менее тяжесть гирсутизма не всегда коррелирует с уровнем андрогенов, так как чувствительность к андрогенам значительно варьирует у разных людей. У некоторых женщин с синдромом гиперандрогении нет гирсутизма, а есть другие кожные проявления, такие как себорея, акне вульгарис, алопеция. А вот появление терминальных волос в нижней части живота, нижней части спины, около сосков, на руках и ногах является нормальным явлением.
Уровень тестостерона в средней фазе менструального цикла сильно изменяется в течение суток — максимальный уровень в утренние часы и ниже перед началом менструальных выделений. Биологически активная часть тестостерона — свободная фракция — может повышаться, при этом уровень общего тестостерона будет в пределах нормы. Это отражает относительно низкий уровень сексстероидсвязывающего глобулина, который определяет долю свободного и связанного с альбуминами плазмы тестостерона [4].
Итак, патогенетические механизмы развития гирсутизма чрезвычайно разнообразны и недостаточно изучены.
Причины гирсутизма
Наиболее часто встречаются андрогенозависимые формы гирсутизма (75–85%). В женском организме гирсутизм, угревая сыпь, себорея, выпадение волос, огрубение голоса, гипертрофия клитора могут стать первыми и порой единственными ранними диагностическими признаками синдрома гиперандрогенемии.
Синдром поликистозных яичников
Синдром поликистозных яичников (СПКЯ), склерокистоз яичников, синдром Штейна–Левенталя. Заболевание, в основе которого лежит процесс кистозной дегенерации яичников. Характеризуется олиго- или аменореей, избыточной массой тела, гирсутизмом, акне вульгарис, алопецией, увеличенными, поликистозно измененными яичниками и ановуляторными циклами. Выявляют СПКЯ, в том числе неполные формы, у 70–80% женщин. Патогенез синдрома окончательно не выяснен. Встречается у 1,4–2,5% обследованных по поводу аменореи девушек. Современные данные свидетельствуют о том, что в формировании синдрома поликистозных яичников участвуют разные факторы. Это нарушение секреции половых стероидов в яичниках; расстройства в системе гипоталамус–гипофиз–яичники, синтеза андрогенов в надпочечниках, яичниках; рецепторные повреждения в клетках эффекторов для этих гормонов, участвующих в реализации биологических эффектов.
Определенный вклад в развитие синдрома поликистозных яичников вносит инсулинорезистентность, которая связана с нарушением действия инсулина как на рецепторном, так и пострецепторном уровнях, а также гиперпролактинемия [5].
Заболевание выявляют в период пубертата в связи с нарушением менструального цикла (первичной или вторичной аменореей). Одновременно развивается гирсутизм различной степени выраженности. Оволосение может быть над верхней губой, вокруг сосков молочных желез, вдоль белой линии живота, на бедрах. У большинства больных имеется различной степени выраженности ожирение. Наружные гениталии сформированы по женскому типу. Лишь у некоторых больных повышенные андрогены вызывают увеличение клитора.
Подтверждает диагноз увеличение почти в 2 раза лютеинизирующего гормона (ЛГ), при нормальном или даже сниженном уровне фолликулостимулирующего гормона (ФСГ). Соотношение ЛГ/ФСГ всегда увеличено. У половины больных увеличено содержание тестостерона и дегидроэпиандростерона-сульфата (ДГЭА-С), у трети — пролактина. Проведение пробы с гонадолиберином (ЛГ-РГ) вызывает гиперергическую реакцию с резким повышением ЛГ и отсутствием реакции со стороны ФСГ. Динамическое исследование гормонов ЛГ, ФСГ, эстрогена, прогестерона выявляет монотонные показатели, что подтверждает отсутствие повышения ректальной температуры. Это свидетельствует об ановуляторных циклах [6].
При ультразвуковом исследовании (УЗИ) яичники увеличены в размере, капсула плотная, строма хорошо определяется, обнаруживаются многочисленные кисты.
Дефицит ароматазы
Ароматаза — фермент, необходимый для превращения тестостерона в эстрадиол (Э2) и андростендиона в эстрон (Э1).
Дефицит ароматазы у девочек приводит к отсутствию эстрогенозависимых признаков полового созревания и появлению симптомов андрогенизации. У новорожденных девочек (ХХ) отмечаются симптомы вирилизации наружных гениталий (гипертрофия клитора, сращение лабиального шва).
В пубертатном периоде у девушек с дефицитом ароматазы отсутствуют увеличение молочных желез и менструальная функция. Симптомы вирилизации усиливаются. В яичниках наблюдаются поликистозные изменения.
При лабораторных исследованиях выявляются высокие уровни тестостерона, андростендиона, дегидроэпиандростерона и его сульфата. Уровень эстрогенов значительно снижен. Гонадотропные гормоны повышены. При генетических исследованиях обнаруживается мутация гена ароматазы CYP19. Терапия эстрогенами оказывает положительное влияние на развитие молочных желез и появление менархе [7].
Гиперпролактинемия
Появление или усиление гирсутизма, особенно у больных с олигоаменореей или аменореей, может быть обусловлено гиперпролактинемией (ГП). Повышение секреции пролактина напрямую стимулирует стероидогенез в надпочечниках, поэтому у больных с аденомой гипофиза существенно увеличивается содержание ДГЭА и ДГЭА-С при умеренной тестостеронемии [8].
Секреция пролактина регулируется гипоталамусом, который вырабатывает пролактолиберин и пролактостатин (дофамин). Патогенез гипогонадизма при гиперпролактинемии обусловлен прежде всего подавлением импульсной секреции ЛГ-РГ избытком пролактина и отрицательным влиянием на процессы стероидогенеза в гонадах. Нарушение гипоталамической регуляции секреции пролактина — снижение дофаминергического влияния или усиление продукции пролактолиберина — приводит к гиперплазии лактофоров гипофиза с возможным развитием микро- и макроаденом.
Самый ранний симптом ГП — нарушение менструальной функции, что является поводом для обращения пациенток к врачу. Обследование позволяет в некоторых случаях выявить аденому гипофиза еще на стадии микроаденом. Пролактиномы, по данным детской клиники ЭНЦ РАМН, составляют 22% от диагностированных аденом гипофиза. Чаще они выявлялись у девочек в период пубертата и проявлялись в виде синдрома первичной аменореи.
Гиперпролактинемия встречается при опухолевых заболевания гипоталамуса и гипофиза, повреждении ножки гипофиза, синдроме «пустого турецкого седла», а также травмах и воспалительных процессах основания черепа [9].
По данным A. Tuzcu и соавт. повышенный уровень пролактина связан с более тяжелыми проявлениями гирсутизма и гиперандрогенной дисфункцией яичников, с более выраженной инсулинорезистентностью. До сих пор не выяснено, является ли ГП причиной или следствием гиперандрогении у части пациенток [10].
Врожденная дисфункция коры надпочечников (ВДКН)
Это большая группа заболеваний, имеющих тот или иной генетический ферментативный дефект различных ступеней биосинтеза стероидных гормонов, приводящий к недостаточной секреции кортизола. Дефицит кортизола стимулирует выработку в аденогипофизе адренокортикотропного гормона гипофиза (АКТГ), что является причиной гиперплазии коры надпочечников. От уровня ферментативного нарушения зависит клиническая картина. При этих заболеваниях накапливаются предшественники андрогенов.
Степень выраженности влияния андрогенов при дефиците 21-гидроксилазы связана с индивидуальными особенностями метаболизма предшественников андрогенов и различием в активности периферических рецепторов андрогенов.
Если диагноз ВДКН не поставили своевременно, не начато соответствующее лечение, то вследствие анаболического действия андрогенов в первые годы девочки быстро растут, у них активно развивается скелетная мускулатура, появляется грубоватый голос, гирсутизм (оволосение по мужскому типу на лице, груди, животе, конечностях), т. е. признаки маскулинизации. У больных увеличивается размер клитора, отмечается его напряжение [11].
У девушек в пре- и пубертатном периодах отсутствуют вторичные половые признаки и менструации. Повышенная секреция андрогенов надпочечниками по принципу обратной связи блокирует выделение гонадотропинов в аденогипофизе. У пациенток по этой причине яичники уменьшены в размерах с множественными кистами, матка недоразвита. Значительно ускоряется дифференцировка скелета («костный» возраст опережает паспортный). К 10–12 годам происходит закрытие эпифизарных зон роста костей, что определяет конечную низкорослость больных. Пропорции тела у них нарушены: широкий плечевой пояс, узкий таз, хорошо развитая мускулатура. У девушек не развиваются молочные железы.
С расширением диагностических возможностей выявляют все больше вариантов неклассических пубертатных вариантов ВДКН. Первым клиническим симптомом может быть ускоренное изолированное пубархе. В ювенильном периоде при умеренной гиперандрогенемии развивается гирсутизм с сопутствующими симптомами. Формируется гиперандрогенная дисфункция яичников.
Неклассический вариант 21-гидроксилазной недостаточности с проявлениями гирсутизма и гипертрихоза очень распространен в некоторых этнических группах Югославии, Испании, у евреев ашкенази.
Преждевременное адренархе
Преждевременное адренархе (ПА) это появление изолированного оволосения на лобке и/или подмышками у девочек до 8 лет (чаще в возрасте 6–8 лет). ПА может быть вариантом нормы, учитывая, что созревание сетчатой зоны коры надпочечников начинается с 6 лет. В то время как секреция гонадолиберинов, ответственных за начало пубертата, запускается позже. Причиной пубертатного оволосения является увеличение выработки надпочечниками ДГЭА и ДГЭА-С, а также 4-андростендиона — предшественников тестостерона, которые стимулируют лобковое и подмышечное оволосение. У девочек ПА может быть связано с избыточной периферической конверсией тестостерона в дигидротестостерон (повышенная активность 5a-редуктазы). При отсутствии других признаков андрогенизации организма — ускорения роста, созревания скелета, допубертатных размеров матки и яичников, нормальных показателей тестостерона и умеренно увеличенных ДГЭА-С, прогноз благоприятный и половое развитие не отклоняется от нормы [12].
Однако у некоторых детей ПА может быть спровоцировано избыточной продукцией АКТГ (гидроцефалия, менингиты и др.). Появляется все больше доказательств связи ПА с неклассическими формами ВДКН и, в частности, дефицита активности фермента 21-гидроксилазы и реже 3β-гидроксистероиддегидрогеназы. Механизм ПА связывают с ранним созреванием сетчатой зоны коры надпочечников, доказательством этому может служить повышенный уровень ДГЭА-С. Показано, что секреция адреналовых андрогенов стимулируется АКТГ и подавляется дексаметазоном.
При наличии вирилизирующего заболевания появляются клинические признаки андрогенизации: гипертрофия клитора, высокая задняя спайка промежности, гирсутизм, развитие мышечной системы; активация сальных и потовых желез. У таких детей наблюдается ускорение роста и костного возраста. Следует отметить, что адренархе опережает повышение гонадотропинов примерно на 2 года и не связано ни с повышением чувствительности гонадотрофов к ЛГ-РГ, ни с увеличением амплитуды и частоты ночных выбросов ЛГ.
Девочки с преждевременным адренархе должны находиться в группе риска по развитию синдрома поликистозных яичников. Этой группе больных требуется корригирующая терапия глюкокортикоидами [13].
В основе гиперандрогении у больных с нарушением функции щитовидной железы (гипотиреоз) лежит существенное уменьшение продукции глобулинов, связывающих половые стероиды. Вследствие снижения уровня СССГ возрастает скорость превращения андростендиона в тестостерон [14].
Ожирение
Примерно половина страдающих гирсутизмом имеют избыточную массу. С прогрессированием ожирения, с увеличением возраста детей появляются осложнения или спутники заболевания.
В настоящее время абдоминальный жир рассматривается как активный гормонопродуцирующий орган, секретирующий большое количество факторов (адипокины) с разнообразными эффектами. Они участвуют в регуляции энергетического баланса, сердечно- сосудистой системы, эндокринной и др.
Ожирение сопровождается развитием серьезных осложнений, включая инсулинорезистентность, гипергликемию, дислипидемию, артериальную гипертензию, гиперандрогенизм. Избыточное количество жировой ткани может влиять на сроки наступления полового развития ребенка, гормональный баланс.
Гиперинсулинемия, связанная с ожирением, вносит вклад в развитие гиперандрогенемии [5]. Инсулин и инсулиноподобный фактор роста 1 обладают способностью повышать андрогеновый ответ тека-клеток яичников на стимуляцию ЛГ. Есть мнение, что инсулин усиливает чувствительность надпочечников к действию АКТГ. Возникающая при ожирении гиперинсулинемия угнетает печеночную выработку СССГ, что приводит к увеличению свободного тестостерона плазмы.
У девочек с ожирением и ПА, подростков с СПКЯ отмечаются более высокие значения инсулинорезистентности, большее снижение уровней СССГ и повышение концентраций андрогенов по сравнению со сверстницами с экзогенно-конституциональным ожирением. Девочки с ПА являются группой риска по развитию синдрома поликистозных яичников.
M. Mustaqeem и соавт. изучили этнические различия клинических и биохимических показателей женщин из Южной Азии и европейских женщин с СПКЯ (47 азиаток и 40 европеек) и контрольной группы (11 азиаток и 22 европейки). Они сообщили о значительно более высокой распространенности гирсутизма, акне, черного акантоза и вторичного бесплодия у азиаток с СПКЯ. Центральным звеном патогенеза СПКЯ считается инсулинрезистентность, однако конкретные причины пока не ясны и активно изучаются [15].
Андрогенсекретирующие опухоли
Андрогенсекретирующие опухоли надпочечников (андростеромы) относятся, как правило, к адренокарциномам. У детей встречаются редко. В раннем подростковом возрасте частота адренокарцином увеличивается у детей с синдромом Видемана–Беквита (висцеромегалия, макроглоссия, гемигипертрофия) и синдромом Ли–Фраумени (множественные злокачественные новообразования).
У больных с адренокарциномами выявлена аномальная экспрессия онкомаркеров и снижение экспрессии факторов, подавляющих рост опухоли, гены которых локализованы на длинном плече 11-й хромосомы. Аномалии этой хромосомы выявляются у большинства больных с адренокарциномой.
У девочек обнаруживаются признаки вирилизации: активизируются апокриновые железы (потовые, сальные, волосяные фолликулы), увеличивается масса тела за счет мышечной ткани, гипертрофируется клитор, ускоряется рост [2].
Стероидсекретирующие опухоли гонад
Стероидсекретирующие опухоли гонад в детском возрасте встречаются нечасто. У девочек старшего возраста обнаруживаются арренобластомы (злокачественные опухоли), располагающиеся в корковом слое или в области ворот яичника. Недифференцированные опухоли обладают более выраженным вирилизирующим действием, в то время как дифференцированные оказывают как слабо выраженное маскулинизирующее, так и феминизирующее влияние [16].
Избыточный рост терминальных волос с распределением их по мужскому типу часто обнаруживается у девушек с гипоталамическим синдромом периода полового созревания, проявляющимся нарушением менструального цикла (олигоменореи, аменореи, маточные кровотечения).
У части больных с истинным преждевременным половым развитием (ППР) не удается выявить причину заболевания. В таких случаях при исключении органических заболеваний ЦНС ставится диагноз идиопатической формы ППР. Однако совершенствование методов исследования (компьютерная и магнитно-резонансная томография) головного мозга позволяют чаще выявлять причину церебральной формы гиперандрогенемии (гамартома, глиома, ХГЧ-секретирующие опухоли и др.) у девочек.
Синдром Корнелии де Ланге
Редкий генетический синдром с общей распространенностью 1,6–2,2:100 000 человек. Является доминантно наследуемым, большинство случаев связано с мутациями de novo. Синдром генетически гетерогенный, половина случаев связана с мутацией в гене регуляторе NIPBL и HDAC8, около 5% случаев — мутациями в гене SMC1A (SMC3, RAD21), кодирующем белок в кохезиновом комплексе. Клиническая картина весьма вариабельна, типична лицевая дисморфия, микроцефалия, тугоухость, пузырно-мочеточниковый рефлюкс, задержка внутриутробного развития и замедление постнатального роста ребенка, пороки развития конечностей и половых органов, гирсутизм, врожденные пороки сердца и желудочно-кишечного тракта. Отличительные черты лица: низкий рост волос, густые сросшиеся брови, густые и длинные ресницы. Гирсутизм отмечается у 78% пациентов. Больше чем у половины новорожденных наблюдается повышенная волосистость спины, а иногда и всего тела.
Часто синдром сопровождается эпилепсией, проблемами с поведением в виде синдрома дефицита внимания, агрессии, в том числе аутоагрессии. Специфического лечения и профилактики в настоящее время не разработано.
Синдром Рубинштейна Тэйби
Редкое генетическое заболевание. Средняя частота 1 на 10 000–300 000 новорожденных. Заболевание характеризуется разной степенью нарушения интеллекта, специфическими чертами лица и строением кисти (аномально широкие и часто изогнутые большие пальцы рук), дисфагия. В половине случаев встречается гирсутизм. Заболевание связано с мутацией гена de novo, может передаваться по наследству по аутосомно-доминантному типу. Самый распространенный вариант дефект гена, расположенного на коротком плече 16-й хромосомы (16р13.3). В основе синдрома лежит дефект гена CREBBP и EP300, у пациентов с мутацией EP300 менее грубые скелетные аномалии. Напротив, у пациентов с делецией 16-й хромосомы, содержащей гены EP300 и CREBBP, грубые множественные пороки развития.
Диагноз часто ставится фенотипически. Особенности строения лица: антимонголоидный разрез глаз, длинные ресницы, арочные брови, высокое небо, низко висящая носовая перегородка (колумелла). Есть много осложнений, ассоциированных с данным синдромом, например, пороки сердца и почек, ожирение, отиты, высокий риск неопластических процессов.
Синдром Донахью
Чрезвычайно редкое генетическое заболевание, характеризующееся нарушением толерантности к инсулину, задержкой роста, эндокринопатиями. Может быть вызван нарушением в гене, расположенном на коротком плече 19-й хромосомы (19p13.2), ответственном за регуляцию рецепторов к инсулину. У детей с синдромом Донахью отмечается задержка постнатального роста, нарушение костного созревания. Низкая мышечная масса. Дети имеют своеобразное строение лица: низко посаженные плохо развитые ушные раковины, толстые губы и большой рот, плоскую спинку носа, широко расставленные глаза, микроцефалию.
В большинстве случаев имеются особенности строения кожи: ее утолщение, потемнение (черный акантоз), гирсутизм, acanthosis nigricans. Гиперандрогения яичникового происхождения.
У девочек отмечается увеличение молочных желез и клиторомегалия. Из-за постоянного гиперинсулинизма выраженная гипогликемия натощак. Прогноз неблагоприятный.
Синдром HAIR-AN
Субфенотип синдрома поликистозных яичников, проявляется гиперандрогенией, инсулинорезистентностью, ожирением и черным акантозом, известен уже более 30 лет. СПКЯ одна из самых распространенных причин нарушения менструального цикла у девушек. Статистика посещения амбулаторных клиник подростками за 2 года показала, что из 1002 девушек (возраст 10–21 год) у 5% (50) был диагностирован HAIR-AN-синдром. Средний возраст пациенток составил 15,5 лет, средний вес на момент постановки диагноза 94,5 кг (ИМТ 33,3 кг/м 2 ). В основе лечения снижение веса, применение метформина. У 80% пациенток был ответ на лечение, у 95% установился регулярный менструальный цикл, уменьшились гирсутизм, акне [15].
Около 5% девушек с гиперандрогенией и инсулинрезистентностью имеют черный акантоз. Пациентки с HAIR-AN-синдромом могут иметь и другие признаки вирилизации при нормальной функции надпочечников, аменорею. Пациентки, как правило, имеют нормальный уровень ЛГ и ФСГ, хотя соотношение их может быть нарушено.
Симптомы гирсутизма могут провоцировать длительное применение гормональных препаратов: анаболические стероиды, андрогены, глюкокортикоиды, эстрогенсодержащие (оральные контрацептивы) и др. Провоцируют активный рост волос антидепрессанты, некоторые цитостатики.
Конституциональный гирсутизм
Избыточный рост волос заложен на генетическом уровне. Наследственная предрасположенность ведет к развитию так называемой конституциональной формы гирсутизма. В этом случае гирсутизм чаще расценивается не как патология, а как один из вариантов нормы. Встречается у женщин Средиземноморья и Ближнего Востока. Причиной наследственного гирсутизма считается повышенная чувствительность волосяных фолликулов к дигидротестостерону. Даже небольшое количество андрогенов, которое является нормой для женщин, ведет к более быстрому и обильному росту волос. Избыточное оволосение начинает проявляться в детстве и достигает пика к подростковому возрасту. Других симптомов андрогенизации нет. При чрезмерном росте волос рекомендуется консультация с дерматологом или косметологом и обычная эпиляция.
Идиопатический гирсутизм
Диагноз «идиопатический гирсутизм» ставят в тех случаях, когда не удается найти какую-либо причину избыточного роста волос. По клиническим симптомам и механизму развития очень близок к наследственной форме избыточного оволосения. У пациенток с идиопатическим гирсутизмом отсутствуют другие жалобы, связанные с андрогенемией. В отличие от наследственного гирсутизма заболевание может проявиться не у подростков, а в более позднем возрасте. В этих случаях механизмы, которые влияют на чувствительность волосяных фолликулов к андрогенам, не выяснены.
Дифференциальная диагностика
Гирсутизм следует отличать от гипертрихоза — общего избыточного роста волос, являющегося следствием конституциональной особенности человека. При гипертрихозе избыточный волосяной покров наблюдается на участках тела, не характерных для женского пола (на конечностях, грудной клетке). Как правило, эти участки кожи покрыты пушковыми обесцвеченными или темноокрашенными волосами. При гипертрихозе не происходит увеличения роста волос только в андрогензависимых зонах и напрямую не связано с гиперандрогенемией, хотя это может усугублять проявление гирсутизма. Гипертрихоз может быть следствием использования медикаментов, таких как стероиды, иммунодепрессанты и др.
Обследование
Гетерогенность гирсутизма требует тщательного поиска ее причины. Следует обращать внимание на возраст пациента, связь с приемом препаратов, отягощенность ближайших родственников по гирсутизму, этническую принадлежность. Степень выраженности гирсутизма проводится по шкале Ферримана–Голлвея, которая позволяет оценить распространенность грубых волос в девяти андрогензависимых зонах — верхней губе, подбородке, плечах, груди, верхней и нижней частях живота, спине, пояснице, бедрах. Оценка производится по пятибалльной шкале, а общий показатель выраженности гирсутизма может варьировать в пределах 0–36 баллов. Если показатель составляет 8 баллов и выше, то можно говорить о наличии гирсутизма.
При обследовании нужно измерять рост, вес, распределение подкожно-жирового слоя, индекс массы тела (ИМТ), окружность талии и бедер, артериальное давление. Определить стадию полового развития. Отметить кожные изменения.
Лабораторные исследования проводятся для подтверждения диагноза при соответствующей клинике гиперандрогенемии и для идентификации источника избыточных андрогенов: надпочечники, яичники, ЦНС.
- Биохимический анализ крови: общий холестерин, ЛПНП, ЛПВП, триглицериды, ферменты (АЛТ, АСТ).
- Гликемия натощак, глюкозотолерантный тест.
- Гормональный профиль: инсулин, С-пептид, ЛГ, ФСГ, кортизол, тестостерон, ДГЭА, ДГЭА-С, пролактин, 17-гидроксипрогестерон, по показаниям ТТГ, Т4, СССГ.
- Костный возраст.
- Для оценки жировой массы используется биоимпедансометрия.
- УЗИ печени, поджелудочной железы, почек, надпочечников, яичников.
- Молекулярно-генетические исследования.
- Для уточнения причины, вызвавшей гирсутизм, рекомендуется ультразвуковое исследование или компьютерная томография органов малого таза и надпочечников, магнитно-резонансная томография головного мозга.
- Для исключения опухолей в яичниках проводят диагностическую лапароскопию.
Лечение
Лечение гирсутизма, если оно вызвано гиперандрогенемией, является трудной задачей. Основная цель лечения это нормализация секреции стероидных гормонов, вызывающих избыточный рост волос и другие симптомы андрогенизации. Данная патология может быть обусловлена нарушением в системе гонадостата на различных уровнях, требующим индивидуального подхода к выбору метода лечения. Применение только косметических мероприятий, особенно при тяжелых формах заболевания, приводит к кратковременному клиническому эффекту и исключительно редко к излечению. Диагностикой и лечением пациенток с гирсутизмом обычно занимается врач-эндокринолог, гинеколог, дерматолог.
Основной проблемой у девушек-подростков с гирсутизмом являются психологические комплексы из-за косметической проблемы. Изменения психики характеризуются симптомами депрессии. Подростки подавлены и практически всегда видят причину своих неудач в дефектах внешности. Они нуждаются в психологической поддержке. Проведение психокоррекционных мероприятий под контролем врача и психолога позволит девушкам с гирсутизмом взять на себя ответственность за контроль и стать соучастниками в лечении своей болезни.
Правильно проведенная психокоррекция способствует уменьшению клинических проявлений заболевания, повышению социальной активации больных, их адаптации в семье и обществе, а также повышает эффективность лечебных мероприятий.
Литература
- Скрипкин Ю. К., Кубанова А. А., Акимов В. Г. Кожные и венерические болезни: учебник. 2011. 544 с.
- Дедов И. И., Семичева Т. В., Петеркова В. А. Половое развитие детей: норма и патология. М., 2002. 232 с.
- Рагимова З. Э., Каиль-Горячкина М. В. Междисциплинарные аспекты андрогензависимой дермопатии (обзор литературы) // Consilium Medicum. Дерматология. 2016, 3: 56–62.
- Руководство по детской эндокринологии / Под ред. Чарльза Г. Д. Брука, РозаЛинд С. Браун: пер. с англ. под ред. В. А. Петерковой. М.: ГЭОТАР-Медиа, 2009. 352 с.
- Гуркин Ю. А. Детская и подростковая гинекология. М.: МИА, 2009. С. 148–180.
- Богатырева Е. М., Новик Г. А., Кутушева Г. Ф. Фенотипы и эндотипы синдрома гиперандрогении у девочек-подростков // Лечащий Врач. 2016, № 2, с. 70.
- Wilson J. D., Aiman J., MacDonald P. C. The Pathogenesis of Gynecomastia // Advanc. in intern. Med. 1980, 25: 1–32.
- Московкина А. В., Пузикова О. З., Линде В. А., Рыбинская Н. П. Гиперпролактинемия у девочек подростков с синдромом гиперандрогении // Детская больница. 2013, № 2, с. 35–39.
- Коколина В. Ф. Гинекологическая эндокринология детей и подростков. М.: Медицинское информационное агентство, 2001. 287 с.
- Журтова И. Б. Синдром гиперпролактинемии у детей и подростков. Оптимизация методов диагностики и лечения. Автореф. дисс. д.м.н, М., 2012.
- Tuzcu A., Bahceci M. et al. Is hyperprolactinemia associated with insulin resistance in non_obese patients with polycystic ovary syndrome // J Endocrinol Invest. 2003; 26: 655–659.
- Дедов И. И., Петеркова В. А. Руководство по детской эндокринологии. М.: Универсум Паблишинг, 2006. 600 с.
- Эндокринология. Национальное руководство. Краткое издание / Под ред. И. И. Дедова, Г. А. Мельниченко. М: ГЭОТАР-Медиа, 2013. 752 с.
- Дедов И. И., Петеркова В. А. Федеральные клинические рекомендации (протоколы) по ведению детей с эндокринными заболеваниями. М.: Практика, 2014. 442 с.
- Onal E. D., Saglam F., Sacikara M., Ersoy R., Cakir B. Thyroid autoimmunity in patients with hyperprolactinemia: an observational study // Arq Bras Endocrinol Metabol. 2014, Feb
- Mustaqeem M., Sadullah S., Waqar W., Farooq M. Z., Khan A., Fraz T. R. Obesity with irregular menstrual cycle in young girls // Mymensingh Med J. 2015, Jan; 24 (1): 161–167.
- Петеркова В. А., Семичева Т. В., Горелышев С. К., Лозовая Ю. В. Преждевременное половое развитие. Клиника, диагностика, лечение. Пособие для врачей. М., 2013. 40 с.
В. В. Смирнов 1 , доктор медицинских наук, профессор
А. А. Накула
ФГБОУ ВО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
Гиперандрогения — симптомы и лечение
Что такое гиперандрогения? Причины возникновения, диагностику и методы лечения разберем в статье доктора Скатова Бориса Валерьевича, андролога со стажем в 29 лет.
Над статьей доктора Скатова Бориса Валерьевича работали литературный редактор Вера Васина , научный редактор Светлана Симанина и шеф-редактор Маргарита Тихонова

Андролог Cтаж — 29 лет
Медицинский центр «Рефлекс»
Клиника «Бионика»
Дата публикации 22 апреля 2021 Обновлено 17 июня 2021
Определение болезни. Причины заболевания
Гиперандрогения — это состояние, при котором у женщины в крови значительно повышен уровень мужских половых гормонов (андрогенов): тестостерона, дигидротестостерона, андростендиона и других.
Распространённость
Гиперандрогения встречается у 17–18 % женщин детородного возраста. Заболеванием страдают 16–22 % пациенток с бесплодием и 55–62 % — с эндокринным нарушением репродуктивных функций [1] .
Причины
- снижение уровня глобулина, связывающего половые гормоны (ГСПГ), и увеличение концентрации свободного тестостерона;
- синдром поликистозных яичников (СПКЯ);
- опухоли яичников и коры надпочечников, выделяющие андрогены;
- гиперплазия коры надпочечников, в том числе врождённые формы, вызванные мутациями генов CYP21, CYP11B1, HSD3B;
- аденома гипофиза (синдром Иценко — Кушинга);
- синдром HAIR-AN — наследственное заболевание, при котором высокий уровень андрогенов сочетается с инсулинорезистентностью и чёрным акантозом (гиперпигментацией кожи);
- профессиональные занятия единоборствами, хоккеем, футболом и тяжёлой атлетикой [14][15] ;
- приём андрогенов и анаболических стероидов;
- хронический стресс;
- табакокурение и злоупотребление алкоголем[2] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы гиперандрогении
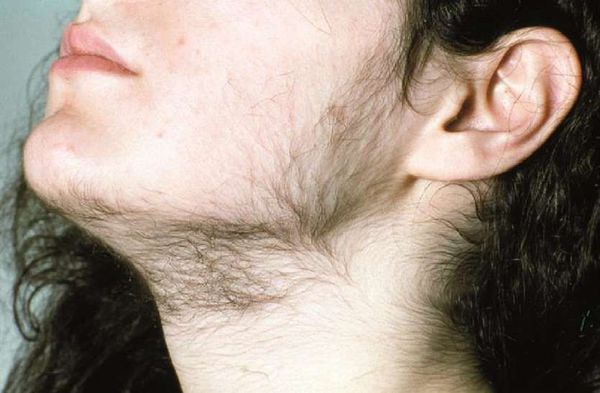
- гирсутизм (избыточное оволосение по мужскому типу) — значительный рост жёстких чёрных волос в зонах, наиболее чувствительных к мужским гормонам: вокруг сосков, на лице, груди, животе, спине и бёдрах;
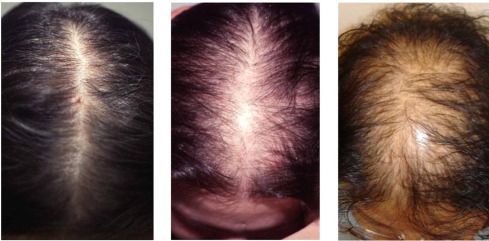
- андрогенная алопеция;
- бесплодие;
- маскулинизация — проявление и усиление у женщин мужских черт, при котором расширяется плечевой пояс, сужаются бёдра и снижается тембр;
- ожирение по мужскому типу, при котором жир откладывается в брюшной полости;
- нарушения менструального цикла: олигоменорея (редкие и скудные менструации) или аменорея (длительное отсутствие менструаций);
- угревая сыпь, жирная кожа и себорея;
- повышенное половое влечение;
- увеличение клитора и уменьшение молочных желёз;
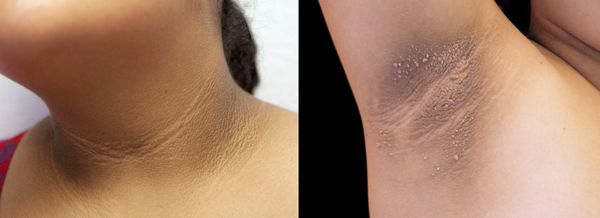
- чёрный акантоз — кожа утолщается и меняет цвет из-за избыточного ороговения клеток эпителия и эпидермиса, а также увеличения уровня пигмента меланина [3] ;
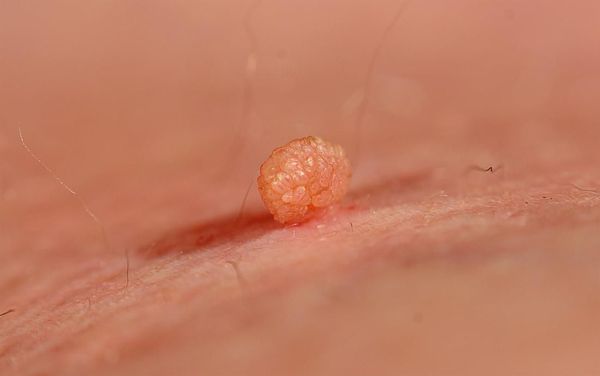
- мягкие фибромы на коже в области шеи, подмышек и паховых складок — доброкачественные новообразования округлой формы и мягкой консистенции.
Патогенез гиперандрогении
Андрогены — стероидные половые гормоны, которые вырабатываются из холестерина в коре надпочечников, а также в клетках фолликулов и соединительной ткани яичников.
К андрогенам относятся:
- тестостерон;
- андростендион;
- дегидроэпиандростерон и др.
В печени, жировой ткани и волосяных фолликулах андрогены способны превращаться в более активную форму — дегидротестостерон. Кроме того, в жировой ткани андрогены преобразуются в женский половой гормон эстрадиол [3] .
Роль андрогенов
В женском организме андрогены поддерживают гормональный баланс и после начала полового созревания инициируют рост волос на лобке и в подмышечных впадинах. Также они необходимы для выработки эстрогена и возникновения полового влечения.
Андрогены замедляют потерю кальция в костях и регулируют работу внутренних органов и систем: репродуктивной, почечной, мышечной и сердечной.
Гормональная регуляция происходит почти мгновенно с малым количеством активного вещества — гормона. Другая её особенность заключается в дистанцировании: гормон может вырабатываться в одной железе, а попадать в орган-мишень, находящийся в другой части организма.
Кроме этого механизма, андрогены могут действовать опосредованно, например через эстрогены — женские половые гормоны [4] .
В плазме крови андрогены взаимодействуют с глобулином, связывающим половые гормоны (ГСПГ). Он выполняет транспортную роль: вместе с ним андрогены доставляются с кровью в клетки органов-мишеней.
Выработка андрогенов зависит от возраста и объёма жировой массы. При старении, ещё до менопаузы, их уровень постепенно уменьшается, особенно снижается концентрация дегидроэпиандростерона и андростендиона. На уровень тестостерона возраст влияет меньше: яичники вырабатывают его почти в прежнем объёме и в постменопаузе [13] .
Избыток андрогенов
К избытку андрогенов могут приводить различные патологические механизмы:
- Развитие опухолей и множественных кист яичников. Изменённые клетки яичников влияют на ферменты, участвующие в обмене стероидных гормонов. К таким ферментам относится 17-альфа-гидроксилаза, играющий ключевую роль в синтезе андрогенов в яичниках.
- Образование опухолей в надпочечниках и гиперплазия коры надпочечников также приводят к избыточной выработке андрогенов.
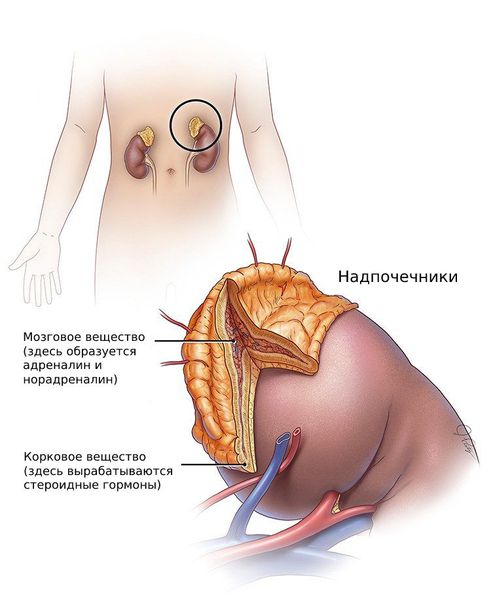
- На дисбаланс андрогенов влияют другие гормоны: пролактин, эстрадиол и тиреотропные гормоны. Они взаимодействуют друг с другом, например при снижении уровня эстрадиола может расти уровень тестостерона. Это происходит из-за нарушения ферментных систем яичников, которые позволяют андрогенам яичникового происхождения превращаться в эстрогены.
- Гипотиреоз (снижение функции щитовидной железы и, соответственно, гормонов Т3, Т4) сопряжён с ростом уровня пролактина, который воздействует на кору надпочечников и стимулирует выработку андрогенов.
- При недостатке трийодитрина (Т3, самый активный гормон щитовидной железы) снижается концентрация глобулина, связывающего половые гормоны, и растёт уровень свободного тестостерона.
Повышать уровень андрогенов могут и другие внешние факторы, например приём стероидов и гормональных препаратов. Интересно, что при всех гиперандрогенных состояниях, андрогены происходят более чем из одного источника. Так, при поликистозе яичников увеличен синтез тестостерона, но большая часть этого гормона образуется вне яичников — в надпочечниках.
Большую роль в развитии первичной гиперандрогении играют генетические факторы. Одной из причин синдрома поликистозных яичников (СПКЯ) является генетически предопределённый избыток лютеинизирующего гормона (ЛГ). ЛГ стимулирует образование мужских половых гормонов: тестостерона и андростендиона. Их чрезмерная выработка нарушает процесс развития фолликулов: они преждевременно перерождаются в жёлтое тело и в этой области образуются фолликулярные кисты.
Другая причина развития СПКЯ — генетически обусловленное нарушение выработки инсулина и развитие инсулинорезистентности, то есть недостаточный ответ тканей на его действие.
К гиперандрогении, как было сказано выше, может приводить врождённая гиперплазия коры надпочечников. Причина её развития — мутации генов, которые отвечают за синтез ферментов или транспортных белков, участвующих в выработке кортизола.
Классификация и стадии развития гиперандрогении
Согласно Международной классификации болезней (МКБ-10), гиперандрогения кодируется как Е.28.1 Избыток андрогенов. Выделяют истинную гиперандрогению и другие её формы.
Истинная гиперандрогения
Истинная гиперандрогения бывает яичниковой и надпочечниковой
Яичниковая гиперандрогения:
1. Синдром поликистозных яичников. Первичный СПКЯ (синдром Штейна — Левенталя) возникает при нарушении в системе гипоталамус-гипофиз-яичники. Вторичный СПКЯ развивается при эндокринной патологии, например на фоне сахарного диабета, заболеваний щитовидной железы или под воздействием внешних факторов: интоксикации, стресса, травмы и инфекции.
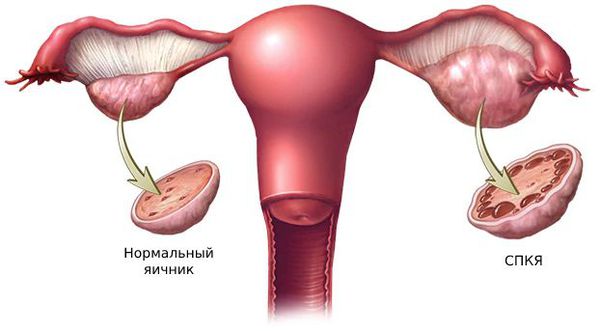
2. Стромальный текоматоз яичников (синдром Френкеля) — тяжёлая форма овариальной неопухолевой гиперандрогении. При заболевании разрастается соединительная ткань и возникает синдром HAIR-AN (высокий уровень андрогенов, инсулинорезистентности, ожирение и чёрный акантоз). Это редкая патология выявляется преимущественно в постменопаузе.
3. Андроген-продуцирующая опухоль яичников:
- гранулезоклеточная опухоль;
- текома;
- андробластома;
- липидоклеточные опухоли.
Надпочечниковая гиперандрогения:
- врождённая гиперплазия коры надпочечников;
- андрогенома — опухоль коры надпочечников, продуцирующая андрогены (тестостерон и дегидроэпиандростерон-сульфат).
Другие формы гиперадрогении
- Транспортная (снижение уровня глобулина, связывающего половые гормоны).
- Периферическая:
- рецепторная;
- метаболическая (повышение уровня фермента 5-альфа-редуктазы).
- Ятрогенная — при приёме андрогенов, анаболических стероидов и глюкокортикоидов. Анаболические гормоны принимаются при выраженном истощении, восстановлении массы тела после тяжёлых заболеваний и травм. Глюкокортикоиды назначают для лечения аутоиммунных заболеваний, например ревматоидных болезней, системной красной волчанки и др.
- Вторичная — андрогензависимые дерматопатии: вульгарные угри, гирсутизм, алопеция и себорея[1] .
Осложнения гиперандрогении
- Ожирение верхней части тела и инсулинорезистентность. Избыток андрогенов влияет на рецепторы инсулина, которыми насыщена жировая ткань верхней части тела. Инсулин переводит углеводы в жировые запасы, и развивается ожирение.
- Сахарный диабет второго типа и гестационный диабет.
- Дислипидемия (повышение уровня холестерина и липопротеидов низкой плотности) и развитие атеросклероза.
- Сердечно-сосудистые заболевания.
- Невынашивание беременности, синдром потери плода, фетоплацентарная недостаточность, гестоз.
- Бесплодие.
- Онкологические процессы матки, молочных желёз и яичников.
- Обильные маточные кровотечения, геморрагический шок и анемия[1][5] .
Наиболее частые осложнения гиперандрогении: бесплодие, инсулинорезистентность и ожирение. Нарушение обмена липидов, сахарный диабет, сердечно-сосудистая патология возникают как следствие этих процессов.
Механизмы развития гиперандрогении и гиперинсулинемии до конца не изучены. Теоретически возможны три варианта взаимодействия: гиперандрогения вызывает гиперинсулинемию, гиперинсулинемия приводит к гиперандрогении и есть третий фактор, ответственный за оба феномена.
Предположение о том, что гиперандрогения вызывает гиперинсулинемию, основано на следующих фактах:
- у женщин, которые принимают оральные контрацептивы, содержащие прогестины с андрогенными свойствами, нарушается толерантность к глюкозе;
- длительный приём тестостерона приводит к развитию инсулинорезистентности.
О том, что гиперинсулинемия вызывает гиперандрогению, свидетельствует следующее: инсулинорезистентность сохраняется у пациенток с удалёнными яичниками и при длительном приёме препаратов, подавляющих выработку андрогенов.
Диагностика гиперандрогении
Диагностика проводится эндокринологом или гинекологом-эндокринологом.
Этапы:
1. Опрос (сбор анамнеза). Врач беседует с пациенткой и выясняет следующие факты:
- приём лекарств, особенно содержащих мужские половые гормоны, например препараты тестостерона — «Андриол», «Омнадрен», «Андрогель» и др.;
- регулярность менструального цикла;
- сведения о беременности и родах;
- время появления и скорость развития избыточного оволосения;
- изменение формы лица и прибавка в весе;
- наличие залысин и характер выпадения волос;
- присутствие угрей и степень жирности кожи;
- наличие диабета у близких родственников;
- образ жизни: употребление алкоголя, курение, уровень физической активности и особенности диеты.
2. Осмотр. Доктор обращает внимание на следующие симптомы:
- признаки синдрома Иценко — Кушинга: лунообразное лицо, жировые отложения на шее, ожирение при тонких конечностях и длинных пальцах, сухая кожа, стрии (растяжки) и язвы на теле;
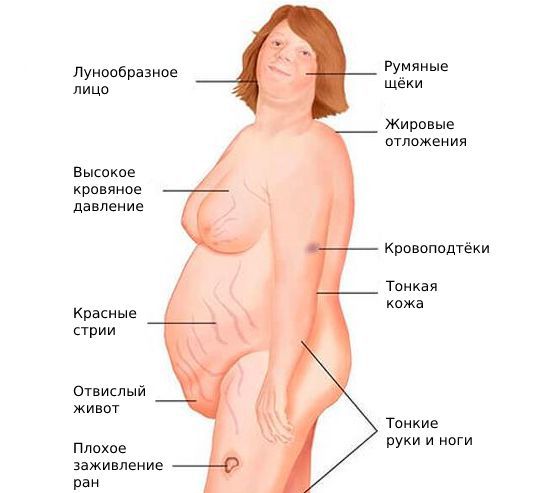
- чёрный акантоз, мягкие фибромы и угревая сыпь;
- признаки мужественности и ожирения по мужскому типу;
- увеличенный клитор;
- распределение волос на теле, которое оценивается по визуальной шкале гирсутизма Ферримана — Голлвея.
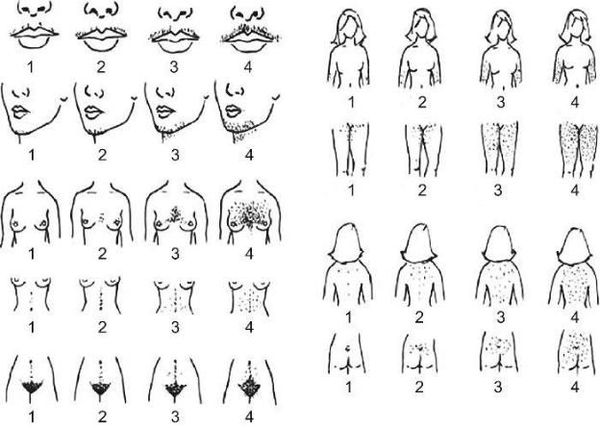
3. Лабораторные исследования:
- Оценка работы половой системы — анализ крови на общий тестостерон, ГСПГ (глобулин, связывающий половые гормоны), ФСГ (фолликулостимулирующий гормон), ЛГ (лютеинизирующий гормон), пролактин, эстрадиол, альбумин, дигидротестостерон, прогестерон, андростендион, дегидроэпиандростерон-сульфат.
- Оценка гормонов надпочечников — анализ крови на кортизол и на 17-гидроксипрогестерон.
- Оценка работы щитовидной железы и углеводного обмена — анализ крови на ТТГ (тиреотропный гормон), Т3 свободный, Т4 свободный, Т3 реверсивный, АТ к ТПО (антитела к тиреопероксидазе), АТ к ТГ (тиреоглобулину), АТ к рецепторам ТТГ (тиреотропному гормону), анализ на содержание йода в моче, уровень глюкозы и инсулина натощак (индекс Хома), гликированный гемоглобин.
Направление на анализы выписывает врач, так как часть из них нужно проводить в определённые дни менструального цикла.
4. Инструментальная диагностика:
- Трансвагинальное УЗИ яичников позволяет обнаружить признаки синдрома поликистозных яичников, кист и других новообразований.
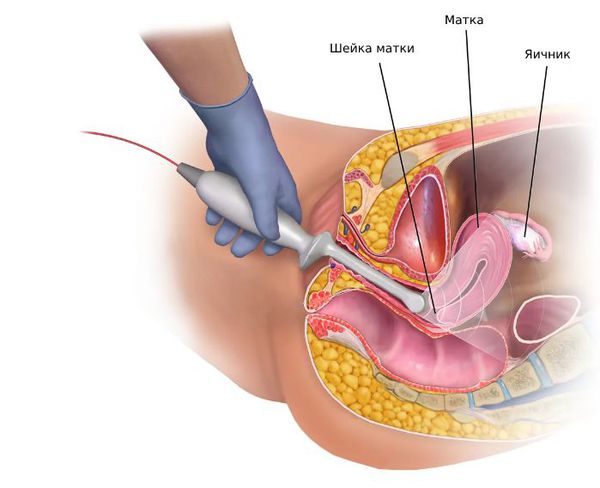
- УЗИ щитовидной железы выявляет новообразования, кисты, признаки воспаления щитовидной железы и позволяет оценить её размер и структуру.
- УЗИ, МСКТ (мультиспиральная компьютерная томография) и МРT (магнитно-резонансная томография) надпочечников. Исследования выявляют дисплазию и новообразования надпочечников.
- Сцинтиграфия надпочечников после внутривенного введения радиоактивного меченого холестерина. Позволяет выявить скрытую дисплазию и небольшие опухоли надпочечников. Несмотря на применение радиоактивных элементов, процедура безопасна для организма. Вводимые вещества обладают высокой скоростью полураспада: обычно процесс длится не более шести часов. Этого времени достаточно, чтобы провести процедуру, но не навредить организму [1][2][3][6][7] .
Лечение гиперандрогении
Заболевание лечит врач-эндокринолог или гинеколог-эндокринолог.
Лечение поможет устранить симптомы и достичь основных целей:
- нормализовать менструальный цикл;
- устранить бесплодие, вызванное нарушением созревания яйцеклетки и выхода её из яичника;
- устранить кожные проявления;
- вылечить обменные нарушения.
Нормализация менструального цикла уменьшает риск гиперплазии эндометрия и рака тела матки, маточных кровотечений и постгеморрагической анемии.
- комбинированные оральные контрацептивы (КОК);
- циклический или постоянный приём прогестогенов и средств, повышающих чувствительность периферических тканей к инсулину (метформин).
В редких случаях выполняют операции на яичниках.
Комбинированные оральные контрацептивы (КОК) снижают уровень гонадотропинов, а значит и концентрацию андрогенов, которые производятся в яичниках. Содержащиеся в КОК эстрогены увеличивают синтез глобулина, связывающего половые гормоны и, следовательно, снижают уровень свободного тестостерона. Кроме того, прогестагены в составе КОК уменьшают синтез андрогенов в надпочечниках, подавляют фермент 5-альфа-редуктазу и блокируют связывание андрогенов с рецепторами.
Оптимальными будут КОК, содержащие прогестаген с антиандрогенным действием: ципротерон, хлормадинон, диеногест и дроспиренон. Также предпочтительны оральные контрацептивы с этинилэстрадиолом.
Наиболее известные КОК, применяемые для лечения гиперандрогении:
- «Джес», «Димиа», «Ярина» — результат достигается быстро, уже через две недели, но у препаратов много побочных эффектов. Среди них: головная боль, боли в животе, тошнота, рвота; болезненность и нагрубание молочных желёз; увеличение веса, нарушение толерантности к глюкозе, задержка жидкости в организме; изменение либидо и снижение настроения; отёки век, кожная сыпь, узловая эритема, конъюнктивит, неприятные ощущения при ношении контактных линз; тромбофлебит, периферическая и центральная тромбоэмболия (может проявляться ухудшением зрения и слуха); генерализованный зуд, холестатическая желтуха, холелитиаз, повышение артериального давления; межменструальное кровотечение, изменение влагалищной секреции, кандидоз влагалища. Побочные эффекты могут возникать в первые несколько месяцев приёма препарата и обычно уменьшаются со временем.
- «Жанин», «Хлое» — могут назначаться молодым нерожавшим женщинам при избыточном оволосении, совместимы со многими препаратами.
- «Логест» — предпочтителен при выпадении волос.
- «Белара» — при СПКЯ и ожирении.
- «Линдинет-30», «Регулон», «Ярина», «Диане-35» и другие препараты [7][8] .
Прогестагены нормализуют менструальный цикл при циклическом или постоянном приёме. Однако есть гипотезы, что прогестерон сам обладает андрогеноподобным действием. Его, как правило, не назначают для лечения гиперандрогении, но применяют для нормализации второй фазы менструального цикла.
Блокаторы андрогенных рецепторов из–за выраженной тератогенности (влияния на внутриутробную закладку органов будущего ребёнка) беременным принимать запрещено.
Основные препараты из группы блокаторов андрогенных рецепторов:
- «Спиронолактон» — широко применяется в США как диуретик и нестероидный антиандроген. Эффективен при избыточном оволосении по мужскому типу.
- «Ципротерон» — снижает уровни тестостерона и андростендиона, подавляя секрецию лютеинизирующего гормона, блокирует действие андрогенов в периферических тканях. Среди побочных эффектов выделяют надпочечниковую недостаточность и снижение полового влечения [8][9] .
- «Финастерид» — уменьшает гирсутизм, но оказывает сильное тератогенное действие на эмбрионы мужского пола, поэтому при его приёме необходима надёжная контрацепция [11] .
Дозировку и режим приёма препаратов врач назначает индивидуально.
Фитотерапия играет вспомогательную роль. Применяют экстракт зелёного чая, сереноа (экстракт южно-американской пальмы), семя льна, пион, сою, стевию и дягель [10] [16] .
Способы удаления волос при гирсутизме
Электроэпиляция позволяет избавиться от волос на долгий срок, но потребуется несколько процедур, количество которых подбирают индивидуально [3] .
Существуют три вида электроэпиляции:
- электролиз — в волосяной фолликул вводят один или несколько стерильных электродов, по ним поступает постоянный ток и специальное химическое вещество;
- термолиз — через стерильный электрод в волосяной фолликул подают высокочастотный переменный ток, создающий тепло и разрушающий фолликул;
- смешанный тип — применяют два вида тока.
Побочные эффекты электроэпиляции: ожоги, раздражение кожи, редко — образование рубцов.
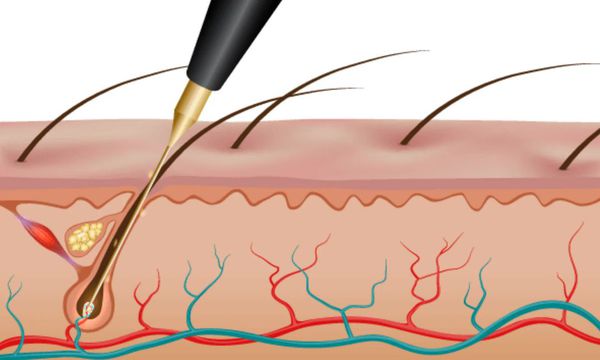
Лазерная эпиляция позволяет повредить волосяной фолликул, не разрушив окружающие его ткани. Процедуры нужно проводить многократно, но полностью избавиться от волос удаётся редко. В зависимости от источника светового излечения лазеры для удаления волос делятся на три группы:
- красные — рубиновый лазер с длиной волны 694 нм;
- инфракрасные — александритовый лазер (с длиной волны 755 нм), диодный (800 нм) и неодимовый (1064 нм);
- импульсные источники лазерного излучения высокой интенсивности (590–1200 нм) [12] .
Прогноз. Профилактика
Если своевременно обратиться к врачу и правильно подобрать лечение, то можно уменьшить неприятные симптомы и избежать серьёзных осложнений.
Результаты терапии следует оценивать через 3–6 месяцев, потому что антиандрогенные препараты действуют медленно: они постепенно накапливаются в организме и встраиваются в обмен веществ. Их приём требует адекватного дозирования, а также регулярной оценки результатов и возможных побочных действий.
Лечение позволяет избавиться от симптомов, поэтому для грамотной коррекции терапии пациентке необходимо регулярно посещать врача-эндокринолога
Профилактика:
- обратиться к доктору при появлении первых признаков гиперандрогении;
- вести здоровый образ жизни;
- избегать хронических стрессов;
- сбалансировать питание;
- не злоупотреблять алкоголем;
- с осторожностью заниматься борьбой, бодибилдингом и тяжёлой атлетикой;
- исключить приём препаратов с мужскими половыми гормонами, анаболических стероидов и глюкокортикоидов [7] .
Список литературы
- Эндокринология. Национальное руководство / под редакцией И. И. Дедова, Г. А. Мельниченко. — М.: ГЭОТАР-Медиа, 2020. — 832 с.
- Williams textbook of endocrinology, 13th edition. Сhapters 17, 18, 19 and 20 // Elsevier. — 2018 .
- Carr, Bruce R. Essential reproductive medicine. — McGraw-Hill, 2015. — 832 p.
- Rosenfield R. L., Ehrmann D. A. The Pathogenesis of Polycystic Ovary Syndrome (PCOS): The Hypothesis of PCOS as Functional Ovarian Hyperandrogenism // Endocr Rev. — 2016; 37 (5): 467-520. ссылка
- Wei D. M. et al. Effect of hyperandrogenism on obstetric complications of singleton pregnancy from in vitro fertilization in women with polycystic ovary syndrome. — 2018; 53 (1): 18-22. ссылка
- Williams T., Mortada R., Porter S. Diagnosis and Treatment of Polycystic Ovary Syndrome // Am Fam Physician. — 2016; 94 (2): 106-113.ссылка
- Carmina E., Guastella E., Longo R. A. Advances in the Diagnosis and Treatment of PCOS. // Curr Pharm Des. — 2016; 22 (36): 5508-5514. ссылка
- Amiri M., Kabir A., Nahidi F., Shekofteh M., Ramezani Tehrani F. Effects of combined oral contraceptives on the clinical and biochemical parameters of hyperandrogenism in patients with polycystic ovary syndrome: a systematic review and meta-analysis. // Eur J Contracept Reprod Health Care. — 2018; 23 (1): 64-77. ссылка
- Fabbrocini G., Cantelli M., Masarà A., Annunziata M. C., Marasca C., Cacciapuoti S. Female pattern hair loss: A clinical, pathophysiologic, and therapeutic review // Int J Womens Dermatol. — 2018; 4 (4): 203-211.ссылка
- Jillian Stansbury. Saw Palmetto May Reduce Elevated Androgens and Prolactin in Women with PCOS // Association for the Advancement of Restorative Medicine. — 2016.
- Diri H., Bayram F., Simsek Y., Caliskan Z., Kocer D. Comparison of Finasteride, Metformin, and Finasteride Plus Metformin in PCOS // Acta Endocrinol (Buchar). — 2017; 13 (1): 84-89. ссылка
- Thomas M. M., Houreld N. N. The “in’s and outs” of laser hairremoval: a mini review // J Cosmet Laser Ther. — 2019; 21 (6): 316-322. ссылка
- Robert L. Rosenfieldcorresponding author and David A. Ehrmann The Pathogenesis of Polycystic Ovary Syndrome (PCOS): The Hypothesis of PCOS as Functional Ovarian Hyperandrogenism // Endocr Rev. — 2016; 37 (5): 467–520. ссылка
- Daniel Bubnis. Does Working Out Increase Testosterone Levels?// Healthline. — 2019.
- David J. Handelsman, Angelica L. Hirschberg and Stephane. Circulating Testosterone as the Hormonal Basis of Sex Differences // Athletic Performance Bermon Endocr Rev. — 2018; 39 (5): 803–829.ссылка
- Joanna Igielska Kalwat. The Use of Serenoa Repens (Saw Palmetto) in Hair Care Products // Faculty of Cosmetology and Educational Sciences. — 2018.
Источник https://diseases.medelement.com/material/%D1%80%D1%83%D0%BA%D0%BE%D0%B2%D0%BE%D0%B4%D1%81%D1%82%D0%B2%D0%BE-%D0%BF%D0%BE-%D0%BE%D0%B1%D1%81%D0%BB%D0%B5%D0%B4%D0%BE%D0%B2%D0%B0%D0%BD%D0%B8%D1%8E-%D0%B8-%D0%BB%D0%B5%D1%87%D0%B5%D0%BD%D0%B8%D1%8E-%D0%B3%D0%B8%D1%80%D1%81%D1%83%D1%82%D0%B8%D0%B7%D0%BC%D0%B0-%D1%83-%D0%B6%D0%B5%D0%BD%D1%89%D0%B8%D0%BD-%D0%B2-%D0%BF%D1%80%D0%B5%D0%B4%D0%BA%D0%BB%D0%B8%D0%BC%D0%B0%D0%BA%D1%82%D0%B5%D1%80%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%BE%D0%BC-%D0%BF%D0%B5%D1%80%D0%B8%D0%BE%D0%B4%D0%B5-2018/699518231520646826
Источник https://www.lvrach.ru/2017/03/15436683
Источник https://probolezny.ru/giperandrogeniya/