Ревматоидный артрит
Ревматоидный артрит – тяжелое, с трудом поддающееся лечению заболевание. Причины развития его установлены не полностью, тем не менее, при проведении правильно назначенного комплексного лечения качество жизни пациента может быть вполне удовлетворительным. Но это при условии неукоснительного выполнения больным всех рекомендаций лечащего врача.
Специалисты клиники «Парамита» в Москве имеют большой опыт в лечении ревматоидного артрита.
Что такое ревматоидный артрит
Ревматоидный артрит (РА) – хроническое системное прогрессирующее заболевание, проявляющееся в виде воспаления в основном мелких суставов. Связано оно не с инфекцией, а с поломкой иммунной системы. Поражается соединительная ткань, поэтому данное заболевание называется системным. Патологический процесс часто распространяется и внутренние органы (сердце, сосуды, почки) – это внесуставные проявления болезни.
Всего в мире ревматоидным артритом болеет около 1% населения. Заболеть можно в любом возрасте, но чаще это случается в 35 – 55 лет у женщин и немного позже (в 40 – 60 лет) у мужчин. Ревматоидный артрит у женщины диагностируют в три раза чаще, чем мужчины.
Причины
Точные причины начала данного заболевания не установлены. Но известны основные причинные факторы:
- Наследственная предрасположенность – встречаются случаи семейных заболеваний.
- Влияние внутренних (эндогенных) факторов – у большинства больных женщин и мужчин отмечается низкий уровень мужских половых гормонов; научно подтверждено, что после использования оральных контрацептивов (ОК) риск развития болезни снижается.
- Влияние факторов внешней среды (экзогенных). Возбудители инфекции запускают аутоиммунную реакцию – аллергию на собственные ткани организма. Это связано с тем, что некоторые инфекционные возбудители имеют в составе своих клеток белки, схожие с белками тканей человека. При попадании этих возбудителей в организм иммунная система вырабатывает антитела (IgG), которые по неизвестной науке причине становятся антигенами (чужеродными для организма веществами). На них вырабатываются новые антитела IgM, IgA, IgG (ревматоидные факторы), уничтожающие их. Нарастание количества антител сопровождается усилением воспаления. Некоторые возбудители выделяют вещества, способствующие разрастанию суставной синовиальной оболочки и ферменты, повреждающие ткани.
В результате целого комплекса причин клетки синовиальной оболочки начинают выделять воспалительные цитокины – белковые молекулы, инициирующие и поддерживающие воспаление. Развивается длительно протекающий воспалительный процесс, происходит разрушение хрящевой и костной суставной ткани, деформация конечности. Хрящевая ткань заменяется соединительной, появляются костные разрастания, нарушается функция сустава. Очень часто причиной развивающегося аутоиммунного поражения суставов является герпетическая инфекция – вирусы простого герпеса 1, 2 типа, цитомегаловирус, вирус Эпштейна – Барр (вызывает мононуклеоз) и другие возбудители, например, микоплазмы.
Предрасполагающие (запускающие, триггерные) факторы:
- травмы, заболевания суставов;
- переохлаждения, постоянное пребывание в сыром помещении или в сыром климате;
- нервные перенапряжения, стрессы;
- имеет значение наличие хронических очагов инфекции – тонзиллиты, кариозные зубы, любые инфекционно-воспалительные процессы;
- прием некоторых лекарств с мутагенными свойствами.
Симптомы
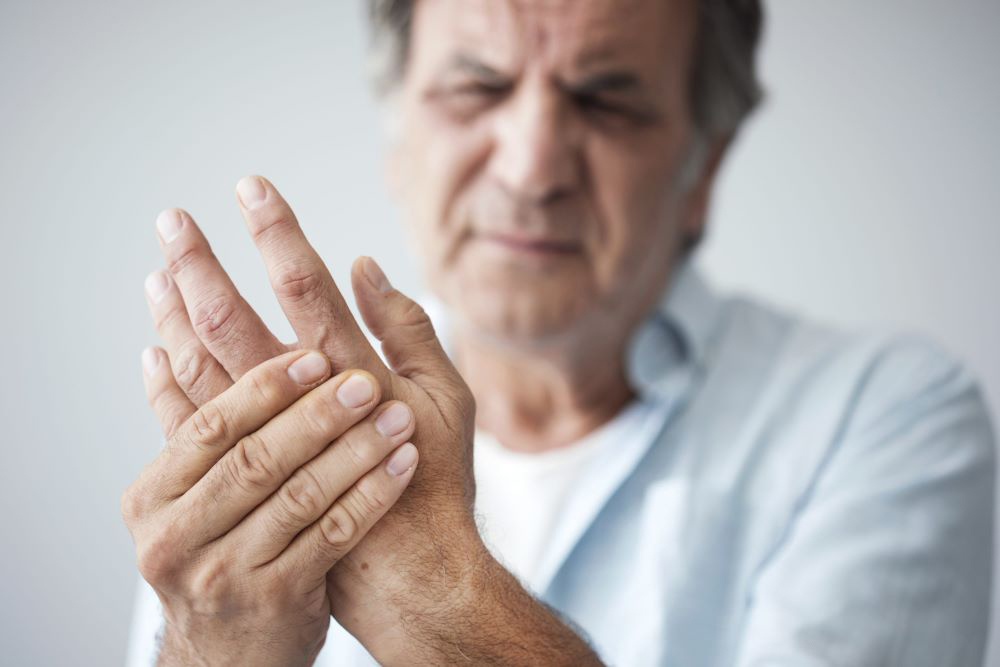
Заболевание протекает волнообразно, в виде периодов обострений (рецидивов) и ремиссий.
Как начинается ревматоидный артрит
Начало в большинстве случаев подострое и имеет связь с перенесенной инфекцией, переохлаждением, травмой или нервным перенапряжением, беременностью, родами.
Один из первых симптомов – появление скованности движений по утрам, которая проходит в течение дня. Иногда это сопровождается небольшой лихорадкой, слабостью, недомоганием.
Одновременно появляются незначительно выраженные боли в пораженных суставах, сначала преходящие, а затем постоянные. Еще один из первых симптомов артрита, на который стоит обратить внимание, — легкая припухлость в суставной области. Она может проходить в течение дня, но затем становится постоянной.
В большинстве случаев при ревматоидном артрите поражается сначала небольшое количество суставов стоп и кистей. На ранней стадии могут также поражаться коленные суставы. Поражения симметричны. При подостром течении первые признаки нарушений появляются через несколько недель, при медленном, хроническом – через несколько месяцев.
Острое начало, высокая активность патологического процесса и системные проявления характерны для ювенильного ревматоидного артрита у детей и подростков. Он может начинаться с высокой температуры, изначального поражения сразу нескольких суставов и признаков поражения внутренних органов.
Симптомы разгара заболевания
Ревматоидный артрит сопровождается признаками общей интоксикации. Это слабость, недомогание, небольшое повышение температуры тела, головные боли. Нарушается аппетит, больной теряет массу тела.
Суставной синдром. Поражаются сначала мелкие суставы кисти (число их увеличивается), а затем и крупные суставы (плечевые, коленные). Они опухают, становятся очень болезненными, постепенно теряют свою функцию, обездвиживаются. Длительное обездвиживание приводит к выраженной атрофии (уменьшению в объеме) мышц. Ревматоидный артрит характеризуется также тем, что поражения разных суставов могут быть неодинаковыми: в одних могут преобладать признаки воспаления (отек), в других – пролиферации (разрастания соединительной ткани с деформацией и нарушением функции).
Появляются подкожные ревматоидные узелки – небольшие, умеренно плотные, безболезненные образования, располагающиеся на поверхности тела, чаще всего на коже локтей.
Поражается периферическая нервная система. Из-за поражения нервов больные ощущают онемение, жжение, зябкость в конечностях.
При ревматоидном васкулите происходит поражение различных мелких и частично средних кровеносных сосудов. Часто это проявляется в виде точечных очагов некроза в области ногтей или безболезненных язв в области голени. Иногда васкулит может проявляться в виде микроинфарктов.
При частых обострениях и прогрессировании ревматоидного артрита происходит поражение внутренних органов — сердца (эндокардит), почек (нефрит), легких (узелковое поражение легочной ткани) и т.д.
Когда нужно срочно обращаться за медицинской помощью
Ревматоидный артрит – тяжелое прогрессирующее заболевание, поэтому важно своевременно провести диагностику и как можно раньше начинать его лечение.
К врачу следует обращаться при появлении следующих симптомов:
- Болей в суставах, легкой скованности движений по утрам, если:
- кто-то из близких родственников болеет ревматоидным артритом;
- вы недавно перенесли какое-то инфекционно-воспалительное заболевание (ОРВИ, ангину), затяжной стресс или просто переохладились;
- вы проживаете в холодной сырой местности.
- Небольшого повышения температуры, недомогания, снижения аппетита, потери массы тела, сопровождающихся легкой утренней скованностью движений.
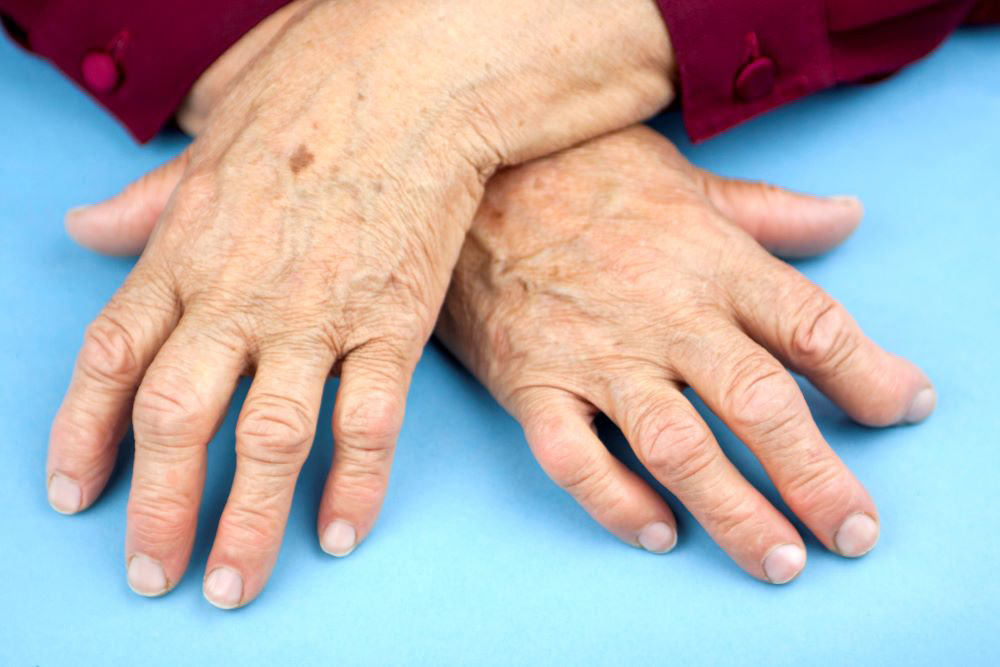
Локализации процесса
При ревматоидном артрите вначале обычно поражаются мелкие суставы кистей, пальцев рук и стоп. Внешний вид верхних х конечностей:
- пальцы кисти деформируются, часто имеют веретенообразную форму, форму «шеи лебедя» или «пуговичной петли»;
- развивается подвывих пястно-фаланговых суставов кисти, отчего она приобретает форму «плавника моржа»;
- при поражении локтевых суставов появляется их сгибательная контрактура (неподвижность);
- в области локтей можно прощупать небольшие безболезненные ревматоидные узелки;
- плечевой сустав обычно поражается вторично, при прогрессировании болезни появляется его припухлость, болезненность, усиливающиеся при движении.
Подробнее про артрит суставов пальцев читайте здесь.
Хруст в суставах — когда стоит беспокоиться
Внутрисуставные инъекции гиалуроновой кислоты
Внешний вид нижних конечностей:
- пальцы стоп приобретают молоточковидную форму;
- подвывихи мелких суставов приводят к развитию плоскостопия;
- для ревматоидной стопы характерно также вальгусное (кнаружи) отклонение стопы, связанное с поражением голеностопа;
- при поражении коленных суставов появляется сгибательная контрактура (неподвижность).
Тазобедренные суставы поражаются редко.
Стадии ревматоидного артрита
Ревматоидный артрит протекает в три стадии:
- Начальная, воспаления– поражение синовиальных сумок сопровождается болями, отеком околосуставных тканей.
- Прогрессирующая, пролиферации – быстрое деление клеток синовиальной оболочки, приводящее к ее уплотнению.
- Завершающая, деформации – при длительном течении воспаленные клетки начинают выделять фермент, разрушающий хрящевую и костную ткань, что приводит к изменению суставной формы и тяжелому нарушению их функции.
По длительности течения выделяют следующие стадии ревматоидного артрита:
- очень ранняя – до полугода;
- ранняя – от полугода до года;
- развернутая – до 2-х лет;
- поздняя – после 2-х лет.
- Околосуставной остеопороз – разрежение, истончение костной ткани;
- Сужение суставной щели и единичные эрозии на хрящевой суставной поверхности;
- Множественные глубокие эрозии суставных хрящей и костей;
- Присоединяется анкилоз — неподвижность сустава из-за сращения суставных поверхностей.
Стадии ревматоидного артрита
Существует несколько типов классификаций ревматоидного артрита по разным критериям.
По клинико-анатомическим признакам выделяют следующие формы ревматоидного артрита:
- суставная форма;
- суставно-висцеральная (системная) – поражаются не только суставы, но и внутренние органы;
- ювенильная форма – развивается у детей до 16 лет, характеризуется острым началом, лихорадкой и выраженными внесуставными проявлениями.
Любая форма артрита имеет серьезные осложнения, поэтому не стоит затягивать с лечением.
- медленнопрогрессирующий РА – самая частая форма, может продолжаться годами;
- быстропрогрессирующий РА – характеризуется злокачественным течением;
- без признаков прогрессирования – встречается редко.
По иммунологическим признакам:
- Наличие или отсутствие содержания в крови ревматоидного фактора (РФ) – антител к собственному иммуноглобулину G:
- серопозитивные – РФ обнаружен;
- серонегативные – РФ не обнаружен.
- Наличие или отсутствие в крови антител к циклическому цитрулинсодержащему пептиду – анти-ЦЦП или АЦЦП (цитрулин – продукт обмена, в норме полностью выводящийся из организма; при РА выделяются ферменты, встраивающие цитрулин в белки и превращающие его в чужеродный белок – антиген; на этот антиген иммунная система вырабатывает антитела):
- серопозитивные – АЦЦП обнаружен;
- серонегативные – АЦЦП не обнаружен.
Выделяют следующие критерии сохранности функций опорно-двигательного аппарата:
- Выполнение движений в полном объеме.
- Снижение двигательной активности. Появляются трудности, не позволяющие выполнять движения в полном объеме, особенно в профессиональной сфере.
- Нарушение подвижности, возможно только самообслуживание.
- Невозможны любые виды двигательной активности, в том числе самообслуживание.
Что будет, если не лечить
Если ревматоидный артрит не начать лечить своевременно, в дальнейшем он начнет быстро прогрессировать, что увеличивает риск развития возможных осложнений:
- деформации и утрата суставных функций, приводящие к инвалидности;
- изменению нервно-мышечной системы с нейропатиями и уменьшением объема мышц;
- поражению сердечно-сосудистой системы в виде васкулитов, эндокардитов, микроинфарктов;
- нарушениям со стороны почек с постепенным формированием хронической почечной недостаточности;
- поражениям органов зрения, в том числе язвенного характера;
- поражению плевры и легких — развитию плеврита и интерстициальной пневмонии;
- развитию анемии и системных тромбозов мелких кровеносных сосудов.
Диагностика
Диагноз ревматоидного артрита подтверждается данными дополнительного обследования. Диагностика ревматоидного артрита включает:
- Лабораторные исследования:
- общий анализ крови – выявляет воспалительный процесс (ускоряется СОЭ, изменяется число лейкоцитов);
- биохимия – позволяет уточнить причины воспаления и нарушения обменных процессов;
- иммунологические исследования – наличие или отсутствие специфических антител.
- Инструментальные исследования:
- рентгендиагностика – выявляет патологию суставов;
- компьютерная и магнитно-резонансная томография (КТ, МРТ) – позволяют провести оценку ранних суставных изменений;
- УЗИ – выявляет увеличение объема суставной жидкости и наличие участков некроза.
Как лечат ревматоидный артрит
Лечение ревматоидного артрита начинается с устранения воспаления и боли. Затем присоединяется комплексное лечение:
- диета;
- медикаментозная терапия (базисное лечение);
- средства народной медицины;
- физиотерапевтические процедуры;
- лечебная гимнастика и массаж;
- новые методики;
- хирургические методы лечения.
Диета
Питание при ревматоидном артрите должно быть регулярным и полноценным. В суточном рационе должны присутствовать продукты, богатые кальцием (творог, сыр, кефир), овощи, фрукты, овощные супы, нежирное мясо и рыба.
Из рациона должны быть исключены: концентрированные бульоны, овощи, богатые эфирными маслами (свежий лук, чеснок, редис), жирные, копченые, консервированные продукты, сладости, сдоба, сладкие газированные напитки. Должен быть полностью исключен прием алкоголя.
Медикаментозное лечение
Это индивидуально подобранная терапия, включающая в себя применение нестероидных противовоспалительных препаратов (НПВП), глюкокортикоидных средств (ГКС), базисных препаратов и биологических агентов.
Чтобы облегчить состояние больного, лечение начинают с назначения НПВП. Современные лекарственные препараты этого ряда (нимесулид, целекоксиб, мелоксикам) снимают воспаление и боль в суставах, не вызывая выраженных побочных явлений, характерных для ранних НПВП (диклофенака и др.).
Если воспаление и боль носят выраженный характер и НПВП не помогают, назначают глюкокортикоидные гормоны (ГКС — преднизалон, дексаметазон, триамсинолон). Они быстро снимают отек, боль, устраняют повышенное содержание синовиальной жидкости, но имеют много побочных эффектов, поэтому их стараются назначать короткими курсами. Препараты этой группы назначают также для того, чтобы подавить разрастание синовиальной оболочки сустава. Иногда ГКС вводят в суставную полость. При сильных болях и воспалении ГКС назначают в виде пульс-терапии: внутривенно большими дозами на протяжении не более трех дней.
При тяжелом течении ревматоидного артрита назначают плазмаферез – очищение крови от антител. С этой же целью назначают сорбенты, например, Энтеросгель, очищающий организм от токсинов.
Препараты базисной терапии подавляют аутоиммунный воспалительный процесс и пролиферацию (размножение) клеток соединительной ткани, оказывающих разрушающее действие на суставы. Базисные средства действуют медленно, поэтому их назначают длительными курсами и подбирают индивидуально. Эффективные, проверенные временем базисные препараты метотрексат, сульфасалазин и лефлуномид (Арава). Последний препарат относится к новому поколению и имеет меньше побочных эффектов.
В последнее время для лечения ревматоидного артрита стали применять биологические агенты – антитела, цитокины и другие активные вещества, играющие значительную роль в иммунных реакциях. Одним из таких препаратов является ритуксимаб (Мабтера, Реддитукс). Активным действующим веществом препарата являются антитела мыши и человека, которые подавляют иммунные реакции. Назначение этого препарата позволяет реже назначать курсы комплексной медикаментозной терапии.
Лечение ревматоидного артрита средствами народной медицины
Народные средства можно включать в состав комплексного лечения ревматоидного артрита, но назначать их должны только врачи, так как эти средства чаще всего имеют растительное происхождение, могут вызывать аллергические реакции и усугублять течение аутоиммунных процессов.
Народные средства при ревматоидном артрите применяют в основном наружно. Вот некоторые из них:
- кору вяза высушить, растереть в порошок, развести водой, разложить на салфетке над пораженной поверхностью в виде компресса на всю ночь; хорошо лечатся воспаление и боль;
- спиртовые растирания с экстрактами растений (корня лопуха, хмеля, цветков одуванчика, чабреца); в стеклянную банку помещают измельченные растения, заливают водкой, настаивают в темном месте 10 дней и используют как растирание.
Физиотерапевтические процедуры, лечебная гимнастика, массаж
Физиотерапевтические процедуры помогают быстрее избавить больного от воспаления и боли. С этой целью назначают:
- электрофорез с диклофенаком;
- фонофорез с дексаметазоном;
- аппликации с димексидом.
Хондропротекторы что это как выбрать, насколько они эффективны
Образ жизни при ревматоидном артрите
Ревматоидный артрит-серьезное хроническое заболевание, протекающее с периодами обострений, ремиссии. Обострение может протекать тяжело, с сильными болями и ограничением движений. Обострение ухудшает общее состояние больного и приводит к ограничению трудоспособности. Периоды ремиссии могут быть как продолжительными, так и ограниченными по времени. В этот период явления воспаления могут стихать, или присутствовать незначительно.
Социальная значимость ревматоидного артрита высока, вследствие высоких показателей нетрудоспособности и инвалидизации. А страдает данным заболеванием примерно 1-2% населения земного шара. Женщины болеют в 1,5-2 раза чаще мужчин. Болезнь может начаться в любом возрасте, но чаще после 40 лет. Поэтому проблема ревматоидного артрита крайне актуальна. Сегодня мы не будем рассматривать методы его трудного лечения в период обострения, а изучим возможности продлить ремиссию, как правильно организовать жизнь и быть активным даже с таким диагнозом.

На приеме у врача
Особенности питания при ревматоидном артрите
Питание при ревматоидном артрите имеет лечебное значение. На разной стадии заболевания диета подбирается индивидуально. Но существуют и общие рекомендации. Принципы составления диеты основаны на:
- восстановлении оптимальной массы тела,
- выведении токсинов,
- избавлении организма от излишней жидкости.
Желательно не употреблять, даже в умеренном количестве, следующие продукты:
- отдельные виды орехов, особенно арахис и миндаль,
- жирные сорта рыб,
- свинину,
- колбасу и колбасные изделия,
- коровье молоко,
- мюсли,
- цитрусовые и фрукты и овощи оранжевой окраски,
- сдобные изделия,мед,мороженое, варенье,
- кетчупы, соусы,
- маринованные продукты,
- острую пищу,
- крепкий чай и кофе,
- необходимо ограничить соль,
- пищу с повышенной кислотностью: щавель, шпинат, сельдерей,
- необходимо употреблять ограниченно:баклажаны, картофель, помидоры,
- газированные напитки и алкоголь исключаются.

Приготовление пищи предпочтительно на пару, или в отварном виде. При этом количество приемов ее 5-6 раз в день.
Что же необходимо включать в рацион: очень приветствуется рыба морская, или речная, но только нежирных сортов; из мясных продуктов лучше употреблять птицу, кролика, не мороженную телятину. Не рекомендуются мясные супы, лучше овощные. Масла лучше употреблятьрастительные:подсолнечное, оливковое, кукурузное.
Не рекомендуются консервы и консервированные соки, но свежевыжатые соки употреблять можно, так же как свежеприготовленные морсы,компоты. Рекомендованы крупы в виде каш- овсяная,гречневая, пшенная, рисовая, перловая, кукурузная. А самое главное, много овощей, свежих и приготовленных; зелень,фрукты, ягоды,семечки. В период обострения нужна низкокалорийная диета, максимальное число калорий-1800; белки ограничиваются до 80 г. в день.Потребление жиров ограничено 70 г. Употребление жидкости -1 л в день.
Диета в период ремиссии такова( стол № 10): белки -100 г, некрепкий чай и кофе ( с лимоном, сливками), продукты с повышенным содержанием витамина D, кальция, фосфора.
Лечебная физкультура
Физические упражнения разрешаются пациенту только после стихания острой фазы процесса. Начинать нужно с простейших движений в суставах: сгибания- разгибания, движения вверх- вниз и в стороны. Но делать эти упражнения необходимо 3-4 раза в день по 30-40 минут. Гимнастика допустима активная и пассивная. Движения стимулируют улучшение обмена веществ, восстановление связочного и мышечного аппарата, уменьшают отложения солей .Далее, после некоторого восстановления движений, можно и нужно заниматься йогой, плаванием. Занятия йогой приводят в равновесие внутренние энергии организма, циркуляция жидкостей выводит токсины.

Поддерживающая терапия в период ремиссии
Лечение и профилактику обострений в период ремиссии можно проводить в домашних условиях, можно получить санаторно-курортное лечение. Роль лечебной гимнастики в этот период усиливается, движения необходимо максимально восстановить. Так как в острую фазу процесса произошло уменьшение суставной жидкости и изменилось ее качество (она стала содержать элементы воспаления, раздражающие ткани), необходимо в первую очередь восстановить ее количество и состав. Если не провести этого лечения, то, при нагрузке во время гимнастики, участки костей будут травмироваться. И это может спровоцировать новое обострение.
Лечение в этом периоде проводится в виде внутрисуставной инъекции с введением в полость сустава заменителей синовиальной жидкости. Препарат вводится , как правило, однократно, в клинике, в условиях асептики и антисептики. После местного обезболивания лекарство вводится в полость сустава.
Выбор препарата для эндопротезирования
Заменители синовиальной жидкости имеют разные характеристики.
Первая группа препаратов производится на основе гиалуроновой кислоты, вторая- синтетические вещества- биополимеры.
Вещества первой группы, гиалуронаты, вырабатываются из животного сырья, поэтому сродни организму, схожи по вязкости, но есть и неприятные последствия. Органическое вещество легко разрушается ферментами организма., поэтому долго не сохраняется. Лучшие препараты этой группы сохраняются в суставе от полугода до года. Кроме того, препараты животного происхождения могут вызывать аллергические реакции. Их не стоит применять у пациентов с другими видами аллергии.
Вторая группа препаратов- синтетическая, представляет собой длинные молекулы полимеров. Они интактны, не разрушаются ферментами, не отторгаются и не вызывают аллергических реакций. Именно поэтому находятся в организме гораздо дольше ( от года до трех лет). Вязкий биополимер заполняет суставную полость и дает возможность человеку активно и безболезненно двигаться, заниматься лечебной физкультурой, разрабатывать поврежденные болезнью суставы.Такой синтетический полимер, как Нолтрекс, содержит в составе еще и активные ионы серебра, значительно уменьшающие воспалительные изменения в суставе.
Итак, несмотря на развитие медицины, ревматоидный артрит не имеет выясненной причины возникновения, нет единого метода лечения и профилактики. Однако, соблюдение описанных требований помогает улучшить состояние больного, избежать, или уменьшить число рецидивов. При этом, конечно, нужно укреплять общее состояние организма, иммунитет, избавиться от вредных привычек, контролировать массу тела, своевременно санировать инфекционные очаги организма и наблюдаться врачом. В этом случае возможна достаточно комфортная и мобильная жизнь пациента.
Современная медикаментозная терапия ревматоидного артрита

Ревматоидный артрит — это заболевание, находящееся в фокусе внимания ревматологов всего мира в течение десятилетий. Это связано с большим медицинским и социальным значением этой болезни. Ее распространенность достигает
#02/07 Ключевые слова / keywords: Ревматология, Rheumatology
2007-02-26 00:00
1018210 прочтений
Ревматоидный артрит — это заболевание, находящееся в фокусе внимания ревматологов всего мира в течение десятилетий. Это связано с большим медицинским и социальным значением этой болезни. Ее распространенность достигает 0,5–2% от общей численности населения в промышленно развитых странах [1, 2]. У больных ревматоидным артритом наблюдается уменьшение продолжительности жизни по сравнению с общей популяцией на 3–7 лет [3]. Трудно переоценить колоссальный ущерб, наносимый этим заболеванием обществу за счет ранней инвалидизации пациентов, которая при отсутствии своевременно начатой активной терапии может наступать в первые 5 лет от дебюта болезни.
Ревматоидный артрит — хроническое воспалительное заболевание неясной этиологии, для которого характерно поражение периферических синовиальных суставов и периартикулярных тканей, сопровождающееся аутоиммунными нарушениями и способное приводить к деструкции суставного хряща и кости, а также к системным воспалительным изменениям.
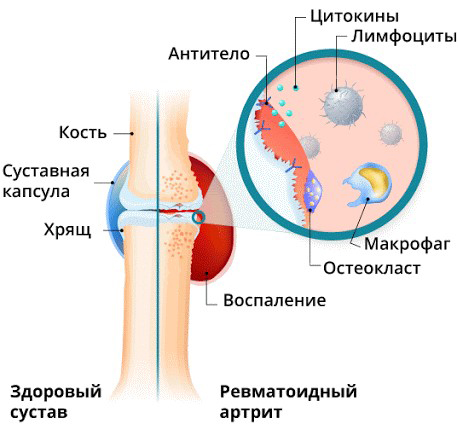
Патогенез заболевания весьма сложен и во многом недостаточно изучен. Несмотря на это, к настоящему времени хорошо известны некоторые ключевые моменты в развитии ревматоидного воспаления, которые определяют основные методы лечебного воздействия на него (рис. 1). Развитие хронического воспаления в данном случае связано с активацией и пролиферацией иммунокомпетентных клеток (макрофагов, Т- и В-лимфоцитов), что сопровождается выделением клеточных медиаторов — цитокинов, факторов роста, молекул адгезии, а также синтезом аутоантител (например, антицитруллиновых антител) и формированием иммунных комплексов (ревматоидные факторы). Эти процессы ведут к формированию новых капиллярных сосудов (ангиогенез) и разрастанию соединительной ткани в синовиальной оболочке, к активации циклооксигеназы-2 (ЦОГ-2) с повышением синтеза простагландинов и развитием воспалительной реакции, к выделению протеолитических ферментов, активации остеокластов, а в результате — к деструкции нормальных тканей суставов и возникновению деформаций.
Лечение ревматоидного артрита
- медикаментозную терапию;
- немедикаментозные методы терапии;
- ортопедическое лечение, реабилитацию.
Исходя из патогенеза заболевания, становится очевидным, что эффективно воздействовать на развитие заболевания можно на двух уровнях:
- подавляя избыточную активность иммунной системы;
- блокируя выработку медиаторов воспаления, в первую очередь простагландинов.
Поскольку, помимо собственно воспаления, активация иммунной системы сопровождается многими другими патологическими процессами, воздействие на первом уровне является существенно более глубоким и эффективным, нежели на втором. Медикаментозная иммуносупрессия представляет собой основу лечения ревматоидного артрита. К иммуносупрессорам, применяющимся для лечения данного заболевания, относятся базисные противовоспалительные препараты (БПВП), биологические препараты и глюкокортикостероиды. На втором уровне действуют нестероидные противовоспалительные препараты (НПВП) и глюкокортикостероиды.
В целом иммуносупрессивная терапия сопровождается более медленным развитием клинического эффекта (в широких рамках — от нескольких дней в случае биологической терапии до нескольких месяцев в случае применения некоторых БПВП), который в то же время бывает очень выраженным (вплоть до развития клинической ремиссии) и стойким, а также характеризуется торможением деструкции суставов.
Собственно противовоспалительная терапия (НПВП) может давать клинический эффект (обезболивание, уменьшение скованности) очень быстро — в течение 1–2 ч, однако при помощи такого лечения практически невозможно полностью купировать симптоматику при активном ревматоидном артрите и, по-видимому, оно совсем не влияет на развитие деструктивных процессов в тканях.
Глюкокортикостероиды обладают как иммуносупрессивным, так и непосредственным противовоспалительным эффектом, поэтому клиническое улучшение может развиваться быстро (в течение нескольких часов при внутривенном или внутрисуставном введении). Имеются данные о подавлении прогрессирования эрозивного процесса в суставах при длительной терапии низкими дозами глюкокортикостероидов и о положительном их влиянии на функциональный статус больного. В то же время из практики хорошо известно, что назначение только глюкокортикостероидов, без других иммуносупрессивных средств (БПВП), редко дает возможность достаточно эффективно контролировать течение болезни.
Немедикаментозные способы терапии ревматоидного артрита (физиотерапия, бальнеотерапия, диетотерапия, акупунктура и др.) представляют собой дополнительные методики, с помощью которых можно несколько улучшить самочувствие и функциональный статус пациента, но не купировать симптоматику и достоверно повлиять на деструкцию суставов.
Ортопедическое лечение, включающее ортезирование и хирургическую коррекцию деформаций суставов, а также реабилитационные мероприятия (лечебная физкультура и др.) имеют особое значение преимущественно на поздних стадиях заболевания для поддержания функциональной способности и улучшения качества жизни больного.
Основными целями лечения при РА являются [2, 6]:
- купирование симптомов заболевания, достижение клинической ремиссии или как минимум низкой активности болезни;
- торможение прогрессирования структурных изменений в суставах и соответствующих функциональных нарушений;
- улучшение качества жизни больных, сохранение трудоспособности.
Надо иметь в виду, что цели лечения могут существенно изменяться в зависимости от длительности болезни. На ранней стадии болезни, т. е. при длительности болезни 6–12 мес, достижение клинической ремиссии — вполне реальная задача, так же как и торможение развития эрозий в суставах. С помощью современных методов активной медикаментозной терапии удается добиться ремиссии у 40–50% пациентов [4, 5], показано также отсутствие появления новых эрозий по данным рентгенографии [7] и магнитно-резонансной томографии [8] у значительного количества больных при длительности наблюдения 1–2 года.
При длительно текущем ревматоидном артрите, особенно при недостаточно активной терапии в первые годы заболевания, достижение полной ремиссии теоретически тоже возможно, однако вероятность этого значительно ниже. То же самое можно сказать и о возможности остановить прогрессирование деструкции в суставах, уже существенно разрушенных за несколько лет болезни. Поэтому при далеко зашедшем ревматоидном артрите возрастает роль реабилитационных мероприятий, ортопедической хирургии. Кроме того, на поздних стадиях заболевания длительная поддерживающая базисная терапия может использоваться для вторичной профилактики осложнений болезни, таких как системные проявления (васкулит и др.), вторичный амилоидоз.
Базисная терапия ревматоидного артрита. БПВП (синонимы: базисные препараты, болезнь-модифицирующие антиревматические препараты, медленно действующие препараты) являются главным компонентом лечения ревматоидного артрита и при отсутствии противопоказаний должны быть назначены каждому пациенту с этим диагнозом [9]. Особенно важно максимально быстрое назначение БПВП (сразу после установления диагноза) на ранней стадии, когда имеется ограниченный период времени (несколько месяцев от появления симптоматики) для достижения наилучших отдаленных результатов — так называемое «терапевтическое окно» [10].
Классические БПВП обладают следующими свойствами.
- Способность подавлять активность и пролиферацию иммунокомпетентных клеток (иммуносупрессия), а также пролиферацию синовиоцитов и фибробластов, что сопровождается выраженным снижением клинико-лабораторной активности РА.
- Стойкость клинического эффекта, в том числе его сохранение после отмены препарата.
- Способность задерживать развитие эрозивного процесса в суставах.
- Способность индуцировать клиническую ремиссию.
- Медленное развитие клинически значимого эффекта (обычно в течение 1–3 мес от начала лечения).
БПВП существенно различаются между собой по механизму действия и особенностям применения. Основные параметры, характеризующие БПВП, представлены в таблице 1.
БПВП условно могут быть подразделены на препараты первого и второго ряда. Препараты первого ряда обладают наилучшим соотношением эффективности (достоверно подавляют как клиническую симптоматику, так и прогрессирование эрозивного процесса в суставах) и переносимости, в связи с чем назначаются большинству пациентов.
К БПВП первого ряда относятся следующие.
- Метотрексат — «золотой стандарт» терапии ревматоидного артрита. Рекомендуемые дозы — 7,5–25 мг в неделю — подбираются индивидуально путем постепенного повышения на 2,5 мг каждые 2–4 нед до достижения хорошего клинического ответа либо возникновения непереносимости. Препарат дается внутрь (еженедельно в течение двух последовательных дней дробно в 3–4 приема каждые 12 ч). В случае неудовлетворительной переносимости метотрексата при приеме внутрь за счет диспепсии и других жалоб, связанных с желудочно-кишечным трактом (ЖКТ), препарат может быть назначен парентерально (одна в/м или в/в инъекция в неделю).
- Лефлуномид (арава). Стандартная схема лечения: внутрь по 100 мг в сутки в течение 3 дней, затем 20 мг/сут постоянно. При риске непереносимости препарата (пожилой возраст, заболевания печени и др.) лечение можно начинать с дозы 20 мг/сут. По эффективности сопоставим с метотрексатом, имеет несколько лучшую переносимость. Есть данные о более высокой эффективности лефлуномида в отношении качества жизни больных, особенно при раннем ревматоидном артрите. Стоимость лечения лефлуномидом достаточно высока, поэтому он чаще назначается при наличии противопоказаний к применению метотрексата, его неэффективности или непереносимости, однако может использоваться и как первый базисный препарат.
- Сульфасалазин. В клинических испытаниях не уступал по эффективности другим БПВП, однако клиническая практика показывает, что достаточный контроль над течением болезни сульфасалазин обычно обеспечивает при умеренной и низкой активности ревматоидного артрита.
БПВП второго ряда применяются значительно реже в связи с меньшей клинической эффективностью и/или большей токсичностью. Они назначаются, как правило, при неэффективности или непереносимости БПВП первого ряда.
БПВП способны вызвать значительное улучшение (хороший клинический ответ) приблизительно у 60% пациентов. В связи с медленным развитием клинического эффекта назначение БПВП на сроки менее 6 мес не рекомендуется. Длительность лечения определяется индивидуально, типичная продолжительность «курса» лечения одним препаратом (в случае удовлетворительного ответа на терапию) составляет 2–3 года и более. Большинство клинических рекомендаций подразумевают неопределенно долгое применение поддерживающих дозировок БПВП для сохранения достигнутого улучшения.
При недостаточной эффективности монотерапии каким-либо базисным препаратом может быть избрана схема комбинированной базисной терапии, т. е. сочетания двух-трех БПВП. Наиболее хорошо зарекомендовали себя следующие сочетания:
- метотрексат + лефлуномид;
- метотрексат + циклоспорин;
- метотрексат + сульфасалазин;
- метотрексат + сульфасалазин + гидроксихлорохин.
В комбинированных схемах препараты обычно применяются в средних дозировках. В ряде клинических исследований было продемонстрировано превосходство комбинированной базисной терапии над монотерапией, однако более высокая эффективность комбинированных схем не считается строго доказанной. Комбинация БПВП ассоциирована с умеренным повышением частоты побочных эффектов.
Биологические препараты в лечении ревматоидного артрита. Термин биологические препараты (от англ. biologics) применяется по отношению к лекарственным средствам, производимым с использованием биотехнологий и осуществляющим целенаправленное («точечное») блокирование ключевых моментов воспаления с помощью антител или растворимых рецепторов к цитокинам, а также другим биологически активным молекулам. Таким образом, биологические препараты не имеют никакого отношения к «биологически активным пищевым добавкам». В связи с большим количеством «молекул-мишеней», воздействие на которые потенциально может подавлять иммунное воспаление, разработан целый ряд лекарственных средств из этой группы и еще несколько препаратов проходят клинические испытания.
К основным зарегистрированным в мире для лечения ревматоидного артрита биологическим препаратам относятся:
- инфликсимаб, адалимумаб, этанерсепт (воздействуют на фактор некроза опухоли (ФНО-α);
- ритуксимаб (воздействует на CD 20 (В-лимфоциты));
- анакинра (воздействует на интерлейкин-1);
- абатасепт (воздействует на CD 80, CD 86, CD 28).
Для биологических препаратов характерны выраженный клинический эффект и достоверно доказанное торможение деструкции суставов. Эти признаки позволяют относить биологические препараты к группе БПВП. В то же время особенностью группы является быстрое (нередко в течение нескольких дней) развитие яркого улучшения, что объединяет биологическую терапию с методами интенсивной терапии. Характерная черта биологических средств — потенцирование эффекта в сочетании с БПВП, в первую очередь с метотрексатом. В связи с высокой эффективностью при ревматоидном артрите, в том числе у резистентных к обычной терапии пациентов, в настоящее время биологическая терапия выдвинулась на второе по значимости место (после БПВП) в лечении этого заболевания.
К отрицательным сторонам биологической терапии относятся:
- угнетение противоинфекционного и (потенциально) противоопухолевого иммунитета;
- риск развития аллергических реакций и индуцирования аутоиммунных синдромов, связанный с тем, что биологические препараты по химической структуре являются белками;
- высокая стоимость лечения.
Биологические методы терапии показаны, если лечение препаратами из группы БПВП (такими, как метотрексат) не является адекватным вследствие недостаточной эффективности или неудовлетворительной переносимости.
Одной из наиболее важных молекул-мишеней служит ФНО-a, который имеет множество провоспалительных биологических эффектов и способствуют персистенции воспалительного процесса в синовиальной оболочке, деструкции хряща и костной ткани за счет прямого действия на синовиальные фибробласты, хондроциты и остеокласты. Блокаторы ФНО-α являются наиболее широко применяемыми биологическими средствами в мире.
В России зарегистрирован препарат из этой группы инфликсимаб (ремикейд), представляющий собой химерное моноклональное антитело к ФНО-α. Препарат, как правило, назначается в сочетании с метотрексатом. У пациентов с недостаточной эффективностью терапии средними и высокими дозами метотрексата инфликсимаб существенно улучшает ответ на лечение и функциональные показатели, а также приводит к выраженному торможению прогрессирования сужения суставной щели и развития эрозивного процесса.
Показанием к назначению инфликсимаба в комбинации с метотрексатом является неэффективность одного или более БПВП, применявшихся в полной дозе (в первую очередь метотрексата), с сохранением высокой воспалительной активности (пять и более припухших суставов, скорость оседания эритроцитов (СОЭ) более 30 мм/ч, С-реактивный белок (СРБ) более 20 мг/л). При раннем ревматоидном артрите с высокой воспалительной активностью и быстрым нарастанием структурных нарушений в суставах комбинированная терапия метотрексатом и инфликсимабом может быть назначена сразу.
До назначения инфликсимаба требуется провести скрининговое обследование на туберкулез (рентгенография грудной клетки, туберкулиновая проба). Рекомендуемая схема применения: начальная доза 3 мг/кг массы тела больного в/в капельно, затем по 3 мг/кг массы тела через 2, 6 и 8 нед, далее по 3 мг/кг массы тела каждые 8 нед, при недостаточной эффективности доза может повышаться вплоть до 10 мг/кг массы тела. Длительность лечения определяется индивидуально, обычно не менее 1 года. После отмены инфликсимаба поддерживающая терапия метотрексатом продолжается. Следует иметь в виду, что повторное назначение инфликсимаба после окончания курса лечения этим препаратом ассоциировано с повышенной вероятностью реакций гиперчувствительности замедленного типа.
Вторым зарегистрированным в нашей стране препаратом для проведения биологической терапии является ритуксимаб (мабтера). Действие ритуксимаба направлено на подавление В-лимфоцитов, которые не только являются ключевыми клетками, отвечающими за синтез аутоантител, но и выполняют важные регуляторные функции на ранних стадиях иммунных реакций. Препарат обладает выраженной клинической эффективностью, в том числе у больных, недостаточно отвечающих на терапию инфликсимабом.
Для лечения ревматоидного артрита препарат применяется в дозе 2000 мг на курс (две инфузии по 1000 мг, каждая с промежутком в 2 нед). Ритуксимаб вводится внутривенно медленно, рекомендуется проведение инфузии в условиях стационара с возможностью точного контроля за скоростью введения. Для профилактики инфузионных реакций целесообразно предварительное введение метилпреднизолона 100 мг. При необходимости возможно проведение повторного курса инфузий ритуксимаба через 6–12 мес.
Согласно европейским клиническим рекомендациям, ритуксимаб целесообразно назначать в случаях неэффективности или невозможности проведения терапии инфликсимабом. Возможность применения ритуксимаба в качестве первого биологического препарата служит в настоящее время предметом исследований.
Глюкокортикостероиды. Глюкокортикостероиды обладают многогранным противовоспалительным действием, обусловленным блокадой синтеза провоспалительных цитокинов и простагландинов, а также торможением пролиферации за счет воздействия на генетический аппарат клеток. Глюкокортикостероиды оказывают быстрый и ярко выраженный дозозависимый эффект в отношении клинических и лабораторных проявлений воспаления. Применение глюкокортикостероидов чревато развитием нежелательных реакций, частота которых также повышается с увеличением дозы препарата (стероидный остеопороз, медикаментозный синдром Иценко–Кушинга, поражение слизистой ЖКТ). Эти препараты сами по себе в большинстве случаев не могут обеспечить полноценного контроля над течением ревматоидного артрита и должны назначаться вместе с БПВП.
Глюкокортикостероиды при данном заболевании применяются системно и локально. Для системного применения показан основной метод лечения — назначение низких доз внутрь (преднизолон — до 10 мг/сут, метилпреднизолон — до 8 мг/сут) на длительный период при высокой воспалительной активности, полиартикулярном поражении, недостаточной эффективности БПВП.
Средние и высокие дозы глюкокортикостероидов внутрь (15 мг/сут и более, обычно 30–40 мг/сут в пересчете на преднизолон), а также пульс-терапия глюкокортикостероидами — внутривенное введение высоких доз метилпреднизолона (250–1000 мг) или дексаметазона (40–120 мг) могут применяться для лечения тяжелых системных проявлений ревматоидного артрита (выпотной серозит, гемолитическая анемия, кожный васкулит, лихорадка и др.), а также некоторых особых форм болезни. Продолжительность лечения определяется временем, необходимым для купирования симптоматики, и составляет обычно 4–6 нед, после чего осуществляется постепенное ступенчатое снижение дозы с переходом на лечение низкими дозами глюкокортикостероидов.
Глюкокортикостероиды в средних и высоких дозах, пульс-терапия, по-видимому, не обладают самостоятельным влиянием на течение ревматоидного артрита и развитие эрозивного процесса в суставах.
Для локальной терапии применяются препараты в микрокристаллической форме, назначающиеся в виде внутрисуставных и периартикулярных инъекций: бетаметазон, триамсинолон, метилпреднизолон, гидрокортизон.
Глюкокортикостероиды для локального применения обладают ярко выраженным противовоспалительным действием, преимущественно в месте введения, а в ряде случаев — и системным действием. Рекомендуемые суточные дозы составляют: 7 мг — для бетаметазона, 40 мг — для триамсинолона и метилпреднизолона, 125 мг — для гидрокортизона. Эта доза (суммарно) может использоваться для внутрисуставного введения в один крупный (коленный) сустав, два сустава среднего размера (локтевые, голеностопные и др.), 4–5 мелких суставов (пястно-фаланговые и др.), либо для периартикулярного введения препарата в 3–4 точки.
Эффект после однократного введения обычно наступает на протяжении 1–3 дней и сохраняется в течение 2–4 нед при хорошей переносимости.
В связи с этим повторные инъекции глюкокортикостероидов в один сустав нецелесообразно назначать ранее чем через 3–4 недели. Проведение курса из нескольких внутрисуставных инъекций в один и тот же сустав не имеет терапевтического смысла и чревато осложнениями (локальный остеопороз, усиление деструкции хряща, остеонекроз, нагноение). В связи с повышенным риском развития остеонекроза внутрисуставное введение глюкокортикостероидов в тазобедренный сустав в целом не рекомендуется.
Глюкокортикостероиды для локального применения назначаются в качестве дополнительного метода купирования обострений ревматоидного артрита и не могут служить заменой системной терапии.
НПВП. Значение НПВП в лечении ревматоидного артрита за последние годы существенно снизилось в связи с появлением новых эффективных схем патогенетической терапии. Противовоспалительное действие НПВП достигается с помощью подавления активности ЦОГ, или избирательно ЦОГ-2, и тем самым снижается синтез простагландинов. Таким образом НПВП действуют на конечное звено ревматоидного воспаления.
Действие НПВП при ревматоидном артрите — уменьшение выраженности симптомов болезни (боль, скованность, припухлость суставов). НПВП обладают обезболивающим, противовоспалительным, жаропонижающим эффектом, но мало влияют на лабораторные показатели воспаления. В подавляющем большинстве случаев НПВП не способны как-либо заметно изменить течение заболевания. Их назначение в качестве единственного противоревматического средства при достоверном диагнозе ревматоидный артрит в настоящее время считается ошибкой. Тем не менее НПВП являются основным средством симптоматической терапии при данном заболевании и в большинстве случаев назначаются в сочетании с БПВП.
Наряду с лечебным эффектом, все НПВП, включая селективные (ингибиторы ЦОГ-2), способны вызывать эрозивно-язвенное поражение ЖКТ (в первую очередь верхних его отделов — «НПВП-гастропатия») с возможными осложнениями (кровотечения, перфорации и пр.), а также нефротоксические и другие нежелательные реакции.
Основные характерные черты, которые необходимо учитывать при назначении НПВП, следующие.
- Не существует значимых различий между НПВП в плане эффективности (для большинства препаратов эффект пропорционален дозе вплоть до максимальной рекомендуемой).
- Существуют значительные различия между разными НПВП по переносимости, особенно в отношении поражения ЖКТ.
- Частота нежелательных эффектов обычно пропорциональна дозе НПВП.
- У пациентов с повышенным риском развития НПВП-ассоциированного поражения ЖКТ риск может быть снижен путем параллельного назначения блокаторов протонной помпы, мизопростола.
Существует индивидуальная чувствительность к различным НПВП как в отношении эффективности, так и переносимости лечения. Дозы НПВП при ревматоидном артрите соответствуют стандартным. Продолжительность лечения НПВП определяется индивидуально и зависит от потребности больного в симптоматической терапии. При хорошем ответе на терапию БПВП препарат из группы НПВП может быть отменен.
К наиболее часто применяющимся при ревматоидном артрите НПВП относятся:
- диклофенак (50–150 мг/сут);
- нимесулид (200–400 мг/сут);
- целекоксиб (200–400 мг/сут);
- мелоксикам (7,5–15 мг/сут);
- ибупрофен (800–2400 мг/сут);
- лорноксикам (8–12 мг/сут).
Селективные НПВП, по эффективности достоверно не отличаясь от неселективных, реже вызывают НПВП-гастропатии и серьезные нежелательные реакции со стороны ЖКТ, хотя и не исключают развитие этих осложнений. Ряд клинических исследований продемонстрировал повышенную вероятность развития тяжелой сосудистой патологии (инфаркт миокарда, инсульт) у пациентов, получавших препараты из группы коксибов, в связи с чем возможность лечения целекоксибом должна обсуждаться с особой осторожностью у больных с ИБС и другими серьезными кардиоваскулярными патологиями.
Дополнительные медикаментозные методы лечения. В качестве симптоматического анальгетика (или дополнительного анальгетика при недостаточной эффективности НПВП) может использоваться парацетамол (ацетаминофен) в дозе 500–1500 мг/сут, который обладает относительно невысокой токсичностью. Для локальной симптоматической терапии используются НПВП в виде гелей и мазей, а также диметилсульфоксид в виде 30–50% водного раствора в форме аппликаций. При наличии остеопороза показано соответствующее лечение препаратами кальция, витамина Д3, бифосфонатами, кальцитонином.
Общие принципы ведения больных РА
Больному с установленным диагнозом ревматоидный артрит должен быть назначен препарат из группы БПВП, который при хорошем клиническом эффекте может применяться как единственный метод терапии [9]. Другие лечебные средства используются по мере необходимости.
Больной должен быть информирован о характере своего заболевания, течении, прогнозе, необходимости длительного сложного лечения, а также о возможных нежелательных реакциях и схеме контроля за лечением, неблагоприятных сочетаниях с другими препаратами (в частности, алкоголем), возможной активации очагов хронической инфекции на фоне лечения, целесообразности временной отмены иммуносупрессивных препаратов при возникновении острых инфекционных заболеваний, о необходимости контрацепции на фоне лечения.
Терапия ревматоидного артрита должна назначаться врачом-ревматологом и проводиться под его наблюдением. Лечение биологическими препаратами может проводиться только под контролем ревматолога, имеющего достаточные знания и опыт для его проведения. Терапия является длительной и подразумевает периодический контроль активности болезни и оценку ответа на терапию. Упрощенный алгоритм представлен на рисунке 2.
Мониторинг активности болезни и ответа на терапию включает оценку показателей суставного статуса (число болезненных и припухших суставов и др.), острофазовых показателей крови (СОЭ, СРБ), оценку боли и активности болезни по визуальной аналоговой шкале, оценку функциональной активности больного в повседневной деятельности с помощью русского варианта опросника состояния здоровья (HAQ). Существуют признанные международным сообществом ревматологов методики количественной оценки ответа на лечение с помощью рекомендованного Европейской лигой по борьбе с ревматизмом (EULAR) индекса DAS (Disease Activity Score) и критериев Американской коллегии ревматологов (ACR) [1]. Кроме того, должен осуществляться мониторинг безопасности проводимой пациенту терапии (в соответствии и формуляром и существующими клиническими рекомендациями). В связи с тем, что эрозивный процесс может развиваться даже при низкой воспалительной активности, помимо оценки активности болезни и ответа на терапию обязательно применяется рентгенография суставов. Прогрессирование деструктивных изменений в суставах оценивают путем стандартной рентгенографии кистей и стоп с использованием рентгенологической классификации стадий ревматоидного артрита, количественных методик по индексам Sharp и Larsen. С целью мониторинга состояния больного обследование рекомендуется проводить с определенной периодичностью (табл. 2).
Лечение резистентного к терапии РА
Резистентным к лечению целесообразно считать пациента с неэффективностью (отсутствием 20% улучшения по основным показателям) как минимум двух стандартных БПВП в достаточно высоких дозах (метотрексат — 15–20 мг/нед, сульфасалазин — 2000 мг/сут, лефлуномид — 20 мг/сут). Неэффективность может быть первичной и вторичной (возникающей после периода удовлетворительного ответа на терапию либо при повторном назначении препарата). Существуют следующие пути преодоления резистентности к терапии:
- назначение биологических препаратов (инфликсимаб, ритуксимаб);
- назначение глюкокортикостероидов;
- применение комбинированной базисной терапии;
- применение БПВП второго ряда (циклоспорин и др.).
С точки зрения отдаленных результатов в отношении функциональных нарушений, качества жизни и ее продолжительности оптимальной стратегией терапии ревматоидного артрита является многолетнее лечение БПВП с планомерной сменой схемы их применения по мере необходимости [11].
Литература
- Клинические рекомендации. Ревматология/ под. ред. Е. Л. Насонова. М.: ГЭОТАР-Медиа, 2006. 288 с.
- Emery P., Suarez-Almazor M. Rheumatoid Arthritis// Clin Evid. 2003; 10: 1454–1476.
- Насонов Е. Л., Каратеев Д. Е., Чичасова Н. В., Чемерис Н. А. Современные стандарты фармакотерапии ревматоидного артрита// Клиническая фармакология и терапия. 2005. Т. 14. № 1. С. 72–75.
- Балабанова Р. М., Каратеев Д. Е., Кашеваров Р. Ю., Лучихина Е. Л. Лефлуномид (Арава) при раннем ревматоидном артрите// Научно-практическая ревматология. 2005. № 5. С. 31–34.
- Goekoop-Ruiterman Y. P., de Vries-Bouwstra J. K., Allaart C. F. et al. Clinical and radiographic outcomes of four different treatment strategies in patients with early rheumatoid arthritis (the BeSt study): a randomized, controlled trial// Arthritis Rheum. 2005; v. 52; 11: 3381–90.
- Smolen et al. Therapeutic strategies in early rheumatoid arthritis //Best Practice & Research Clinical Rheumatology. 2005; 19; 1: 163–177.
- Breeveld F. C., Emery P., Keystone E. et al. Infliximab in active early rheumatoid arthritis// Ann Rheum Dis 2004; 63: 149–155.
- Quinn M. A., Conaghan P. G., O’Connor P. J. et al. Very early treatment with infliximab in addition to methotrexate in early, poor-prognosis rheumatoid arthritis reduces magnetic resonance imaging evidence of synovitis and damage, with sustained benefit after infliximab withdrawal: results from a twelve-month randomized, double-blind, placebo-controlled trial// Arthritis Rheum. 2005; 52; 1: 27–35.
- American College of Rheumatology Subcommittee on Rheumatoid Arthritis Guidelines. Guidelines for the management of rheumatoid arthritis. 2002 Update// Arthritis Rheum. 2002; 46: 328–346.
- Quinn M. A., Emery P. Window of opportunity in early rheumatoid arthritis: possibility of altering the disease process with early intervention// Clin Exp Rheumatol. 2003; 21; Suppl 31: 154–157.
- Каратеев Д. Е. Ретроспективная оценка многолетней базисной терапии у больных ревматоидным артритом// Научно-практическая ревматология. 2003. № 3. С. 32–36.
Д. Е. Каратеев, доктор медицинских наук
Институт ревматологии РАМН, Москва
Источник https://clinica-paramita.ru/info/revmatoidnyj-artrit/
Источник https://www.noltrexsin.ru/publikacii/obraz-zhizni-pri-revmatoidnom-artrite/
Источник https://www.lvrach.ru/2007/02/4534789