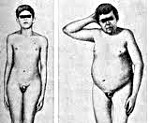
Гипогонадизм у женщин — симптомы и лечение
Что такое гипогонадизм у женщин? Причины возникновения, диагностику и методы лечения разберем в статье доктора Облауховой Вероники Игоревны, эндокринолога со стажем в 7 лет.
Над статьей доктора Облауховой Вероники Игоревны работали литературный редактор Юлия Липовская , научный редактор Светлана Симанина и шеф-редактор Маргарита Тихонова

Эндокринолог Cтаж — 7 лет
Центр новых медицинских технологий (ЦНМТ) на Пирогова
Центр новых медицинских технологий (ЦНМТ) на Сакко и Ванцетти
Дата публикации 24 марта 2022 Обновлено 24 марта 2022
Определение болезни. Причины заболевания
Гипогонадизм (hypogonadism) — это снижение активности гонад: яичков у мужчин и яичников у женщин. При этом состоянии гонады вырабатывают недостаточно половых гормонов (тестостерона у мужчин, эстрогенов и прогестерона у женщин) или организм нечувствителен к этим гормонам [1] .
Самые яркие проявления заболевания — отсутствие менструаций (аменорея) или нарушения менструального цикла у женщин, эректильная дисфункция у мужчин, снижение полового влечения и бесплодие как у мужчин, так и у женщин.
В зависимости от уровня поражения выделяют:
- первичный (гипергонадотропный) гипогонадизм — недостаток половых гормонов из-за первичного поражения гонад;
- вторичный (гипогонадотропный, или центральный) гипогонадизм — дефицит половых гормонов из-за недостаточной стимуляции гонад гормонами гипоталамуса и гипофиза.
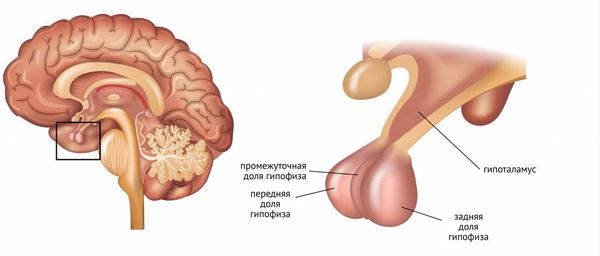
Распространённость гипогонадизма
Гипогонадизм одинаково часто встречается у людей всех рас. Первичный гипогонадизм чаще развивается у мужчин. Согласно исследованиям, частота синдрома Клайнфельтера (самой распространённой причины первичного гипогонадизма у мужчин) выше, чем частота синдрома Шерешевского — Тёрнера (самой распространённой причины гипогонадизма у женщин): синдром Клайнфельтера встречается у одного из 300–600 новорождённых мальчиков, а синдром Шерешевского — Тёрнера диагностируют у одной из 2000–5000 новорождённых девочек [3] [4] .
Заболеваемость вторичным гипогонадизмом одинаковая у мужчин и женщин [1] .
Болезнь может возникнуть в любом возрасте, но последствия различаются в зависимости от возраста, в котором началось заболевание:
- Если гипогонадизм возникает пренатально (внутриутробно), то следствием будет нарушение формирования пола, при котором у ребёнка могут быть признаки обоих полов, например мужской кариотип (хромосомный набор клеток) и женские половые органы.
- Если гипогонадизм развивается до полового созревания (пубертата), у девочек не начинаются менструации, не появляются вторичные половые признаки (например, молочные железы), у мальчиков наблюдается крипторхизм, малый размер яичек, микропенис.
- Если болезнь проявляется после полового созревания, то характерны бесплодие и сексуальная дисфункция (снижение либидо, отсутствие эрекций у мужчин).
Что такое женский гипогонадизм
Женский гипогонадизм — это состояние, при котором яичники вырабатывают недостаточно половых гормонов (эстрогена и прогестерона) или вообще не вырабатывают их. В большинстве случаев это проявляется ановуляцией, нарушениями менструального цикла (вторичной аменореей или олигоменореей) и бесплодием. При врождённом гипогонадизме наблюдается задержка полового созревания и отсутствие менструаций (первичная аменорея).
Первичным гипогонадизмом страдает 1–2 % всех женщин мира, вторичным гипогонадизмом — 3–5 %. В структуре эндокринного бесплодия частота этих нарушений составляет 5 и 10 % соответственно, т. е. гипогонадизм — довольно редкая причина бесплодия [5] .
Причины женского гипогонадизма
Причины гипергонадотропного (первичного) гипогонадизма:
1. Врождённых форм:
- Синдром Шерешевского — Тёрнера. Это хромосомное заболевание, при котором одна из Х-хромосом отсутствует или в ней есть дефект. Кариотип при этом синдроме — 45X, а нормальный женский кариотип — 46ХХ. Для этого синдрома характерны недоразвитые яичники.
- Мозаичный кариотип (наличие клеток с разным набором хромосом) — 45X/46XX.
- Мозаичный кариотип с обязательным присутствием Y хромосомы или её участка, чаще всего встречается кариотип 45X/46XY.
- XY-дисгенезия гонад (синдром Свайера). У человека с этим нарушением мужской кариотип, но он выглядит как женщина и имеет все женские внутренние органы, кроме яичников.
- XX-дисгенезия. У человека женский кариотип, он выглядит как женщина, но не имеет яичников.
- Синдром резистентных яичников. Это нечувствительность яичников к гормонам гипофиза: фолликулостимулирующему (ФСГ) и лютеинизирующему (ЛГ) , которые в норме воздействуют на яичники и стимулируют рост фолликулов и выход яйцеклетки (овуляцию).
- Избыток галактозы — одного из основных источников энергии организма.
- Синдром нарушения гликозилирования 1-го типа. Это редкая врождённая ошибка углеводного обмена.
- Мутации гена рецептора ФСГ.
- Синдром Нунана. Это генетическая патология, которая характеризуется развитием у больных симптомов, похожих на болезнь Шерешевского — Тёрнера.
2. Приобретённых форм:
- Инфекционные поражения яичников.
- Радиация.
- Преждевременная менопауза, или синдром истощения яичников.
- Травма яичников.
- Операция на яичниках.
- Химиотерапия (алкилирующие и антинеопластические агенты).
- Аутоиммунные заболевания, например аутоиммунный оофорит, при котором собственная иммунная система атакует яичники.
- Приём токсичных веществ.
- Приём препаратов, которые подавляют синтез половых гормонов: блокаторов стероидогенеза, блокаторов ароматазы и т. д.
Причины гипогонадотропного (вторичного) гипогонадизма:
1. Врождённых форм:
- Нарушения секреции гонадотропин-рилизинг-гормона (ГнРГ) — синдром Кальмана в сочетании с аносмией (потерей обоняния) и без неё.
- Изолированное нарушение секреции ФСГ и ЛГ.
- Гипофизарная недостаточность, при которой снижена секреция большинства гормонов гипофиза.
- Мозжечковые атаксии с гипогонадизмом. Это нарушение координации, вызванное патологией мозжечка.
- Синдром Прадера — Вилли, синдром Барде — Бидля и др. При этих синдромах кроме гипогонадизма выявляются и другие нарушения.
2. Приобретённых форм:
- Инфекции и опухоли гипоталамуса, серого бугра и гипофиза, в том числе со сдавлением окружающих структур.
- Гиперпролактинемия (избыток пролактина в крови), в том числе на фоне приёма антипсихотических препаратов.
- Гиперандрогения (избыток андрогенов в крови) на фоне дефицита кортизола при врождённой дисфункции коры надпочечников .
- Лучевая и химиотерапия.
- Аутоиммунные заболевания, например лимфоцитарный гипофизит (воспаление гипофиза).
- Инфекционные заболевания, затрагивающие область гипофиза и гиполатамуса.
- Апоплексия гипофиза (резкое увеличение размера опухоли гипофиза из-за её кровоизлияния);
- Приём лекарственных препаратов: аналогов ГнРГ, половых стероидов, глюкокортикоидов, опиатов и др.
- Тяжёлые хронические заболевания: пороки сердца, заболевания желудочно-кишечного тракта, печени, почек, лёгких и др.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы гипогонадизма у женщин
Общие симптомы всех форм гипогонадизма, появившегося до полового созревания:
- нет менархе (первой менструации) в возрасте 16 лет и старше;
- нет признаков полового созревания (молочных желёз, оволосения) в возрасте 14 лет и старше;
- нет первой менструации в течение трёх и более лет после развития вторичных половых признаков;
- биологический возраст не соответствует календарному;
- нет обоняния (аносмия) при синдроме Кальмана [2][22] .
Проявления гипогонадизма, возникшего после начала полового созревания:
- нарушается менструальный цикл и развивается вторичная аменорея;
- замедляется развитие молочных желёз или они уменьшаются в размере;
- не наступает беременность (бесплодие);
- до 40 лет появляются симптомы климакса: приливы жара, ночная потливость, приступы удушья, озноб, ощущение усиленного сердцебиения, слабость, сонливость, беспричинное беспокойство и раздражительность [2][22] .
Патогенез гипогонадизма у женщин
Ось гипоталамус-гипофиз-гонады играет решающую роль в формировании пола, половом созревании и фертильности (способности к зачатию).
Гипофиз вырабатывает ФСГ и ЛГ. У женщин ФСГ стимулирует развитие доминантного фолликула в яичнике и созревание в нём яйцеклетки [11] . Также ФСГ помогает развиваться следующему поколению фолликулов, которые будут созревать во время остальных циклов.
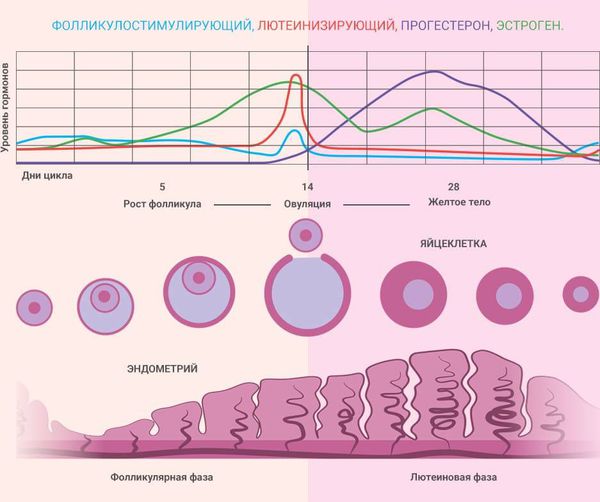
ЛГ — это главный регулятор синтеза половых гормонов яичниками. Он стимулирует производство эстрогенов из их предшественников — андрогенов [12] . Всплеск ЛГ в середине цикла стимулирует созревание яйцеклетки в фолликуле, разрыв доминирующего фолликула и выход яйцеклетки (овуляцию). Благодаря ЛГ стенки фолликула преобразуются в жёлтое тело, которое вырабатывает прогестерон (гормон беременности), андрогены и эстрогены [11] [14] .
Так ФСГ и ЛГ управляют менструальным циклом и синтезом половых стероидных гормонов. Яичники, в свою очередь, тоже регулируют уровень этих гормонов по принципу обратной связи. В лютеиновой фазе яичники вырабатывают больше половых гормонов и за счёт этого снижается выработка ФСГ и ЛГ. Если зачатия не происходит, то уровень эстрогенов и прогестерона снижается и начинается менструация, а уровень ФСГ и ЛГ, наоборот, начинает подниматься.
Гипоталамус регулирует синтез и секрецию ЛГ и ФСГ с помощью ГнРГ, обратной связи со стороны яичников, а также с помощью самого гипофиза за счёт местных факторов (активинов, ингибинов и фоллистатина) [10] .
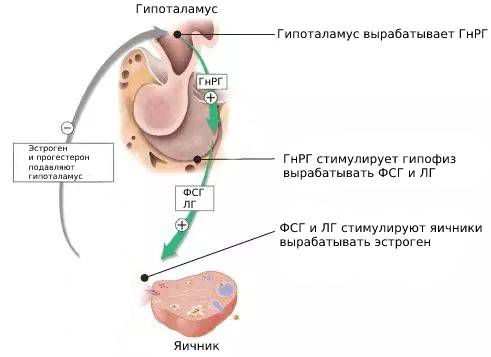
Гипергонадотропный (первичный) гипогонадизм вызван первичной недостаточностью яичников. В норме яичники вырабатывают эстрогены, которые подавляют синтез ГнРГ, ЛГ и ФСГ. Но если яичники производят недостаточно эстрогенов, уровень ГнРГ, ЛГ и ФСГ увеличивается.
Такая реакция может быть связана с генетическими причинами, при которых яичники недоразвиты, химио- или лучевой терапией, операциями на яичниках, перенесёнными инфекционными заболеваниями с вовлечением ткани яичников и др.
При гипогонадотропном (вторичном) гипогонадизме гипоталамус не вырабатывает ГнРГ или вырабатывает его недостаточно. Также это состояние возможно, если гипофиз не производит ЛГ и ФСГ или производит недостаточно. Если этих гормонов мало, снижается стимуляция яичников и они вырабатывают меньше эстрогенов.
Если такое нарушение развивается до полового созревания, причиной могут быть аномалии развития центральной нервной системы (ЦНС), нарушения чувствительности рецептора к ГнРГ или нарушения закладки гипоталамо-гипофизарных структур [15] [16] . Известно около 40 генов, нарушения в которых приводят к возникновению вторичного гипогонадизма [17] [18] .
После полового созревания эта форма гипогонадизма возникает из-за патологий гипоталамо-гипофизарной области или воздействий, которые нарушают её функцию: перенесённого энцефалита, посттравматических изменений, радиации (в том числе лучевой терапии по поводу онкозаболеваний), опухолевых процессов, туберкулёза, саркоидоза, некоторых лекарств и др.
Транзиторный (функциональный, или временный) гипогонадизм возникает при чрезмерных физических нагрузках и снижении веса из-за нарушения синтеза нейропептидов, лептина и грелина, влияющих на секрецию ГнРГ [19] .
Временный гипогонадизм также может быть связан с синдромом гиперторможения яичников. Он развивается после длительного приёма эстроген-гестагенных препаратов (КОК), которые тормозят выделение ЛГ и ФСГ в гипофизе.
В итоге, независимо от формы гипогонадизма и его причин, развивается первичное или вторичное бесплодие.
Классификация и стадии развития гипогонадизма у женщин
Классифиакция гипогонадизма:
- Первичный (гипергонадотропный) гипогонадизм: врождённый и приобретённый.
- Вторичный (гипогонадотропный) гипогонадизм: врождённый и приобретённый (включая временный гипогонадизм).
Классификация вторичного гипогонадизма в зависимости от причины и длительности:
- Функциональный (временный) гипогонадизм:
- Конституциональная задержка роста и пубертата (синдром позднего пубертата). Наследственное нарушение, при этом у одного или обоих родителей было позднее половое созревание. Чаще встречается у мальчиков.
- Соматогенная задержка пубертата. Возникает из-за нарушений питания (гипо- или авитаминоза, дефицита белка или минеральных веществ), ожирения, хронических заболеваний (пороков сердца, заболеваний желудочно-кишечного тракта, печени, почек, лёгких и др.) или негативных социальных факторов.
- Перманентный (постоянный) гипогонадизм. В этом случае гипоталамо-гипофизарно-гонадная ось не восстанавливается и требуется пожизненная заместительная гормональная терапия (ЗГТ) [8] .
- Реверсивный (обратимый) гипогонадизм. Через несколько лет лечения гипоталамо-гипофизарно-гонадная ось восстанавливается [9] .
Осложнения гипогонадизма у женщин
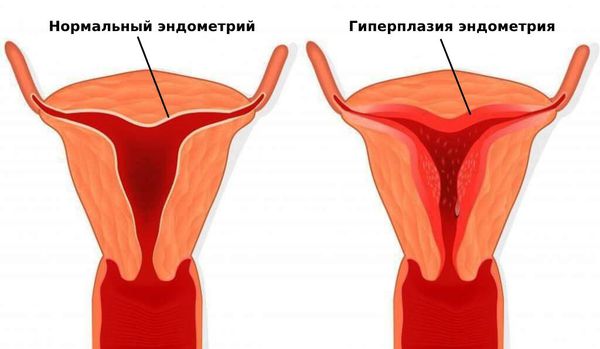
Нарушения менструального цикла и аменорея повышают риск развития гиперплазии и рака эндометрия. Гиперплазия эндометрия может приводить к частым обильным кровотечениям и анемии на фоне хронической кровопотери [24] .
Из-за недостатка эстрогена у женщин замедляется обмен веществ и, как следствие, возникает дефицит минералов и витаминов, из-за этого повышается риск остеопороза (повышенной хрупкости костей) и переломов. Также могут развиваться урогенитальные осложнения: сухость слизистой влагалища и боль при половом акте [24] . Помимо этого, снижается половое влечение и сексуальная активность.
Гипогонадизм часто сопровождается избыточным весом или ожирением, а это повышает риск возникновения серьёзных патологий:
- предиабета;
- сахарного диабета 2-го типа;
- неалкогольной жировой болезни печени (жирового гепатоза);
- гипертонии;
- сердечно-сосудистых заболеваний: атеросклероза, ишемической болезни сердца, инфаркта миокарда, ишемического инсульта[2] .
Чтобы предотвратить эти осложнения, нужно своевременно обратиться за медицинской помощью к специалисту.
Диагностика гипогонадизма у женщин
Диагностикой и лечением гипогонадизма занимается врач-эндокринолог.
Сбор анамнеза и жалоб
Чтобы изучить историю болезни пациента, врач на приёме может спросить:
- Когда наступило половое созревание у ближайших родственников и есть ли у кого-то из родных гипогонадизм или бесплодие. Позднее половое созревание у одного или обоих родителей позволяет заподозрить конституциональную задержку полового развития, а наличие в семье родственников с гипогонадизмом указывает на генетическую предрасположенность.
- Есть ли задержки психического и умственного развития, врождённые пороки развития, хронические заболевания (сахарный диабет, гипертония и др.), были ли операции в прошлом. Эти состояния характерны для некоторых форм гипогонадизма.
- Есть ли неврологическая симптоматика: сильные головные боли, нарушение зрения и терморегуляции, тошнота, рвота и др. Это может указывать на органические нарушения гипоталамо-гипофизарной области.
- При сборе анамнеза у детей врач может спросить, как изменился рост ребёнка за последние 2–3 года, когда и в какой последовательности появились вторичные половые признаки.
- У взрослых женщин при наличии вторичной аменореи специалист поинтересуется, соблюдает ли пациентка диету при избыточном весе, какие у неё физические нагрузки, принимает ли КОК и как долго.
Осмотр
Данные осмотра будут различаться в зависимости от времени появления, вида и формы гипогонадизма:
- До полового созревания у девочек нет никаких специфических проявлений гипогонадизма.
- В период полового созревания у девочек старше 13 лет не растут молочные железы, вторичные половые признаки не появляются или не соответствуют возрасту либо нет первой менструации в 16 лет и старше (первичная аменорея) [20] .
При гинекологическом исследовании наружные и внутренние половые органы недоразвиты, слизистые оболочки вульвы и влагалища атрофированы.
Низкий вес у пациентки может указывать на функциональный гипогонадизм. При этом вторичные половые признаки будут развиты нормально. При гинекологическом исследовании наблюдается атрофия слизистых вульвы и влагалища.
При синдроме гиперторможения яичников никаких отклонений при общем осмотре не обнаруживается.
Лабораторная диагностика
Анализы крови на ФСГ, ЛГ и эстрадиол позволяют поставить диагноз «гипогонадизм» и определить его вид.
Первичный гипогонадизм устанавливают при повышении уровней ЛГ и ФСГ выше возрастных норм при сниженном значении эстрадиола. Для взрослых женщин критерием служит ФСГ > 30 Ед/л при двукратном определении [5] . У девочек этот критерий зависит от возраста, так как есть физиологические пики секреции ФСГ [22] .
Вторичный гипогонадизм диагностируют при снижении уровней ЛГ и ФСГ ниже возрастных норм при сниженном значении эстрадиола. Для взрослых женщин критерием служит ФСГ < 1,6 Ед/л при двукратном определении [5] . У девочек в любом возрасте — ЛГ < 0,9 Ед/л, ФСГ < 2,5 Ед/л и неопределяемый/низкий уровень эстрадиола [21] .
Анализы крови на тиреотропный гормон (ТТГ), пролактин, адренокортикотропный гормон (АКТГ), инсулиноподобный фактор роста (ИФР-1), кортизол и глюкозу крови помогают отличить гипогонадизм от других причин аменореи и бесплодия и выявить сопутствующие патологии.
Генетическое обследование включает:
- Определение полового хроматина (неактивной X-хромосомы) в мазках с внутренней поверхности щеки. При гипогонадизме половой хроматин не выявляется.
- Определение кариотипа. При гипогонадизме набор хромосом он будет типичен для той или иной формы болезни, например при синдроме Шерешевского — Тёрнера чаще всего пациентки имеют кариотип 45Х.
Это не обязательное исследование, так как оно дорогостоящее и не влияет на тактику лечения. Зато этот анализ позволяет проводить семейное генетическое консультирование пар, которые планируют беременность, что помогает предотвратить рождение детей с наследственными патологиями. Может выполняться у пациенток с симптомами синдрома Шерешевского — Тёрнера, а также у пациенток с нормальным уровнем гонадотропных гормонов, сформированными вторичными половыми признаками, но с первичной аменореей и отсутствием матки по данным УЗИ или МРТ.
Пробы с аналогом ГнРГ, гестагенами, эстрогенами и гестагенами. Эти пробы проводятся, чтобы отличить первичный и вторичный гипогонадизм:
- При пробах с аналогом ГнРГ сначала определяют уровень ФСГ и ЛГ, затем вводят аналог ГнРГ короткого действия, через 1 и 4 часа после введения оценивают, как изменились ФСГ и ЛГ: подъём ЛГ выше 10 мЕд/л позволяет исключить вторичный гипогонадизм.
- На фоне приёма препаратов гестагенов могут появиться кровянистые выделения, это говорит о достаточной количестве эстрогенов в организме и исключает первичный гипогонадизм.
Инструментальная диагностика
УЗИ органов малого таза позволяет оценить развитие яичников и матки, определить толщину эндометрия. Проводится во всех случаях гипогонадизма.
МРТ головного мозга проводится при подозрении на органические нарушения в гипоталамо-гипофизарной системе.
Оценка плотности костной ткани назначается девочкам пубертатного возраста и взрослым женщинам с гипогонадизмом при наличии отягощённого анамнеза: вторичной аменореи; функционального гипогонадотропного гипогонадизма, связанного с хроническими воспалительными заболеваниями кишечника (болезнью Крона, неспецифическим язвенным колитом); целиакии; сахарного диабета 1-го типа и др.
При подозрении на гипогонадизм дифференциальный диагноз проводится между его видами и формами.
Лечение гипогонадизма у женщин
Если в кариотипе есть мужская Y-хромосома или её фрагмент, то чаще всего яичники удаляют до 20 лет из-за высокого риска их злокачественного перерождения. После удаления яичников проводят заместительную гормональную терапию (ЗГТ) до возраста естественной менопаузы (как правило, она наступает в 46–50 лет) для профилактики осложнений, таких как остеопороз. Лечение начинают с назначения эстрогенов в форме таблеток или пластырей, далее переходят на циклическую гормональную терапию с добавлением гестагенов. Для стимуляции роста также применяют малые дозы гормона роста [2] [22] .
При опухолях гипофиза лечение хирургическое. ЗГТ требуется, если гипофиз перестал вырабатывать гормоны. Объём терапии зависит от результатов клинических и лабораторных исследований, как правило, ЗГТ в этом случае проводится пожизненно или до возраста физиологической менопаузы, если речь о половых гормонах.
При врождённом вторичном гипогонадизме также требуется ЗГТ [2] [22] . Половое созревание в этом случае стимулируется препаратами эстрогенов. При появлении на УЗИ фолликулов в яичниках, повышении уровня эстрогенов и появлении менструальноподобных выделений к терапии добавляют прогестерон, чтобы предотвратить гиперплазию эндометрия и установить регулярный менструальный цикл. Если выделений нет, значит эстрогена недостаточно и терапию нужно скорректировать.
Если пациентка хочет забеременеть, проводят стимуляцию овуляции [5] [13] . При успешном зачатии женщину будет наблюдать акушер-гинеколог согласно клиническим рекомендациям по нормальной беременности.
При гипогонадизме, который связан с синдромом резистентных яичников, проводят менопаузальную гормональную терапию двух- и трёхфазными эстроген-гестагенными препаратами до возраста физиологической менопаузы [2] .
В случаях функционального гипогонадизма и синдрома гиперторможения яичников специфическую терапию не проводят. Пациентке нужно нормализовать режим сна и отдыха, питание и отменить КОК, тогда система гипоталамус-гипофиз-гонады восстановится самостоятельно в течение 3–4 месяцев [2] .
Прогноз. Профилактика
При первичном гипогонадизме пациентка не сможет забеременеть самостоятельно, но благодаря программам вспомогательных репродуктивных технологий (ВРТ) с донорской яйцеклеткой женщина может забеременеть и родить [5] .
У таких пациенток повышен риск развития опухолей яичников, поэтому им рекомендуется регулярно посещать гинеколога и проходить дополнительные обследования, если обнаруживаются отклонения.
При врождённом вторичном гипогонадизме рекомендовано применение ВРТ со стимуляцией овуляции [5] . Спонтанная беременность чаще всего невозможна.
При функциональном гипогонадизме способность к зачатию восстанавливается, когда исчезают провоцирующие факторы. Если беременность не наступает в течение года у женщин до 35 лет и в течение 6 месяцев у женщин старше 35 лет, также требуется стимуляция овуляции [5] .
Во всех вышеперечисленных случаях пациентки могут выносить ребёнка самостоятельно. Беременность наблюдает акушер-гинеколог согласно рекомендациям по нормальной беременности.
Профилактика женского гипогонадизма
Специфической профилактики не существует. Всем пациенткам с гипогонадизмом независимо от его вида и формы рекомендуется вести здоровый образ жизни, чтобы не допустить осложнений: спать не менее 8 часов в сутки, рационально питаться и быть физически активными.
Список литературы
- Vogiatzi M. G. Hypogonadism // Medscape. — 2021.
- Эндокринология: национальное руководство / под ред. И. И. Дедова, Г. А. Мельниченко. — 2-е изд., перераб. и доп. — М.: ГЭОТАР-Медиа, 2018. — 832 с.
- Paduch D. A., Bolyakov A., Cohen P., Travis A. Reproduction in men with Klinefelter syndrome: the past, the present, and the future // Semin Reprod Med. — 2009. — Vol. 27, № 2. — Р. 137–148.ссылка
- Donaldson M. D., Gault E. J., Tan K. W., Dunger D. B. Optimising management in Turner syndrome: from infancy to adult transfer // Arch Dis Child. — 2006. — Vol. 91, № 6. — Р. 513–520.ссылка
- Российское общество акушеров-гинекологов. Женское бесплодие: клинические рекомендации. — 2021. — 82 с.
- Silveira L. F., Latronico A. C. Approach to the patient with hypogonadotropic hypogonadism // J Clin Endocrinol Metab. — 2013. — Vol. 98, № 5. — Р. 1781–1788. ссылка
- Gravholt C. H., Andersen N. H., Conway G. S. et al. International Turner Syndrome Consensus Group. Clinical practice guidelines for the care of girls and women with Turner syndrome: proceedings from the 2016 Cincinnati International Turner Syndrome Meeting // Eur J Endocrinol. — 2017. — Vol. 177, № 3. — Р. G1–G70.ссылка
- Palmert M. R., Dunkel L. Clinical practice. Delayed puberty // N Engl J Med. — 2012. — Vol. 366, № 5. — Р. 443–453.ссылка
- Sidhoum V. F., Chan Y. M., Lippincott M. F. Reversal and relapse of hypogonadotropic hypogonadism: resilience and fragility of the reproductive neuroendocrine system // J Clin Endocrinol Metab. — 2014. — Vol. 99, № 3, — Р. 861–870. ссылка
- Coss D., Mellon P. L., Thackray V. G. A FoxL in the Smad house: activin regulation of FSH // Trends Endocrinol Metab. — 2010. — Vol. 21, № 9. — Р. 562–568.ссылка
- Richards J. S., Pangas S. A. The ovary: basic biology and clinical implications // J Clin Invest. — 2010. — Vol. 120, № 4. — Р. 963–972.ссылка
- Themmen A. P. N., Huhtaniemi I. T. Mutations of gonadotropins and gonadotropin receptors: elucidating the physiology and pathophysiology of pituitary-gonadal function // Endocr Rev. — 2000. — Vol. 21, № 5. — Р. 551–583.ссылка
- Российское общество акушеров-гинекологов. Аменорея и олигоменорея: клинические рекомендации. — 2021. — 57 с.
- Macklon N. S., Stouffer R. L., Giudice L. C., Fauser B. C. The science behind 25 years of ovarian stimulation for in vitro fertilization // Endocr Rev. — 2006. — Vol. 27, № 2. — Р. 170–207. ссылка
- Макрецкая Н. А., Герасимова М. В., Васильев Е. В. и др. Клиническая и молекулярно-генетическая характеристика случаев изолированного гипогонадотропного гипогонадизма, обусловленного дефектами рецептора гонадотропин-рилизинг-гормона // Проблемы эндокринологии. — 2021. — Т. 67, № 3. — C. 62–67.
- Young J., Xu C., Papadakis G. E. et al. Clinical Management of Congenital Hypogonadotropic Hypogonadism // Endocr Rev. — 2019. — Vol. 40, № 2. — Р. 669–710. ссылка
- Maione L., Dwyer A. A., Francou B. Genetics in endocrinology: genetic counseling for congenital hypogonadotropic hypogonadism and Kallmann syndrome: new challenges in the era of oligogenism and next-generation sequencing // Eur J Endocrinol. — 2018. — Vol. 178, № 3. — Р. R55–R80.ссылка
- Stamou M. I., Cox K. H., Crowley W. F. Jr. Discovering Genes Essential to the Hypothalamic Regulation of Human Reproduction Using a Human Disease Model: Adjusting to Life in the «-Omics» Era // Endocr Rev. — 2015. — Vol. 36, № 6. — Р. 603–621.ссылка
- Celik O., Celik N., Aydin S. et al. Ghrelin action on GnRH neurons and pituitary gonadotropes might be mediated by GnIH-GPR147 system // Horm Mol Biol Clin Investig. — 2016. — Vol. 25, № 2. — Р. 121–128.ссылка
- Persani L., Bonomi M., Cools M. et al. ENDO-ERN expert opinion on the differential diagnosis of pubertal delay // Endocrine. — 2021. — Vol. 71, № 3. — Р. 681–688.ссылка
- Boehm U., Bouloux P. M., Dattani M. T. et al. Expert consensus document: European Consensus Statement on congenital hypogonadotropic hypogonadism — pathogenesis, diagnosis and treatment // Nat Rev Endocrinol. — 2015. — Vol. 11, № 9. — Р. 547–564. ссылка
- Российская ассоциация эндокринологов. Гипогонадизм у детей и подростков: клинические рекомендации. — 2016. — 23 с.
Гипогонадизм женский
Гипогонадизм женский — это патологическое состояние, проявляющееся нарушением функций яичников. При этом наблюдается недостаток эстрогенов – половых гормонов, а также сбои в циклической работе яичников. В зависимости от причин, различают первичный и вторичный гипогонадизм. Эти заболевания по-разному проявляются клинически.

Акушер-гинеколог, оперирующий гинеколог
Стаж работы 17 лет.
Статья проверена акушером-гинекологом, к.м.н. Пироговой Марией Николаевной.
| Причины женского гипогонадизма |
| Признаки и симптомы женского гипогонадизма |
| Диагностика женского гипогонадизма |
| Лечение женского гипогонадизма |
| Профилактика женского гипогонадизма |
| Причины женского гипогонадизма Причины женского гипогонадизма кроются в недостаточном синтезе эстрогенов (женский половой гормон). Под воздействием гонадотропина увеличивается продуцирование ЛГ (лютеинизирующий гормон) и фоллитропина (фолликулостимулирующий гормон). Повышенный уровень ЛГ является нормальным для климактерического периода, но это патология для женщин в репродуктивном возрасте. В норме лютропин повышается у женщин только при овуляции. Постоянный сдвиг ФСГ в сторону повышения приводит к снижению либидо, сексуальной холодности, торможению созревания фолликулов, бесплодию.
Концентрации гормонов в менструальном цикле Все это характерно для первичного гипогонадизма у женщин, причинами которого могут быть:
Причиной вторичного гипогонадизма является гипоталамо-гипофизарные заболевания, чаще всего новообразования или нейроинфекции. Это может быть арахноидит, менингит, энцефалит, нейроглиомы, астроцитомы и другие виды опухолей головного мозга, поражающие гипоталамо-гипофизарную область. При этом гонадотропины, влияющие на функцию яичников, не синтезируются вообще либо наблюдается их существенный недостаток. Симптомы и лечение женского гипогонадизма зависят от причины возникновения заболевания. В зависимости от причин возникновения, различают такие формы заболевания:
В данном случае гипофиз не вырабатывает гормоны гонадотропины, или их секреция значительно уменьшается. Следовательно, нарушается функция яичников, так как отсутствует их стимуляция. Установить форму патологии по клиническим проявлениям невозможно, поэтому пациенткам обязательно назначаются все необходимые обследования для выяснения причины женского гипогонадизма. Признаки и симптомы женского гипогонадизмаКлинические проявления патологии зависят от степени выраженности недостатка женских половых гормонов, а также от возрастного периода, в котором началось заболевание. Гипогонадизм, возникший у девушек до периода полового созревания. Проявляется в виде недоразвития органов репродуктивной системы (гипоплазии органов малого таза и молочных желез). У женщины могут наблюдаться деформации скелета, нарушение размера и формы таза. Характерные симптомы женского гипогонадизма — отсутствие вторичных половых признаков. К ним относят оволосение в подмышечных и лобковой области, рост груди, начало менструации, формирование женственной фигуры за счет отложения жировой ткани на бедрах и ягодицах. При осмотре у больной наблюдаются:
Гипогонадизм, возникший после периода полового созревания. У женщин наблюдаются такие проявления, как нерегулярные менструации или даже полное их прекращение. Со временем происходит атрофия органов репродуктивной системы, редеют волосяные покровы в подмышечных впадинах и на лобке. Появляются симптомы климакса: сухость слизистых оболочек, остеопороз, внезапные приливы, повышенная потливость. Относительно нарушения цикла возможны такие варианты
Для постановки точного диагноза «женский гипогонадизм» учитываются все признаки, а не только нарушение цикла. В обоих случаях к клиническим проявлениям гипогонадизма у женщин присоединяется и бесплодие. Причиной этому является угнетение функциональной деятельности яичников и нарушение созревания яйцеклетки. Последствиями гипогонадизма у женщин могут быть следующие патологические состояния:
Женщины, болеющие сахарным диабетом, ВИЧ-инфекцией, перенесшие хирургическое вмешательство по поводу злокачественной опухоли больше подвержены заболеваемости гипогонадизмом. Диагностика женского гипогонадизмаПри подозрении на патологию, пациентке назначается обследование для подтверждения диагноза. Диагностика женского гипогонадизма включает:
Дополнительно может быть назначена денситометрия (определение плотности костных тканей) и рентгенография, что требуется для выявления остеопороза. Помимо этого, в диагностику женского гипогонадизма входят дополнительные обследования. Например, для оценки степени минерализации костей назначается денситометрия. Анализ мочи берется для выявления кетостероидов – веществ, образующихся в результате метаболизма андрогенов. При подозрении на гипофизарную опухоль проводится МР-сканирование или компьютерная томография. При постановке окончательного диагноза учитывается анамнез, жалобы пациентки, результаты диагностики, характерные симптомы женского гипогонадизма. Лечение женского гипогонадизмаЛечение патологии зависит от ее формы, причины возникновения, а также возраста, в котором она началась. Основной задачей лечебных мероприятий является снижение проявлений дефицита эстрогенов. В основном пациенткам назначают терапию, замещающую выработку необходимых гормонов организмом, если нет противопоказаний. Препараты, дозировки и схема приема определяется для каждой женщины индивидуально врачом. Как лечить гипогонадизм у женщин с тяжелыми нарушениями сердечно-сосудистой системы, наличием злокачественных новообразований? В данном случае заместительная терапия, как правило, не назначается. Лечение женского гипогонадизма подбирается индивидуально, в зависимости от конкретного случая. Заболевание требует обязательного лечения, поскольку осложнения женского гипогонадизма, могут привести к бесплодию. Причем терапию нужно начинать как можно раньше еще в подростковом возрасте. Если этого не сделать, то возможна задержка полового развития у девочек-подростков, недоразвитие внутренних половых органов. Так, среди осложнений женского гипогонадизма встречаются гипоплазия матки, фаллопиевых труб, дисфункция яичников. Кроме того, наблюдаются деформации костей скелета, малокровие, заболевания сердца и сосудов. Восстановить репродуктивную функцию при первичном гипогонадизме очень сложно, хотя есть возможность при своевременном обнаружении заболевания провести заместительную терапию для правильного развития вторичных половых признаков. В некоторых случаях используя импульсную замещающую гормональную терапию, удается добиться нормального менструального цикла. При вторичном гипогонадизме, нормальное развитие половых органов позволяет на фоне заместительной терапии женщине забеременеть и выносить ребенка. Здесь требуется постоянный контроль и коррекция доз препаратов. Профилактика женского гипогонадизмаПри первичной форме заболевания профилактика женского гипогонадизма может быть пренатальной и заключается в тщательном обследовании женщины на хромосомные патологии, инфекционные заболевания. Выявление таких болезней, как туберкулез, сифилис являются относительным противопоказанием для беременности. Во избежание развития у плода гипогонадизма следует планировать беременность после полного излечения или достижения стабильной клинической ремиссии. Беременная должна вовремя встать на учет, регулярно посещать врача на протяжении беременности. Необходимо также выполнять рекомендации акушера-гинеколога:
Профилактика женского гипогонадизма также заключается в бережном отношении к своему здоровью, своевременному выявлению и лечению заболеваний, приводящих к нему. Необходимо с осторожностью выбирать половых партнеров, использовать барьерные методы контрацепции, а при обнаружении симптомов инфекционного заболевания обратиться к врачу. Терапия должна быть полноценной и адекватной, чтобы полностью вылечить болезнь и не допустить ее перехода в хроническую форму. Особое значение приобретают заболевания половых органов инфекционного и воспалительного характера, которые могут привести к поражению тканей яичника, необходимости его резекции. Это могут быть ЗППП, аднекситы, оофориты, перитониты на фоне аппендицита, перфорации желудка, кишечника и другие болезни. Удаление обеих яичников, при отсутствии адекватной замещающей терапии приведет не только к появлению симптоматики гипогонадизма и раннему климаксу, но и полностью исключит возможность женщины самостоятельно забеременеть. Конечно, можно воспользоваться вспомогательными репродуктивными технологиями и программой донорства яйцеклеток. В случае вторичного гипогонадизма, есть возможность путем стимуляции яичников добиться созревания фолликулов. Если у больной обнаружена опухоль и требуется химио- или лучевая терапия лучше заранее обеспокоиться и сделать забор и криоконсервацию яйцеклеток. Это позволит после лечения использовать качественный, неповрежденный биоматериал, для того чтобы забеременеть и родить. У Вас есть вопросы? Получите квалифицированный ответ от ведущих специалистов клиники. Гипогонадизм
Гипогонадизм – синдром, сопровождающийся недостаточностью функций половых желез и нарушением синтеза половых гормонов. Гипогонадизм, как правило, сопровождается недоразвитием наружных или внутренних половых органов, вторичных половых признаков, расстройством жирового и белкового обмена (ожирением или кахексией, изменениями костной системы, сердечно-сосудистыми нарушениями). Диагностика и терапия гипогонадизма осуществляется совместной работой эндокринологов, гинекологов и гинекологов-эндокринологов (у женщин), андрологов (у мужчин). Основу лечения гипогонадизма составляет заместительная гормональная терапия. При необходимости проводится хирургическая коррекция, пластика и протезирование половых органов.
Общие сведенияГипогонадизм – синдром, сопровождающийся недостаточностью функций половых желез и нарушением синтеза половых гормонов. Гипогонадизм, как правило, сопровождается недоразвитием наружных или внутренних половых органов, вторичных половых признаков, расстройством жирового и белкового обмена (ожирением или кахексией, изменениями костной системы, сердечно-сосудистыми нарушениями). Различают мужской и женский гипогонадизм. Гипогонадизм у мужчинКлассификация гипогонадизма у мужчинГипогонадизм делится на первичный и вторичный. Первичный гипогонадизм вызван нарушением функции тестикулярной ткани вследствие дефекта самих яичек. Хромосомные нарушения могут приводить к аплазии или гипоплазии тестикулярной ткани, что проявляется отсутствием секреции андрогенов или их недостаточностью для нормального формирования половых органов и вторичных половых признаков. Возникновение вторичного гипогонадизма обусловлено нарушением структуры гипофиза, снижением его гонадотропной функции или поражением гипоталамических центров, регулирующих деятельность гипофиза. Первичный гипогонадизм, развивающийся в раннем детском возрасте, сопровождается психическим инфантилизмом, вторичный — психическими расстройствами. Различают также гипогонадотропный, гипергонадотропный и нормогонадотропный гипогонадизм. Гипергонадотропный гипогонадизм проявляется первичным поражением тестикулярной ткани яичек в сочетании с повышенным уровнем гонадотропных гормонов гипофиза. Гипогонадотропный и нормогонадотропный гипогонадизм возникают при поражении гипоталамо-гипофизарной системы. Гипогонадотропный гипогонадизм связан со снижением секреции гонадотропинов, в результате чего уменьшается выработка андрогенов тестикулярной тканью яичек. Нормогонадотропный гипогонадизм вызван гиперпролактинемией, проявляется нормальным уровнем гонадотропинов и сниженной тестикулярной функцией яичек. Как первичный, так и вторичный гипогонадизм могут быть врожденными и приобретенными. Проявлением гипогонадизма могут служить некоторые формы мужского бесплодия (от 40 до 60% всех случаев мужского бесплодия). В зависимости от возраста развития недостаточности половых гормонов различаются эмбриональная, допубертатная (от 0 до 12 лет) и постпубертатная формы гипогонадизма. Врожденный первичный (гипергонадотропный) гипогонадизм встречается:
Приобретенный первичный гипогонадизм развивается в результате воздействия на яички внутренних или внешних факторов после рождения.
Врожденный вторичный (гипогонадотропный) гипогонадизм развивается при состояниях:
Приобретенный вторичный гипогонадизм развивается при:
Причины и механизмы развития гипогонадизма у мужчинНедостаточность андрогенов может быть вызвана снижением количества вырабатываемых гормонов или нарушением их биосинтеза в результате патологии самих яичек или нарушения гипоталамо-гипофизарной регуляции. Этиологическими факторами первичного гипогонадизма нередко служат:
Некоторые случаи первичного гипогонадизма являются идиопатическими. Современная эндокринология не располагает достаточными данными об этиологии идиопатического гипогонадизма. При первичном гипогонадизме происходит снижение уровня андрогенов в крови, развитие компенсаторной реакции надпочечников на гипоандрогенизацию, возрастание продукции гонадотропинов. К вторичному гипогонадизму приводят нарушения гипоталамо-гипофизарной регуляции (воспалительные процессы, опухоли, сосудистые нарушения, патология эмбрионального развития). Развитие гипогонадизма могут вызывать аденомы гипофиза, продуцирующие гормон роста (при акромегалии) или адренокортикотропный гормон (при болезни Кушинга), пролактинома, послеоперационная или посттравматическая гипоталамо-гипофизарная дисфункция, гемохроматоз, процессы старения, сопровождающиеся возрастным снижением уровня тестостерона крови. При вторичном гипогонадизме отмечается низкий уровень гонадотропинов, приводящий к уменьшению секреции андрогенов яичками. Одной из форм мужского гипогонадизма является снижение продукции спермы при нормальном уровне тестостерона, а также крайне редкие случаи снижения уровня тестостерона без уменьшения продукции спермы. Симптомы гипогонадизма у мужчинКлинические проявления гипогонадизма обусловлены возрастом возникновения заболевания и степенью андрогенной недостаточности. Нарушение продукции андрогенов во внутриутробном периоде может приводить к развитию двуполых наружных половых органов. Если поражение яичек произошло у мальчиков в допубертатном периоде, происходит задержка полового развития, формируется типичный евнухоидизм: непропорционально высокий рост, связанный с запаздыванием окостенения эпифизарных (ростовых) зон, неразвитая грудная клетка и плечевой пояс, длинные конечности, слаборазвитая скелетная мускулатура. Может отмечаться развитие ожирения по женскому типу, истинной гинекомастии, гипогенитализма, что проявляется в малом размере полового члена, отсутствии пигментации и складчатости мошонки, гипоплазии яичек, недоразвитии предстательной железы, отсутствии оволосения на лице и лобке, недоразвитии гортани, высоком голосе. В случаях вторичного гипогонадизма часто возникает ожирение, возможна симптоматика гипофункции коры надпочечников, щитовидной железы, проявления пангипопитуитаризма, отсутствие полового влечения и потенции. Если снижение функции яичек развивается после завершения полового созревания, то симптомы гипогонадизма выражены слабее. Наблюдается уменьшение размеров яичек, незначительное оволосение лица и тела, жировые отложения по женскому типу, потеря эластичности и истончение кожи, бесплодие, снижение половой функции, вегетативно-сосудистые нарушения. Уменьшение яичек наблюдается почти во всех случаях мужского гипогонадизма (исключение – если заболевание началось недавно). Уменьшение размеров яичек обычно тесно связано с уменьшением выработки спермы. При утрате спермопродуцирующей функции яичек развивается бесплодие с прекращением продукции тестостерона, снижается либидо, возникает регрессия вторичных половых признаков, эректильная дисфункция, отмечаются генерализованные симптомы (снижение мышечной силы, утомляемость, общая слабость). Диагностика гипогонадизма у мужчинОсновывается на жалобах пациента, данных анамнеза, исследовании общего статуса с использованием антропометрии, осмотре и пальпации гениталий, оценке клинических симптомов гипогонадизма, степени полового созревания. По данным рентгенологического исследования оценивается костный возраст. Для определения минеральной насыщенности костей проводится денситометрия. При рентгенографии турецкого седла определяются его размеры и наличие опухоли. Оценка костного возраста позволяет по срокам окостенения лучезапястного сустава и кисти достаточно точно определить начало полового созревания. Начало полового созревания связывают с формированием сесамовидной кости в I пястно-фаланговом суставе (примерно в 13,5 — 14 лет). О полной половой зрелости свидетельствует появление анатомических синостозов. Этот признак дает возможность разграничить допубертатный возраст от пубертатного. Оценивая костный возраст, нужно учитывать возможность более раннего (для пациентов из южных районов) и позднего (для пациентов из северных районов) окостенения, а также то, что нарушение остеогенеза может быть обусловлено и другими факторами. При допубертатном гипогонадизме отмечается отставание на несколько лет «костного» возраста от паспортного. Лабораторное исследование анализа спермы (спермограмма) при гипогонадизме характеризуется азо- или олигоспермией; иногда эякулят получить не удается. Проводится измерение уровня половых и гонадотропинов: сывороточного тестостерона (общего и свободного), лютеинизирующего, фолликулостимулирующего гормона и гонадолиберина, а также антимюллеровского гормона сыворотки крови, пролактина, эстрадиола. Содержание тестостерона в крови снижено. При первичном гипогонадизме уровень гонадотропинов в крови повышен, при вторичном — понижен, иногда их содержание находится в пределах нормы. Определение уровня сывороточного эстрадиола необходимо при клинически выраженной феминизации и при вторичном гипогонадизме, в случае эстрагенпродуцирующих опухолей яичек или надпочечников. Уровень 17-КС (кетостероидов) в моче при гипогонадизме может быть в норме или снижен. При подозрении на синдром Клайнфелтера показано проведение хромосомного анализа. Биопсия яичек редко дает информацию для диагностики, а также оценки прогноза или лечения. Лечение гипогонадизма у мужчинТерапия гипогонадизма осуществляется строго индивидуально, и направлена на устранение причины заболевания. Цель проводимого лечения заключается в профилактике отставания полового развития, в дальнейшем — малигнизации тестикулярной ткани яичек и бесплодия. Лечение гипогонадизма должно осуществляться под контролем уролога и эндокринолога. Лечение гипогонадизма зависит от его клинической формы, выраженности нарушений в гипоталамо-гипофизарной и половой системах, сопутствующих патологий, времени возникновения болезни и возраста постановки диагноза. Терапию гипогонадизма начинают с лечения основного заболевания. Лечение взрослых пациентов состоит в коррекции недостаточности андрогенов и половой дисфункции. Бесплодие, возникшее на фоне врожденного и допубертатного гипогонадизма неизлечимо, особенно в случае аспермии. В случае первичного врожденного и приобретенного гипогонадизма (при сохраненных резервах эндокриноцитов в яичках) применяется стимулирующая терапия: у мальчиков — негормональными препаратами, а у взрослых пациентов — гормональными средствами (небольшие дозы гонадотропинов, андрогенов). При отсутствии резервной способности яичек показан заместительный прием андрогенов (тестостерона) постоянно, в течение всей жизни. При вторичном гипогонадизме и у детей, и у взрослых необходимо применять стимулирующую гормональную терапию гонадотропинами (при необходимости комбинируя их с половыми гормонами). Показано также проведение общеукрепляющей терапии, лечебной физкультуры. Оперативное лечение гипогоандизма состоит в трансплантации яичка, низведение яичка в случае крипторхизма, при недоразвии полового члена — фаллопластике. В косметических целях проводится имплантация синтетического яичка (при отсутствии неопустившегося яичка в брюшной полости). Операции осуществляются с использованием микрохирургической техники с контролем иммунологического и гормонального статуса пациента и пересаженного органа. В процессе систематического лечения гипогонадизма уменьшается андрогенная недостаточность: возобновляется развитие вторичных половых признаков, частично восстанавливается потенции, снижается выраженность сопутствующих проявлений, (остеопороза, отставания «костного возраста» и др.). Гипогонадизм у женщинЖенский гипогонадизм характеризуется недоразвитием и гипофункцией половых желез — яичников. Первичный гипогонадизм обусловлен либо врожденным недоразвитием яичников, либо повреждением их в период новорожденности. В организме возникает дефицит женских половых гормонов, что вызывает увеличение продукции гонадотропинов, стимулирующих яичники в гипофизе. В сыворотке крови отмечается высокий уровень фолликулостимулирующего и лютеинизирующего гормонов (гипергонадотропный гипогонадизм) и низкая концентрация эстрогенов. Дефицит эстрогенов вызывает недоразвитие и атрофические изменения женских половых органов, молочных желез, первичную аменорею. Если нарушение в яичниках возникло в допубертатный период, то вторичные половые признаки отсутствуют. Причинами первичного гипергонадотропного гипогонадизма являются врожденное генетическое нарушение (синдром Шерешевского-Тернера), врожденная гипоплазия яичников, инфекционные процессы (сифилис, туберкулез, эпидемический паротит), ионизирующее излучение (лучевое, рентгеновское), оперативное удаление яичников, аутоиммунное поражение яичников (аутоиммунный оофорит), синдром тестикулярной феминизации (врожденное состояние, при котором внешний вид человека соответствует женщине при мужском генотипе), синдром поликистозных яичников. Вторичный женский гипогонадизм (гипогонадотропный) возникает при гипоталамо-гипофизарной патологии, характеризуется дефицитом или полным прекращением синтеза и секреции гонадотропинов, регулирующих функцию яичников. Развивается вследствие воспалительных процессов в головном мозге (энцефалит, менингит, арахноидит), повреждающего действия опухолей головного мозга и сопровождается снижением стимулирующего действия гонадотропинов на функцию яичников. Симптомы гипогонадизма у женщинОдин из основных симптомов гипогонадизма в детородном периоде – нарушение менструального цикла и аменорея. Недостаток женских половых гормонов ведет к недоразвитию половых признаков: гениталий, молочных желез, нарушению отложения жировой клетчатки по женскому типу, скудному оволосению. Если заболевание врожденное, или оно возникло в раннем детском возрасте, то вторичные половые признаки отсутствуют. Характерны узкий таз и плоские ягодицы. Если гипогонадизм развился в пуберантном периоде, половые признаки, которые уже успели развиться, сохраняются, но менструации прекращаются, ткани женских гениталий подвергаются атрофии. Диагностика гипогонадизма у женщинПри гипогонадизме наблюдается заметное снижение содержания эстрогенов в крови, повышение уровня гонадотропинов (фолликулостимулирующего и лютеинизирующего гормонов). Ультразвуковое исследование выявляет матку, уменьшенную в размерах (гипоплазия матки), уменьшенные яичники. Рентгенография обнаруживает остеопороз или задержку формирования скелета. Лечение гипогонадизма у женщинПри первичном гипогонадизме у женщин назначается медикаментозная заместительная терапия женскими половыми гормонами (этинилэстрадиолом). В случае наступления менструальноподобной реакции, назначают комбинированные оральные контрацептивы, содержащие два типа гормонов — эстрогены и гестагены. Женщинам после 40 лет назначают эстрадиол + ципротерон, эстрадиол + норэтистерон. Заместительная гормональная терапия противопоказана при злокачественных опухолях молочных желез и половых органов, сердечно – сосудистых заболеваниях, болезнях почек, печени, тромбофлебите и др. Прогноз для жизни при гипогонадизме – благоприятный. Профилактика гипогонадизма состоит в медико-санитарном просвещении населения, наблюдении беременных женщин и охране их здоровья. Источник https://probolezny.ru/gipogonadizm-u-zhenshchin/ Источник https://altravita-ivf.ru/informatsiya-dlya-patsientov/spravochnik-zabolevanij/gipogonadizm-zhenskij-sz.html Источник https://www.krasotaimedicina.ru/diseases/zabolevanija_endocrinology/hypogonadism |