Чума: причины, симптомы, лечение
Чума у человека представляет острое, вызываемое особой бактерией, заболевание, протекающее в двух формах: бубонной и легочной.
Этиология
Заболевание вызывается чумной палочкой (Yersinia pestis из семейства Enterobacteriaceae), открытой в 1894 году в Гонконге.
Человек заражается чумой от блох, которые переносят бактерии от инфицированных грызунов (крысы, полевки, белки). Другой путь заражения – воздушно-капельный.

Клиническая картина
Чумное заболевание у человека может протекать в бубонной или легочной форме.
Бубонная чума
Инкубационный период длится 2-5 дней и никогда не превышает 10 дней. При типичном течении болезнь развивается внезапно: появляется озноб, головная боль, тошнота, иногда рвота. Температура в первый же день доходит до 39-40° C, больные жалуются па сильный упадок сил, бессонницу. Конъюнктивы часто гиперемированы, язык обложен толстым налетом, пульс очень учащен, мягок.
Общий вид чумных больных напоминает брюшнотифозных: лежат они пассивно, неподвижно, в полусонном состоянии, с полуоткрытыми глазами, на вопросы отвечают с трудом, неохотно, часто бредят. Иногда наоборот: замечается сильное возбуждение, больные непрерывно мечутся в постели, вскакивают, убегают. Обыкновенно уже в первый день заболевания можно констатировать наличие первичного бубона, реже в этом месте сначала ощущается боль. Иногда присутствие бубона обнаруживается только на 4-5-й день болезни.
По способу заражения необходимо отличать первичные и вторичные бубоны. В первичном бубоне прежде всего локализируется инфекция, занесенная по лимфатическим путям; вторичный бубон образуется благодаря заражению через кровеносные сосуды, то есть на почве бактериальной эмболии, источником которой всегда служит первичный бубон. Поражаются вторично почти все периферические железы, но увеличение их не достигает значительных размеров. Кроме того, от первичного бубона еще инфицируются через лимфатические пути соседние, лежащие по пути, железы, которые носят название первичных бубонов второго порядка. Таковы, например, паховые и подвздошные бубоны при первоначальном поражении бедренных желез соответствующей стороны или опухание подключичных и надключичных желез при появлении с той же стороны подмышечного лимфаденита.

Первичный бубон отличается от вторичных своей значительной величиной и резко выраженными изменениями в окружающих тканях (периаденит). Анатомически в бубоне констатируется геморрагическое воспаление, часто сопровождающееся некротическими изменениями и заканчивающееся иногда нагноением. Окружающая железу клетчатка пропитана кровоизлияниями и резко отечна. Увеличение железы обусловливается огромным количеством размножившихся чумных бацилл и излившейся кровью. Во вторичных бубонах изменения не так резки, часто в них имеется лишь мозговидное набухание и немногочисленные геморрагии; нагноение обычно отсутствует.
У некоторых больных первичный бубон благодаря малой величине и мягкой консистенции клинически не определяется, но на секционном столе его всегда можно найти со всеми присущими ему особенностям. Величина первичного бубона вначале колеблется от лесного ореха до волошского, но он может быстро увеличиваться и достигать размеров куриного яйца и даже большого яблока.
Увеличение идет не только за счет железы, но и периаденита, достигая максимума к концу первой недели. Периаденит, то есть инфильтрация и отек в окружности железы, иногда выражен очень резко, отечное припухание кожи может распространиться на большое протяжение, захватывая всю конечность или половину груди.
В первые дни контуры бубона прощупываются ясно и покрывающая его кожа часто не изменена, но вскоре благодаря периадениту контуры сглаживаются и становятся неясными, появляется воспалительное покраснение кожи. Почти постоянным признаком чумного бубона, кроме периаденита, нужно считать его значительную болезненность.
Дальнейшее течение чумы после появления первичного бубона отличается тем, что температура или носит характер постоянной, или имеются ремиссии, редко тип лихорадки бывает интермиттирующим. В случаях средней тяжести, не сопровождающихся осложнениями, спустя 10-12 дней больной перестает лихорадить, причем падение температуры до нормы происходит в течение 3-4-х дней. Параллельно улучшается самочувствие, болезненность лимфаденита уменьшается, периаденит начинает рассасываться, благодаря чему контуры железы выступают резче.
Полное восстановление бывает редко, обыкновенно бубон превращается в небольшую твердую эластичную опухоль, остающуюся на всю жизнь.
При бубонной чуме средней тяжести смертельный исход обычно наступает к концу первой недели и часто зависит от присоединившейся чумной септицемии.
Кроме описанной, наблюдаются тяжелые молниеносные формы бубонной чумы, когда спустя несколько часов развивается бессознательное состояние, бред, судороги, резкая болезненность на месте бубона и больной погибает спустя сутки после начала болезни.
В легких случаях (pestis minor) картина совершенно иная: больные остаются на ногах и даже исполняют обычные обязанности, некоторые только ложатся в постель, жалуясь на головную боль, тошноту, головокружение. Температура редко превышает 38° C. Спустя несколько дней болезненные симптомы проходят. При pestis minor местные признаки чумы выражаются лишь в незначительной болезненности и припухлости железы. Диагноз может быть установлен только бактериологически.
Легочная чума
Главными особенностями первичной чумной пневмонии являются быстрое течение и почти неминуемый смертельный исход в случае отсутствия лечения. После скрытого периода в 2-3 дня болезнь начинается остро, вскоре развивается сильный упадок сил, беспокойство, возбуждение, температура поднимается сразу до 39-40° C. Симптомы со стороны легких обнаруживаются спустя 1-2 дня, имеются жалобы на боль в боку, кашель и сильную одышку.
При исследовании находят признаки бронхита, позже явления катаральной, реже крупозной пневмонии. При аускультации прослушиваются сухие и мелкопузырчатые хрипы, иногда бронхиальное дыхание. Появляются симптомы сердечной слабости, пульс учащен, нитевидный. Больные легко, почти без кашлевых толчков, выделяют сначала окрашенную кровью мокроту, позже даже чистую кровь. Сознание у большинства теряется только незадолго до смерти. Спустя 2-6 дней наступает смертельный исход при явлениях одышки и расстройства сердечной деятельности.
В крови большинства больных обнаруживаются при посеве чумные палочки даже в ранние периоды болезни; в редких случаях их находят и в мазках из крови. В мокроте, особенно содержащей примесь крови, бацилл так много, что во время эпидемии для диагноза достаточно микроскопического исследования. Иногда к чумному процессу в легких присоединяется смешанная инфекция, чаще пневмококки и стрептококки.
На секции при первичной пневмонии легкие гиперемированы и содержат множество обширных кровоизлияний. Пневмонические фокусы желто-красного цвета, в желтых участках имеется густая инфильтрация лейкоцитами, в красных альвеолы сплошь выполнены кровью и бациллами. В бронхиальных железах определяется изменения, свойственные первичному бубону, в редких случаях эти железы не изменены.
Диагностика и прогноз
Диагноз по клиническим симптомам затруднителен у первых больных, особенно при легком течении процесса. Характерными признаками первичных чумных бубонов нужно считать значительную болезненность, быстро развивающиеся в окружности отек и инфильтрацию тканей, а также припухание соседних желез. Вообще чумные бубоны можно смешать с лимфаденитами, вызываемыми стрептококками, стафилококками и другими бактериями. На мысль о легочной чуме наводит тяжелое состояние больного и большая примесь крови в мокроте.
Точные указания дает бактериологический диагноз. Производится пункция с аспирацией бубона, добываются 1-2 капли жидкости, которая должна непременно содержать элементы лимфатической железы или гной. Часть пунктата сеется на агар, из остальной делаются мазки. В легких случаях чумы однократная, даже удачно произведенная пункция не всегда дает положительный результат.
У большинства больных уже в мазках можно найти биполярные палочки. При удачной пункции количество бактерий в препарате обыкновенно соответствует тяжести случая; при легком течении их очень мало.
Довольствоваться одной микроскопической картиной нельзя, необходимо получить культуры. Засеянные пробирки помещаются в термостат при 30° C; следует обратить внимание, чтобы посев делался не только на поверхность агара, но и в конденсационную воду, так как на мазках из последней вырастают характерные, иногда очень длинные цепочки. На вторые или на третьи сутки в пробирках имеется уже видимый рост.
Распознавание чумы ставится по исследованию не только мазка содержимого бубона и культур, необходимо еще произвести агглютинацию, пользуясь специфическими сыворотками с определенным достаточно высоким титром. Следует иметь в виду, что не все свежевыделенные разводки агглютинируются сывороткой, иногда реакция получается лишь после 2-3-х пересевов.
При отсутствии лечения при первичной пневмонии процент смертности составляет около 100%, при вторичной он значительно ниже. При бубонной чуме погибает от 30 до 90% больных. Прогноз зависит и от локализации первичных бубонов, самыми опасными являются поражения шейных желез. Прогноз ухудшается при наличии чумных палочек в крови, но выздоровление при этих условиях не исключается.
Лечение
Своевременная диагностика и применение соответствующего лечения зачастую позволяет избежать летального исхода, хотя по статистике и в таком случае 15% инфицированных людей умирает от чумы. Пациентам с чумой вводят антибиотики, например стрептомицин, тетрациклин, гентамицин или цефалоспорин.
Изоляция пациентов не всегда необходима; она показана только для людей, страдающих легочной чумой.
Лечение продолжается в среднем 2-3 недели.
Эта запись была размещена в Ч. Добавить в закладки постоянная ссылка.
Все представленные на сайте материалы предназначены исключительно для образовательных целей и не предназначены для медицинских консультаций, диагностики или лечения. Администрация сайта, редакторы и авторы статей не несут ответственности за любые последствия и убытки, которые могут возникнуть при использовании материалов сайта.
Смертельный поцелуй чумы
Статья на конкурс «био/мол/текст»: Возбудитель чумы как самая опасная бактерия в мире продолжает создавать угрозу безопасности мировому сообществу. Что делает его столь смертоносным? В статье рассмотрены основные причины уникальной патогенности чумного микроба на уровне биомолекул и их систем, а также обозначена перспектива поиска новых маркеров вирулентности.

Конкурс «био/мол/текст»-2017
Эта работа опубликована в номинации «Свободная тема» конкурса «био/мол/текст»-2017.

Генеральный спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

Спонсором приза зрительских симпатий и партнером номинации «Биомедицина сегодня и завтра» выступила фирма «Инвитро».

Один монах, странствуя по белому свету, встретил Чуму, которая направлялась в его город.
— Ты куда это направляешься, Чума? — спросил он ее.
— Иду в твой родной город, — ответила она. — Мне нужно забрать там тысячу жизней.
Через некоторое время монах снова встретил Чуму на своем пути.
— Почему ты меня обманула тогда? — спросил он ее с укором. — Ты говорила, что должна забрать тысячу жизней, а забрала пять тысяч.
— Я тогда сказала тебе правду, — ответила Чума. — Я действительно забрала тысячу жизней. Остальные умерли от страха.
Жертвы чумы исчислялись сотнями тысяч и даже миллионами человек, вымирали города, становились безлюдными целые области, и ужас пандемий чумы затмевал ужасы всех войн, какие знала история человечества. Целые тысячелетия люди не понимали, что является источником заболевания [2].
Библия — одно из древнейших дошедших до нас свидетельств эпидемий чумы (1 книга Царств, глава 5; 4 книга Царств, глава 19, стихи 35–36). В мировой истории отмечают три пандемии этой болезни:
- первая пандемия — «юстинианова чума» — по имени византийского императора Юстиниана, началась в Египте (542 г. н. э.) и охватила территорию всего цивилизованного мира;
- вторая пандемия — «черная смерть» (1340 г.) — неистово свирепствовала от Китая до Западной Европы и сопровождалась смертью около 25 млн. человек (примерно четвертой части тогдашнего населения Европы), а количество жертв во всем мире исчислялось 75 млн. человек [3];
- третья пандемия, зародившаяся в китайской провинции Юньнань в 1855 году, за несколько десятилетий распространилась на все обитаемые континенты. Только в Китае и Индии общее число умерших составило более 12 миллионов человек. По данным Всемирной организации здравоохранения, отголоски пандемии наблюдали и в 1959 году [4].
Крупные вспышки чумы регистрируют с определенной периодичностью (Индия — 1994 г.; Мадагаскар — 2011 и 2013 гг.). В США с 1965 по настоящее время ежегодно регистрируют до 40 случаев заражения людей чумой (в среднем 10 больных в год) [5]. В России в сентябре 2014 г. и в августе 2015 г. впервые за последние 35 лет были зарегистрированы два случая заражения человека чумой [6], [7].
Бубонная форма чумы является наиболее распространенной формой заболевания и при отсутствии лечения приводит к гибели 40–60% заболевших. Легочная форма возникает либо как осложнение бубонной или септической форм, либо при вдыхании воздуха, зараженного возбудителем чумы. Если лечение не начинают в первые 24 часа после появления симптомов, смерть наступает через 48 часов [8].
В природе чумной микроб встречается практически на всех континентах, исключая Австралию, Антарктиду, а также Арктику, что обусловливает ежегодно регистрируемые случаи этой болезни. Стремительная эволюция микроорганизмов приводит к появлению популяций бактерий (штаммов), устойчивых к антибиотикам [9], что в случае с возбудителем чумы особенно опасно. Кроме того, этих бактерий могут использовать в качестве агента биотерроризма. Все вышесказанное объясняет необходимость изучения чумного микроба.
Возбудитель чумы Yersinia pestis — самая опасная бактерия в мире [10]. Что делает ее столь смертоносной?
Факторы вирулентности, или вооружен и очень опасен
Любые патогенные бактерии должны обладать целым рядом свойств: «способностями» к инвазии (внедрению), колонизации, противостоянию иммунным реакциям организма хозяина и токсичностью. Биомолекулы, осуществляющие эти функции, называются факторами патогенности (вирулентности).
Со времен открытия возбудителя чумы в 1894 году французом Александром Йерсеном и японцем Китасато Сибасабуро ученые пытались выяснить, что определяет патогенность Y. рestis. В результате многолетней тяжелой и рискованной работы, которая продолжается и по сей день, выделили следующие факторы патогенности возбудителя:
- белки внешней мембраны (Yersinia outer proteins — называемые Yop-белками, эффекторными белками, или комплексом Yop-вирулона) [11];
- комплекс области пигментации [12];
- активатор плазминогена [13];
- капсульный антиген [14];
- пили адгезии или pH6-антиген [15].
Белки внешней мембраны, или зачем возбудителю чумы шприц?
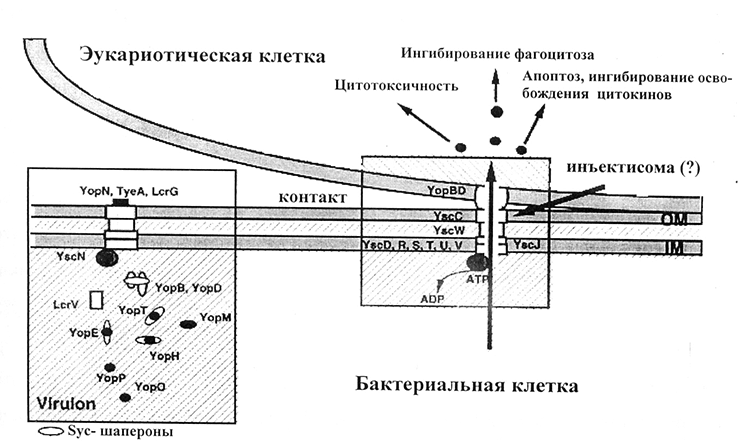
Изучение отдельных Yop-белков, а именно V- и W-антигенов, началось еще в 1956 году [16]. Описаны также YopM, YopN, YopH, YopE, YopD и другие белки [17]. Они подавляют развитие иммунных реакций, в частности, фагоцитоз, а при «заглатывании» микробов макрофагами (иммунными клетками) обеспечивают размножение возбудителя внутри макрофагов [11]. Белки внешней мембраны синтезируются только при температуре 37 °С и в условиях дефицита ионов кальция (low calcium response) [18]. Механизм действия Yop-белков — система секреции III типа — открыт в конце прошлого века [19]. Согласно этому механизму, чумной микроб, приблизившись к эукариотической клетке, впрыскивает эффекторные белки в цитоплазму (по принципу работы шприца с образованием особого канала — «иглы») (рис. 1) [20]. Особое внимание ученые уделяют V-антигену, так как на его основе создают химическую вакцину против чумы [21].
Комплекс области пигментации, или может ли стать потребность в чем-либо фактором патогенности?
В ходе лабораторных работ исследователи установили, что чумной микроб может стать авирулентным (безопасным) для мышей. При высеве таких бактерий на питательные среды с гемином (железосодержащим веществом, образующимся при действии соляной кислоты на гемоглобин) они образуют неокрашенные колонии, в отличие от пигментированных колоний вирулентных штаммов. Так появился один из простейших способов определения вирулентности штаммов возбудителя чумы без использования лабораторных животных. Если популяция бактерий на среде с гемином (среде Джексона—Берроуза) «дает» рост пигментированным колониям, то она является опасной (вирулентной), если непигментированным — то не опасной (авирулентной) [22].
Впоследствии выяснилось, что за окраску вирулентных колоний отвечают гены hms-локуса области пигментации на бактериальной хромосоме. В этой области пигментации также находится остров патогенности Y. pestis — HPI. Чем же примечательны гены этого острова и почему ему присвоили такое емкое название? Оказывается, для жизнедеятельности чумной бактерии необходимы ионы железа Fe 3+ . Захват и транспорт Fe 3+ в клетку осуществляют низкомолекулярные молекулы, обладающие высоким сродством к железу — сидерофоры [23]. Гены, кодирующие сидерофоры, и образуют остров патогенности. По крайней мере, одна сидерофорная система, а именно система синтеза и транспорта белка иерсиниобактина, обеспечивает активный транспорт железа у иерсиний. Однако вся область пигментации крайне нестабильна и может спонтанно делетироваться из хромосомы. Выпадение из генома сидерофорной системы приводит к значительному снижению вирулентности возбудителя чумы [24]. Поэтому потребность в железе стали рассматривать как детерминанту вирулентности чумного микроба. А поскольку при делеции области пигментации удаляется и hms-локус, кодирующий признак пигментсорбции, по этой «метке» начали разделять опасные и неопасные популяции иерсиний.
Активатор плазминогена, или двуликий Янус
Большое внимание уделяют омптинам — семейству протеаз наружных мембран, которые выполняют множество функций в бактериальной клетке, в том числе перенос различных веществ через внешнюю мембрану, и, в целом, способствуют адаптации микроорганизма к условиям окружающей среды. Один из них — активатор плазминогена (Pla) [25]. Еще до выделения Pla, специалисты приходили к противоречивым, на первый взгляд, выводам. С одной стороны, чумной микроб сворачивает плазму крови (плазмокоагулирующая активность), с другой стороны — предотвращает образование кровяного сгустка (фибринолитическая активность). Тем более удивительно, что обеими этими активностями, как впоследствии выяснилось, обладает один и тот же белок — активатор плазминогена. Оказалось, что при температуре ниже 30 °С Pla проявляет плазмокоагулирующую активность. В преджелудке зараженной блохи (переносчика чумных микробов) сворачивается кровь, поступившая из больного чумой грызуна, и образуется «блок» — резервуар для размножения иерсиний. При этом голодная блоха начинает активно кусать животное или человека, не чувствуя насыщения. При поступлении свежей порции крови возбудитель с «отрыжкой» блохи проникает в ранку и инфицирует ее. Попадая в другую среду с температурой 36–37 °С — температурой тела человека (или немного выше — теплокровного животного), — активатор плазминогена начинает действовать в прямо противоположном направлении: проявляет фибринолитическую активность — препятствует образованию кровяного сгустка в месте укуса и тем самым обеспечивает распространение возбудителя [26].
При вдыхании чумных микробов (и развитии легочной чумы) этот белок обеспечивает быстрое размножение бактерий в тканях легких и приводит к развитию молниеносной пневмонии и отеку легких, тогда как в отсутствии Pla инфекция не развивается в смертельную пневмонию. Установлено, что активатор плазминогена нарушает постоянство внутренней среды организма хозяина и блокирует иммунные реакции, направленные на уничтожение патогена [27].
Капсульный антиген, или скользкий тип этот возбудитель чумы
Бактерии окружены капсулой из слизистого вещества (фракция I, Fra1), которая препятствует поглощению и обезвреживанию Y. pestis иммунными клетками организма-хозяина в процессе фагоцитоза. На выявлении этого вещества-антигена основаны многие современные методы лабораторной диагностики чумы, оно входит в состав многих экспериментальных химических вакцин против чумы. Однако позднее обнаружили популяции бактерий, лишенные капсулы [28]. Кроме того, слизистая капсула есть у многих других микроорганизмов, например, возбудителя сибирской язвы, туляремии. Капсульное вещество иерсинии образуют при температуре 37 °С.
Пили адгезии (pH6-антиген), или «агент 007»
Специфический антиген pН6 (пили адгезии — мелкие ворсинки, белок PsaA) также синтезируется только при температуре 37 °С, но есть и еще одно условие — pН ниже 6,4 (что нашло отражение в его названии). Cчитается, что это значение рН близко к рН лизосом макрофагов или некротического содержимого абсцессов, где, вероятно, и синтезируется этот антиген. рН6-антиген ответственен за прикрепление чумных микробов к эпителиальным клеткам дыхательных путей и колонизацию их. Этот антиген интересен еще и тем, что подавляет фагоцитоз: при попадании иерсиний в кровь, pH6-антигены соединяются с аполипопротеинами В плазмы, что делает бактериальные клетки «невидимыми» для макрофагов [29]. Следовательно, в изначально агрессивном теплокровном организме хозяина популяции чумного микроба с рН6-антигеном имеют больше шансов на выживание, чем популяции возбудителя чумы без рН6-антигена — феномен селекции PsaA+ бактерий [30]. В природных очагах чумы выделяют только штаммы Y. pestis с рН6-антигеном.
Антигены, схожие с рН6, были обнаружены у ряда возбудителей, вызывающих менее опасные болезни — кишечные инфекции (Y. pseudotuberculosis [31], Y. enterocolitica [32], Escherichia coli [8]).
Температурный фактор, или то, что действительно имеет значение
Необходимо заострить внимание на особой роли температуры в физиологии чумного микроба. Именно при температуре 37 °С у него повышаются питательные потребности [33] и синтезируются практически все известные детерминанты вирулентности (рис. 2) [34]. У других бактерий подобная зависимость выражена в меньшей степени, что позволяет говорить о ведущей роли температурного фактора в вирулентности возбудителя чумы [8].
Геном или все важное внутри
Современные технологии позволили расшифровать геном чумного микроба , который, как выяснилось, имеет более чем 98-процентное сходство с относительно безобидной бактерией Y. pseudotuberculosis — эволюционным предшественником возбудителя чумы (событие 5–7-тысячелетней давности) [35]. Интересно, что приобретение уникальной вирулентности Y. pestis сопровождалось утратой части генов. Например, потеря чумным микробом гена, кодирующего адгезин А (YadA), — одного из важнейших факторов вирулентности возбудителя псевдотуберкулеза, — приводит к блокированию процесса образования внеклеточных нейтрофильных ловушек — самого эффективного на настоящий момент процесса уничтожения патогенов [36]. Нейтрофильные лейкоциты в отсутствии адгезина А не могут образовывать «ловчую сеть» из собственной ДНК и протеолитических ферментов, захватывать в нее бактерий и расщеплять их [37]. У возбудителя чумы также «беднее» набор генов эффекторных белков Yop-вирулона, чем у других представителей рода иерсиний [8].
О секвенировании генома иерсиний, вызвавших «черную смерть» 1340 года, читайте в материале «Это чума» [3]. — Ред.
Помимо хромосомы у чумного микроба есть плазмиды — внехромосомные участки ДНК [38]. Большинство белковых факторов вирулентности закодированы на плазмидах: эффекторные белки на плазмиде pCad; капсула — pFra; активатор плазминогена — рPla (pPst, pPCP). Плазмиды pFra и рPla обнаружены только у Y. pestis (видоспецифические), pCad является общей с возбудителем псевдотуберкулеза (родоспецифическая) [20].
Заключение
Несмотря на успехи, достигнутые в изучении чумного микроба, вопрос о ведущих факторах вирулентности его возбудителя остается открытым. Так отмечена «неодинаковая агрессивность» штаммов Y. pestis, обладающих одинаковым набором известных факторов патогенности [8].
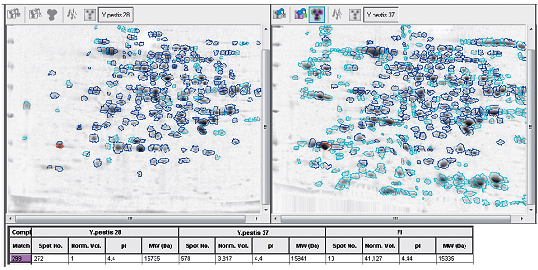
В настоящее время продолжается работа по выявлению новых, еще не изученных маркеров вирулентности [39]. С использованием 2D-электрофореза, масс-спектрометрии, полногеномного секвенирования проводят сравнительный анализ отличающихся по вирулентности популяций чумного микроба для выявления различий в их белковых спектрах и геномных последовательностях. Ранее не известные белки и участки генома становятся объектом пристального внимания и изучения как потенциальные детерминанты вирулентности.
Таким образом, патогенность возбудителя чумы — это множественный (полидетерминантный) признак. Соединение многих факторов в единое целое создает страшную угрозу чумных эпидемий, с противостоянием которым, однако, прогрессивное человечество успешно справляется.
Литература
- Частникова В. Еврейские притчи. Мудрец выше пророка. Litres, 2017. — 518 с.;
- Даниэл М. Тайные тропы носителей смерти / Под ред. Черкасского Б.Л. М.: «Прогресс», 1990. — 416 с.;
- Это чума;
- Википедия:Третья пандемия;
- Арутюнов Ю.И. (2016). Чума: случаи инфицирования людей в природных очагах США и сложность их выявления. ЖМЭИ. 6, 94–100;
- Кутырев В.В., Попова А.Ю., Ежлова Е.Б., Демина Ю.В., Пакскина Н.Д., Щучинов Л.В. с соавт. (2014). Заболевание человека чумой в Горно-Алтайском высокогорном природном очаге в 2014 г. Сообщение 1. Эпидемиологические и эпизоотологические особенности проявления чумы в Горно-Алтайском высокогорном (Сайлюгемском) природном очаге чумы. Проблемы особо опасных инфекций. 4, 9–16;
- Балахонов С.В., Ярыгин М.Б., Рождественский Е.Н., Базарова Г.Х., Витязева С.А., Остяк А.С. с соавт. (2016). Случай заболевания человека чумой в Кош-Агачском районе Республики Алтай в 2015 г. Сообщение 2. Микробиологическая и молекулярно-генетическая характеристика изолированных штаммов. Проблемы особо опасных инфекций. 4, 51–55;
- Домарадский И.В. Чума. М.: «Медицина», 1998. — 176 с.;
- Эволюция наперегонки, или Почему антибиотики перестают работать;
- Санитарно-эпидемиологические правила СП 1.3.3118-13 «Безопасность работы с микроорганизмами I–II групп патогенности (опасности)»;
- Gregory V. Plano, Kurt Schesser. (2013). The Yersinia pestis type III secretion system: expression, assembly and role in the evasion of host defenses. Immunol Res. 57, 237-245;
- Vladimir V. Kutyrev, Andrew A. Filippov, Olga S. Oparina, Olga A. Protsenko. (1992). Analysis of Yersinia pestis chromosomal determinants Pgm+ and Psts associated with virulence. Microbial Pathogenesis. 12, 177-186;
- Куклева Л.М. и Бойко А.В. (2016). Активатор плазминогена — многофункциональный белок возбудителя чумы. Проблемы особо опасных инфекций. 3, 13–20;
- Baker E.E., Sommer H., Foster L.E., Meyer E., Meyer K.F. (1952). Studies on immunization against plague. I. The isolation and characterization of the soluble antigen of the Pasteurella pestis. J. Immunol.68, 131–145;
- Linder L.E., Klempner M.S., Straley S.C. (1990). Yersinia pestis pH6 antigen genetic, biochemical and virulence characterization of a protein involved in the pathogenesis of bubonic plague. Infect. Immun.58, 2569–2577;
- Bacon G.A. and Burrows T.W. (1956). The basis of virulence in Pasteurella pestis: an antigen determining virulence. Brit. J. Exp. Pathol.37, 481–493;
- S. Felek, T. M. Tsang, E. S. Krukonis. (2010). Three Yersinia pestis Adhesins Facilitate Yop Delivery to Eukaryotic Cells and Contribute to Plague Virulence. Infection and Immunity. 78, 4134-4150;
- Goguen J., Yother J., Straley S. (1984). Genetic analysis of the low calcium response in Yersinia pestis mu d1 (Ap-lac) insertion mutants. J. Bacteriol.160, 842–848;
- Å. Forsberg, A.-M. Viitanen, M. Skurnik, H. Wolf-Watz. (1991). The surface-located YopN protein is involved in calcium signal transduction in Yersinia pseudotuberculosis . Unknown journal title.. 5, 977-986;
- Cornelis G.R., Boland A., Boyd A.P., Geuijen C., Iriarte M., Neyt C. et al. (1998). The virulence plasmid of Yersinia, an antihost genom. Microbiol. Mol. Biol. Rev.62, 1315–1352;
- Hill J., Williamson E., Titball R. (2009). Vaccine against Yersinia comprising one or two antibodies, one specific for Yersinia pestis F1-antigen and the other one for Yersinia pestis V-antigen. Patent US7572449 B2;
- Аракелян И.С., Кенжебаева К.Ж., Сулейменов Б.М., Некрасова Л.Е. (2002). Способ дифференциации популяции чумного микроба Yersinia pestis по Psb+ признаку. Патент 12419 (Казахстан);
- Ракин А. и Газетти Д. (2013). Различные сидерофоры обуславливают фенотип высокой патогенности иерсиний. Проблемы особо опасных инфекций. 3, 58–62;
- R. D. Perry, P. B. Balbo, H. A. Jones, J. D. Fetherston, E. DeMoll. (1999). Yersiniabactin from Yersinia pestis: biochemical characterization of the siderophore and its role in iron transport and regulation. Microbiology. 145, 1181-1190;
- Richard W Titball, Petra C F Oyston. (2007). A plague upon fibrin. Nat Med. 13, 253-254;
- W. W. Lathem, P. A. Price, V. L. Miller, W. E. Goldman. (2007). A Plasminogen-Activating Protease Specifically Controls the Development of Primary Pneumonic Plague. Science. 315, 509-513;
- J. L. Eddy, J. A. Schroeder, D. L. Zimbler, A. J. Caulfield, W. W. Lathem. (2016). Proteolysis of plasminogen activator inhibitor-1 by Yersinia pestis remodulates the host environment to promote virulence. J Thromb Haemost. 14, 1833-1843;
- Кадникова Л.А., Копылов П.Х., Дентовская С.В., Анисимов А.П. (2015). Капсульный антиген чумного микроба. Инфекция и иммунитет. 5, 201–218;
- X.-Z. Huang, L. E. Lindler. (2004). The pH 6 Antigen Is an Antiphagocytic Factor Produced by Yersinia pestis Independent of Yersinia Outer Proteins and Capsule Antigen. Infection and Immunity. 72, 7212-7219;
- Бахтеева И.В. Исследование функциональной активности рН6 антигена Yersinia pestis с помощью наборов изогенных мутантов: автореф. . канд. мед. наук. — Москва, 2008;
- Luther E. Lindler, Ben D. Tall. (1993). Yersinia pestis pH 6 antigen forms fimbriae and is induced by intracellular association with macrophages. Mol Microbiol. 8, 311-324;
- Maite Iriarte, Jean-Claude Vanooteghem, Isabelle Delor, Ramon Diaz, Stuart Knutton, Guy R. Cornelis. (1993). The Myf fibrillae of Yersinia enterocolitica. Mol Microbiol. 9, 507-520;
- Балтазар М. (1964). Стойкость чумы в постоянных очагах. Журн. Гиг. Эпидемиол. (Прага). 8, 333–343;
- Полунина Т.А., Заднова С.П., Краснов Я.М. (2017). Применение 2D-электрофореза для получения белкового спектра фракций экзопротеинов возбудителей чумы и холеры. Проблемы особо опасных инфекций. 2, 40–44;
- Черная смерть. История о том, как безобидная бактерия стала беспощадной убийцей;
- V. Brinkmann. (2004). Neutrophil Extracellular Traps Kill Bacteria. Science. 303, 1532-1535;
- Salome Casutt-Meyer, Francesco Renzi, Mathias Schmaler, Naja J. Jann, Marlise Amstutz, Guy R. Cornelis. (2010). Oligomeric Coiled-Coil Adhesin YadA Is a Double-Edged Sword. PLoS ONE. 5, e15159;
- Мобильные генетические элементы прокариот: стратификация «общества» бродяжек и домоседов;
- Красильникова Е.А., Копылов П.Х., Шайхутдинова Р.З., Иванов С.А., Дентовская С.В., Анисимов А.П. Поиск факторов, отвечающих за избирательную вирулентность Yersinia pestis // Молекулярная диагностика 2017: сб. трудов. Тамбов: ООО фирма «Юлис», 2017. С. 316–317.
Чума

Чума — одна из наиболее опасных для человека бактериальных инфекционных заболеваний. За последние 2000 лет история человечества помнит три масштабных эпидемии, а за 300 лет в Европе эта инфекция унесла жизни 25 миллионов человек. Многие люди считают, что чума осталась далеко в прошлом и в современном мире встретиться с ней едва ли возможно. Это не так. Несмотря на строгие эпидемиологические меры, наличие эффективных вакцин и антибиотиков болезнь продолжает угрожать человечеству. Мы расскажем, в каких странах и регионах РФ наиболее высок риск заражения, на какие симптомы нужно обратить внимание и как лечат заболевание.
Как можно заразиться чумой
Возможностей подцепить «чумной микроб» существует множество. Человеку достаточно контакта с любым носителем или переносчиком. Заразным может оказаться дикое животное, которое, к примеру, было убито на охоте. При его разделке бактерия может попасть на кожу человека. Так, в 2014-2015 годах на Алтае двое охотников заразились чумой, разделывая сурков. Инфекция проникла в организм через мелкие повреждения на коже. До этого с 1961 года на территории РФ чума у людей не регистрировалась ни разу. Похожий случай произошел в 2013 году с 15-летним подростком в Киргизии, который пожарил шашлык из сурка, предварительно разделав его 7 .

Меры предосторожности
Если вы отправляетесь в район, который признан природным очагом чумы, помните о следующих правилах:
- Используйте средства для защиты от насекомых, особенно блох (спреи, мази).
- Не прикасайтесь к животным, не будучи уверенными в том, что они не инфицированы.
- Не прикасайтесь к тканям любых умерших животных, их выделениям, биологическим жидкостям (крови).
- Регулярно мойте руки с мылом или дезинфицируйте их спиртосодержащим раствором.
- Подвергайте овощи и фрукты тепловой обработке кипятком, не употребляйте некипяченое молоко и воду.
Заразиться чумой (и принести ее в дом) может собака — при контакте с инфицированными дикими особями, почвой, водой. Инфекция может поражать лошадей, овец, коров. При употреблении в пищу недостаточно обработанного мяса этих животных или молока возможно заражение. Но в основном люди заражаются от крысиных блох, которые при укусе выбрасывают бактерии в кровь или на поверхность кожи. Кроме того, достаточно даже блошиного помета, который остался на поверхности тела. Однако заразится можно далеко не от любой блохи, а только от той, которая до этого паразитировала на зараженном чумой животном (крысе 7 ).
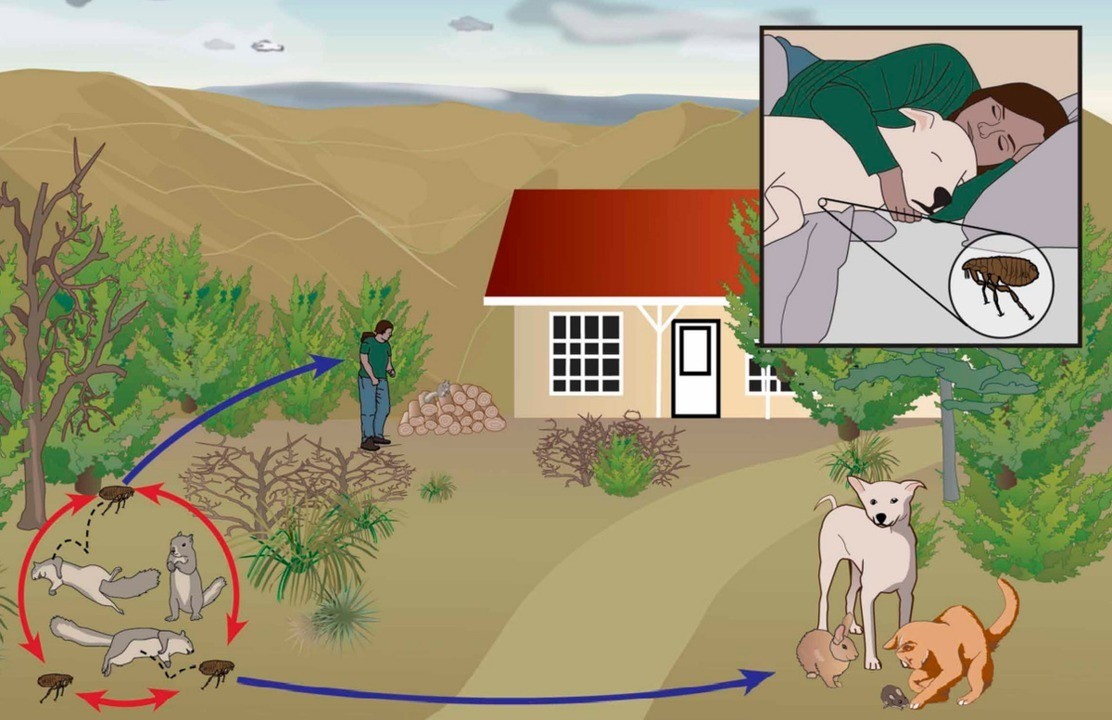
Еще один путь заражения — воздушно-капельный. Он наиболее опасный, так как любой зараженный человек или животное легко и постоянно выделяет возбудителя чумы в воздух. При этой форме заболевания — легочной чуме — инфекция распространяется максимально быстро.

Как внешне определить больного
Из-за обширной интоксикации организма, возникающей в результате деятельности бактерий, человек ведет себя неадекватно. В различных исследованиях ученые отмечают, что поведение больного можно принять за поведение человека в состоянии алкогольного опьянения:
- возбужденное состояние;
- беспокойство;
- невнятная речь;
- притупленный слух;
- шаткая и неуверенная походка;
- опухшее, покрасневшее лицо с отсутствующим выражением;
- живые, блестящие, но неподвижные глаза.
Следует обратить внимание на язык — на нем образуется известково-белый налет, похожий на мел. Больной жалуется на жар внизу живота и постоянно просить пить. Однако питье не утоляет жажду. Далее начинаются озноб и рвота. На основании этих признаков любой врач может диагностировать тяжелую интоксикацию. Однако они еще не дают основания поставить уверенный диагноз «чума».
Какие симптомы должны вызвать тревогу
Первые признаки могут проявиться спустя 1-7 суток после заражения. Именно таков инкубационный период Yersinia Pestis, возбудителя чумы. Наиболее распространены три формы чумы — бубонная, септическая и легочная. Сейчас около 75% всех клинических случаев приходится на бубонную чуму, около 17% — на септическую и около 8% — на легочную 7 . Они имеют свои отличительные признаки, о которых мы расскажем ниже. Однако в качестве общих симптомов для всех форм Всемирная организация здравоохранения выделяет:
- резкое повышение температуры тела;
- озноб;
- головную боль;
- ломоту в теле;
- слабость;
- тошноту;
- рвоту.
Типичные признаки чумы, характерные практически для любого клинического случая — резкое начало и головная боль. Болезнь всегда протекает в острой форме.

Известен случай в одной из южных республик СССР, когда пациенту с симптомами сильной интоксикации отказали в медицинской помощи под предлогом, что он находится в состоянии алкогольного опьянения. К сожалению, через несколько часов мужчину нашли во дворе поликлиники без признаков жизни. Посмертно у него была диагностирована чума 7 .
Лечение чумы
Любого пациента с подозрением на это заболевание немедленно госпитализируют и изолируют. Лечебные мероприятия начинают без промедлений. В основном, это антибактериальная и дезинтоксикационная терапия.

Еще в середине ХХ века были созданы антибиотики, которые успешно борются с возбудителем чумы. Это аминогликозиды, тетрациклины, левомицетин. Их назначают в дозе, которая соответствует форме болезни.
Одним из наиболее эффективных антибиотиков считается стрептомицин. Его вводят внутримышечно 2 раза в день в течение 10 суток. Распространена схема терапии с применением гентамицина, доксициклина, хлорамфеникола, хлорамфеникола. В любом случае стандартная антибактериальная терапия длится 10 суток. Доксициклин имеет ограничения для применения в случаях заражения беременных женщин. Хлорамфеникол не применяют для лечения детей.
Однако одной лишь антибактериальной терапии недостаточно, так как организм больного страдает от тяжелой интоксикации.
- Для восстановления объема выделяемой мочи назначают салуретики. К ним относят препараты с действующими веществами фуросемид, этакриновая кислота.
- Для улучшения гемодинамики (движения крови) используют глюкокортикостероидные препараты.
При проведении дезинтоксикационной терапии важно вывести токсины, скорректировать показатели гемостаза, стабилизировать кровообращение и функции жизненно важных органов. Для этого пациенту внутривенно (через капельницу) вводят трансфузии глюкозосолевых растворов и коллоидов: альбумин, раствор Рингера-Локка и другие.

С созданием антибиотиков, вакцин и антибактериальных лекарств лечение чумы не представляет проблемы. Однако крайне важно своевременно обратиться за медицинской помощью при первых симптомах. Если терапия начата вовремя, причин для волнения нет — прогноз практически всегда благоприятный.
Возбудитель чумы
Причина болезни — палочковидная бактерия Yersinia pestis (чумная палочка), которая, по данным исследований, существует уже более 20 тыс. лет. В народе ее называют «чумным микробом». Она стремительно размножается в питательных средах и передается множеством способов. Наиболее опасен воздушно-капельный.

Факты о «чумном микробе»
- Хорошо переносит замораживание, например, при –22 о С может существовать до 4 месяцев. А при высокой температуре — погибает. При +50. +70 о С — через 10 минут, в кипятке — через 1 минуту.
- Не переносит прямой солнечный свет и погибает за 2-3 часа.
- Содержится в любых выделениях зараженного организма: слюне, мокроте и т.д.
- Может сохраняться в молоке, воде, в почве, на овощах, фруктах. В частности, на одежде — до 6 месяцев.
Бактерия чумы относится к крайне агрессивным по отношению к человеческому организму и при отсутствии лечения приводит к летальному исходу. Болезнь развивается эпидемически или пандемически, как правило, с высокой летальностью 7 , поэтому ее относят к особо опасным.

В Демократической республике Конго, на Мадагаскаре и в Перу каждый год фиксируют вспышки чумы. Это наиболее неблагоприятные страны с точки зрения риска заражения. В остальном мире природные очаги зафиксированы в Казахстане, Туркменистане, Узбекистане, Монголии, Китае, Индии, Мадагаскаре, Мозамбике, Уганде, Танзании, Бразилии, Боливии, Эквадоре.
Российским туристам, бизнесменам, сотрудникам фирм, которые пребывают в этих странах, нужно знать, где именно находятся природные очаги чумы. И предпринимать меры для того, чтобы снизить риск инфицирования 7 .
Кто переносит инфекцию
Носители инфекции — различные грызуны (крысы, полевые мыши, землеройки, песчанки и полевки) и некоторые животные, в основном, обитающие в степной зоне. Это зайцы, суслики, сурки, тарбаганы, ежи. Они выделяют возбудителя чумы с пометом, бактерии содержатся в умерших животных — так они попадают в воду, почву, откуда разносятся далее другими особями. Переносчиками же выступают чаще всего блохи, которые паразитируют на носителях, живут в почве³.

Осторожно! Чума!
Ученые выделяют множество природных очагов чумы. Это географические места, где циркулирует данная инфекция. Такие места формировались тысячелетиями, а главное условие для циркуляции Yersinia pestis — наличие большого количества носителей и переносчиков. Природные очаги заболевания занимают около 7% суши. Исключительно «привозная» чума существует только в Австралии и Антарктиде. На остальных континентах есть области, где риск заражения максимально высокий.
Так как для природных очагов характерно наличие большого количества грызунов (чаще всего сусликов), то сосредоточены они, в основном, в степной и лесостепной зоне 9 . В России это:
- Ингушетия.
- Тыва (Овюрский и Монгун-Тайгинский районы).
- Горный Алтай (Кош-Агачский район).
- Кабардино-Балкария (Тырныаузский, Баксанский, Эльбрусский, Зольский районы).
- Карачаево-Черкессия (Карачаевский, Малокарачаевский районы).
- Дагестан (Тарумовский, Бабаюртский, Кизлярский, Кулинский, Агульский, Ногайский, Буйнакский районы).
- Калмыкия (Черноземельский, Яшкульский, Каспийский, Ики-Бурильский районы).
- Чеченская республика.
- Ставропольской край (Курской район).
- Астраханская область (Черноярский, Наримановский, Лиманский районы).
В РФ эпидемическую обстановку называют неустойчивой, так как в стране есть природные очаги инфекции, Россия граничит со странами, где неоднократно регистрировались вспышки чумы 7 .

Последние крупные вспышки
Всемирная организация здравоохранения подсчитала, что в 2003-2011 годах в 16 странах Азии, Африки и Америки произошло 15 243 случая инфицирования чумой. Летальный исход наступил в 5,9%. В целом же почти 98% всех случаев заражения и более 96% летальных исходов приходятся на Африку 5 .
- В 2004 году несколько животных и людей заболели предположительно бубонной чумой в Туркмении и Узбекистане.
- В 2005-2006 годах 1304 случая легочной чумы зафиксировали в Демократической республике Конго. На данный момент это самое опасное место на Земле.
- В августе 2009 года в связи со вспышкой заболевания был изолирован город Зикетан в провинции Цинхай.
- В августе 2010 года в Перу (провинция Аскопе департамента Ла-Либертад) 17 человек заболели легочной и бубонной чумой.
- В 2010 году на Мадагаскаре заразились более 300 человек, в 2014-м — более 100. Мадагаскар — второе по опасности место, где регулярно фиксируют вспышки заболевания 5 .
Видео 1. Вспышка бубонной чумы в Китае. Как побеждали болезнь
Какие симптомы заметны при первом клиническом обследовании
При первичном физикальном осмотре врач в большинстве случаев фиксирует резкую тахикардию. Сердце пациента бьется с такой неравномерностью, что иногда сложно подсчитать частоту пульса. Он может становиться нитевидным. При осмотре также заметны признаки сердечной и почечной недостаточности. Живот вздувается, а моча приобретает выраженный темный оттенок. Эти и вышеперечисленные симптомы характерны в начальный период развития чумы. Далее появляются признаки местных, общих поражений, которые свидетельствуют об определенной форме заболевания.
Летальный исход возможен и в начальный период — если заболевание развивается молниеносно. Организм переживает сильнейший инфекционно-токсический шок и может не справиться.
Симптомы бубонной чумы
Название этой формы заболевания происходит от арабского и греческого слов «джума» и «бубон», обозначающих «боб» и «пах». Характерный признак — воспаление лимфоузлов в паху (более 50% случаев). Воспаленные лимфоузлы внешне напоминают бобы, фасоль. Бубоны появляются уже через несколько часов после истинного начала болезни. Они развиваются также в подмышках (около 20% случаев), под челюстью и на шее. Мелкие напоминают размерами лесной орех, крупные — куриной яйцо. Бубоны сильно болят, поэтому пациент старается принять позу, при которой воспаленный лимфоузел не затрагивается.
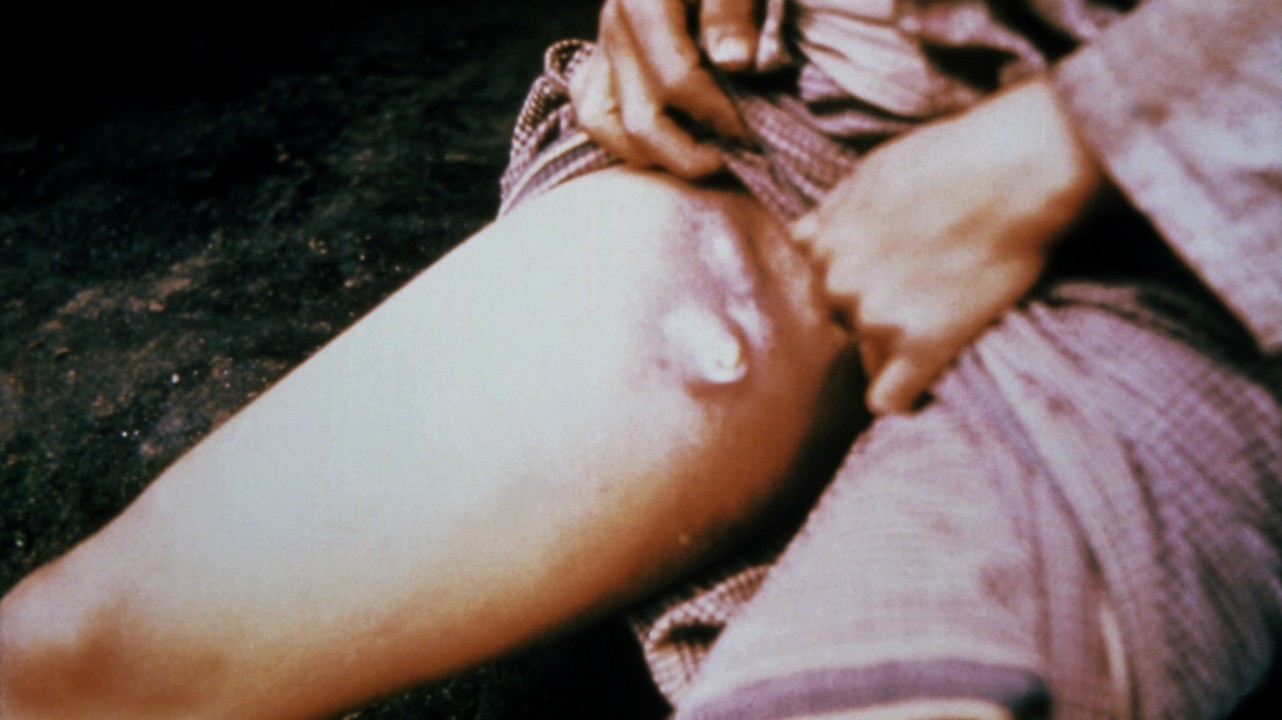
- Чаще всего у человека появляется один бубон в паху. Воспаление затрагивает соседние ткани, кожу, поэтому спустя сутки бубон напоминает плотную опухоль с четкими границами, которая отличается острой болезненностью.
- В подмышечной впадине опухоль может иметь желеобразную консистенцию. Опасность представляет распространение инфекции в легкие.
- Бубоны на шее максимально опасны, сопровождаются массивным отеком тканей вплоть до лопаток и нижней части груди. Состояние больного по мере распространения отека по голове значительно ухудшается. Возможно развитие менингита.
Как протекает бубонная чума
Пик клинических проявлений бубонной чумы наступает на 4-6 сутки, когда интоксикация организма достигает максимума. У пациента постоянно держится высокая температура около 40°С, его лихорадит. Лицо покрасневшее и отечное, на нем часто появляется выражение ужаса. При физикальном осмотре заметны нарушения работы сердца, увеличение печени. Артериальное давление снижается. Уже на этом этапе у пациента с низким иммунитетом возможен летальный исход.
Если же больной переживает пик заболевания, то на 6-8 сутки бубон заметно краснеет и отекает, а еще через 2 суток вскрывается. Из него выделяется гной желто-зеленого цвета, в котором могут присутствовать следы крови. Явного запаха гной не имеет. В этот период пациенту становится значительно лучше. Если организм не атаковала вторичная инфекция, прогноз благоприятный. Зарастание гнойного свища происходит медленно — в течение 3-4 недель. На его месте образуется глубокий рубец.
В любой момент заболевания до прорыва бубона может произойти распространение инфекции на другие лимфоузлы и образование вторичных бубонов. Это одно из самых распространенных осложнений.

Температура при бубонной чуме
- В ряде случаев за 1-2 суток до появления бубона пациента беспокоит лихорадка с высокой температурой. После начала воспаления температура стабильно высокая — 39-40 о С.
- Если она начала постепенно и стабильно снижаться — это положительный признак.
- Если произошло резкое снижение и последующее также резкое повышение — это, напротив, свидетельствует о сепсисе и значительном ухудшении и неблагоприятным прогнозом.
Источник https://el-klinika.ru/chuma-prichiny-simptomy-lechenie/
Источник https://biomolecula.ru/articles/smertelnyi-potselui-chumy
Источник https://medportal.ru/enc/infection/exotic/9/