Рак простаты (предстательной железы)
Рак простаты — патология, проявляющаяся в виде злокачественного новообразования в тканях данной железы. Ранние стадии заболевания характеризуются отсутствием выраженной симптоматики. Некоторые пациенты сталкиваются с учащенными позывами к мочеиспусканию (в т. ч. по ночам), болями в тазовой области, ощущением неполного опустошения мочевого пузыря. Урологи часто связывают перечисленные симптомы с хроническим простатитом или аденомой простаты, диагностированными у пациентов ранее.
Статистика заболеваемости
Рак простаты — третья по распространенности онкологическая патология среди мужчин (уступает только раку легких и желудка). В группу риска ходят возрастные пациенты, но в последние десятилетия онкологи стали выявлять злокачественные новообразования предстательной железы у лиц 35–40 лет (до 10% пациентов). Около 30% случаев рака простаты выявляются на третьей–четвертой стадиях, когда опухоль становится неоперабельной. Часто патология протекает бессимптомно, что затрудняет обнаружение новообразований до появления метастазов.
Причины развития патологии
Современная онкология относит злокачественные поражения простаты к заболеваниям с неясной этиологией. Основным фактором риска остается возраст пациента. До 70% мужчин с подтвержденным диагнозом «рак простаты» оказываются старше 65 лет. Вероятность развития патологического процесса в железе увеличивается при систематическом употреблении пациентами избыточного количества животных жиров и прохождении ЗГТ на фоне дефицита тестостерона. Онкологи из Соединенных Штатов установили, что причинами рака простаты могут стать вазэктомия и дефицит витамина D.
Классификация патологии
Злокачественные новообразования предстательной железы делятся на четыре основных типа:
- аденокарциномы;
- переходно-клеточный рак;
- плоскоклеточный рак;
- недифференцированный рак.
Наиболее распространенной гистологической формой патологии остается аденокарцинома. Железистые опухоли выявляются в 90% клинически регистрируемых случаев.
При разработке курса лечения на фоне рака предстательной железы онкологи используют шкалу Глисона. Эта методика основана на изучении степени дифференцировки клеток в биоптате — тканях простаты, полученных во время биопсии. Каждому образцу присваивается оценка в диапазоне от 1 до 5. Результат двух исследований суммируется. Показатели интерпретируются следующим образом:
- 2–6 баллов — опухоль с высокой дифференцировкой клеток, новообразование неагрессивно, растет медленно;
- 7 баллов — опухоль со средней дифференцировкой клеток, агрессивность новообразования умеренная;
- 8–10 баллов — опухоль с низкой дифференцировкой клеток, новообразование агрессивно, растет быстро.
Подтвержденные характеристики опухоли позволяют онкологам выбрать наиболее эффективный метод лечения рака простаты.
Симптоматика патологии
Симптомы рака простаты на ранних стадия неспецифичны. Дискомфорт, который испытывает пациент, рассматривается урологами как следствие простатита. Лица, страдающие от злокачественной патологии, сталкиваются с учащенными позывами к мочеиспусканию в ночные часы, струя мочи становится прерывистой, поток оказывается неравномерным.
По мере роста опухоли появляются иные признаки рака простаты: жжение во время семяизвержения и мочеиспускания, присутствие крови в моче и эякуляте, боли в поясничном отделе позвоночника, эректильная дисфункция. На фоне этой симптоматики пациент обращается к урологу или онкологу. В большинстве случаев злокачественные новообразования в железистых структурах выявляются случайно.
Диагностические процедуры
Наличие у мужчины одного или нескольких симптомов рака простаты становится причиной для обращения в клинику. Во время осмотра пациента онколог проводит пальцевое исследование предстательной железы через стенку прямой кишки. Эта мера направлена на оценку размеров простаты и ее плотности, наличия в тканях пальпируемых новообразований. Пальпация не позволяет дифференцировать злокачественные опухоли и хронический простатит, гиперплазию или туберкулез. Подтверждение первичного диагноза выполняется с помощью лабораторных и аппаратных исследований.
Врачи-онкологи направляют пациента на следующие диагностические процедуры:
- ПСА-анализ крови — рост концентрации простат-специфического антигена указывает на злокачественный процесс;
- ультразвуковое исследование железы — позволяет визуализировать раковые очаги, выполняется трансабдоминально или трансректально;
- биопсия предстательной железы — забор биоптата проводится из двенадцати точек (по шесть на каждую долю органа).
В качестве дополнительных диагностических приемов применяются УЗИ брюшной полости, рентгенография легких, сцинтиграфия скелета. Эти процедуры позволяют обнаружить метастазы в организме пациента или подтвердить их отсутствие.
Терапия при подтвержденном диагнозе
Лечение рака простаты предполагает применение хирургических методов, радиотерапии и химической терапии . Порядок применения перечисленных методик определяется врачом-онкологом на основании данных анамнеза пациента, результатов лабораторных тестов и аппаратных исследований.

Малоинвазивные способы лечения применяются при низком онкологическом риске или наличии у мужчины противопоказаний к проведению хирургического вмешательства. Наибольшее распространение в онкологических центрах получили:
- HIFU-терапия, направленная на разрушение злокачественной опухоли посредством фокусированного ультразвука высокой интенсивности;
- брахитерапия, обеспечивающая радиотерапевтический эффект посредством размещения в тканях простаты источника излучения.
При отсутствии у пациента противопоказаний к оперативному вмешательству хирурги выполняют простатэктомию. Радикальная методика предполагает удаление предстательной железы, семенных пузырьков, простатического отдела мочеиспускательного канала и шейки мочевого пузыря. Побочными эффектами процедуры становятся эректильная дисфункция и недержание мочи. Перед проведением операции пациент проходит курсы химио– и радиотерапии. Эта мера призвана замедлить рост опухоли и повысить эффективность хирургического вмешательства.
Часто гормональная и химическая терапия применяются после резекции простаты. Аналогичное лечение назначается пациентам, которые страдают от неоперабельной опухоли простаты с метастазами в брюшной полости, лимфатических узлах или костной ткани.
Эффективность терапии
Онкологи формируют прогноз выживаемости при раке предстательной железы с учетом стадии патологического процесса и дифференцировки опухолевых клеток, выявленных у пациента. На ранних этапах развития злокачественного новообразования радикальная простатэктомия остается наиболее эффективным методом лечения. Пятилетняя выживаемость пациентов после операции достигает 85%, десятилетняя — 60%. Лучевая терапия простаты обеспечивает показатели на уровне 75% и 50% соответственно. Гормональные способы лечения патологии позволяют добиться пятилетней выживаемости пациентов в 55% случаев.
Профилактические меры
Современная онкология не может предложить пациентам действенные методы профилактики рассматриваемой патологии. Мужчинам старше 45 лет рекомендуется регулярно посещать уролога для пальцевого исследования простаты, УЗИ её тканей и сдачи ПСА-анализа крови.
Диагностика и лечение рака предстательной железы в Москве
Институт ядерной медицины (Московская область, г. Химки, квартал «Клязьма») обладает всем необходимым оборудованием для диагностики и лечения злокачественных новообразований простаты. Прием пациентов осуществляется в современном амбулаторно-диагностическом комплексе, построенном с учетом последних достижений онкологии и радиологии.
Вопросы и ответы
— Как проявляется патология?
— На начальных стадиях развития злокачественной опухоли пациенты сталкиваются с частыми позывами к мочеиспусканию и затрудненным оттоком жидкости из мочевого пузыря. Позднее к этим симптомам присоединяются боли в поясничном отделе позвоночника, следы крови в моче и эякуляте, жжение при семяизвержении и мочеиспускании.
— Поддается ли лечению рак простаты?
— Основными методами лечения патологии становятся хирургические вмешательства, лучевая терапия и химиотерапия. Некоторым пациентам в качестве паллиативного лечения назначается прием гормональных препаратов.
— Какова продолжительность жизни пациентов с раком простаты?
— Прогноз формируется онкологом на основании формы рака и стадии патологического процесса. Наибольшей эффективностью обладает радикальная простатэктомия, обеспечивающая пятилетнюю выживаемость в 85% случаев.
Рак предстательной железы (рак простаты) — симптомы и лечение
Что такое рак предстательной железы (рак простаты)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Скатова Бориса Валерьевича, уролога со стажем в 29 лет.
Над статьей доктора Скатова Бориса Валерьевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Уролог Cтаж — 29 лет
Медицинский центр «Рефлекс»
Клиника «Бионика»
Дата публикации 27 апреля 2018 Обновлено 29 октября 2021
Определение болезни. Причины заболевания
Рак предстательной железы (РПЖ) — это злокачественное новообразование, развивающееся из патологических клеток предстательной железы. Рак предстательной железы является самым распространённым новообразованием у мужчин старше 50 лет и характеризуется значительной летальностью (свыше 16% в отдельных случаях), занимая второе место в структуре смертности после рака лёгких. [1]
Предстательная железа — особый орган мочеполовой системы мужчин, расположенный в промежутке между прямой кишкой, лобковой костью и мочевым пузырём, охватывает значительный участок мочеиспускательного канала. Простата вырабатывает гормоны и сок простаты, являющийся средой для жизни сперматозоидов, при попадании их в матку участвует в регуляции мочеиспускания.
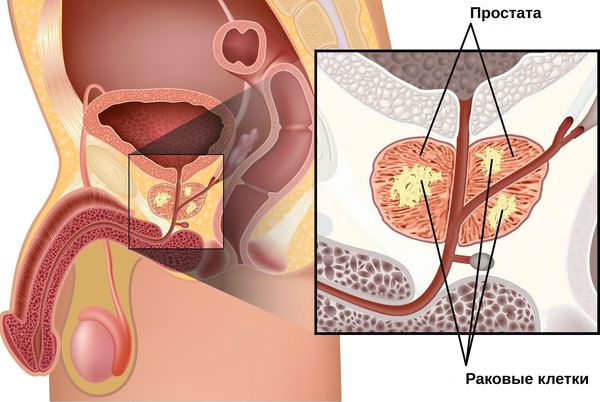
Наиболее высокий процент заболевания РПЖ наблюдается в США, Канаде, а также в некоторых европейских странах — там болезнь занимает первое место среди всех онкологических заболеваний. Согласно данным Национального института рака (National Cancer Institute, США), с 1986 по 1992 год процент заболеваемости раком простаты среди белокожего населения вырос на 108% и на 102% — для афроамериканцев. [2]
Уровень заболеваемости РПЖ на территории России также неумолимо увеличивается. В 2006 году впервые было выявлено 18 092 случая рака предстательной железы, а стандартизованный показатель равнялся 21,4 на 100 тысяч населения. Прирост заболеваемости с 1996 по 2006 год составил 94,84% при учёте среднего темпа прироста за 2006 год — 6,9%.
Прирост летальности от рака простаты за последние 20 лет составил 58,76%. Такой прирост равнозначен распространению самой настоящей эпидемии. Так, в США в 2016 году было заявлено 272843 (а в 2009 году — 207789) первичных выявлений рака предстательной железы, приведших к 29225 летальным случаям в 2009 году. По данным европейских урологов, в 2017 году заболеваемость в Европе составила 219 случаев на 1000 мужчин. В России, согласно эпидемиологическим данным Чиссова В.И., в 2012 году впервые выявлено 24911 случаев рака предстательной железы. [3]
Следует понимать, что интенсивный прирост заболеваемости раком предстательной железы связан, в частности, с широким внедрением в клиническую практику новейших диагностических методов обследования пациентов среднего и пожилого возраста. Огромное значение имеет определение ПСА в качестве скрининга мужчин старше 50 лет, основанный на выявлении простатического специфического антигена в крови и моче мужчин. Например, в 60-х и 70-х годах прошлого века, при отсутствии данной методики, рак предстательной железы выявляли только на поздних стадиях уже в крайне запущенном состоянии. [4]
Частота распространения онкологии этой локализации неодинакова в разных регионах, а также среди лиц разных профессий и представителей определённых национальностей. Чаще всего рак предстательной железы выявляется у североамериканцев и европейцев, реже всего у азиатов. [5]
Причины заболевания раком предстательной железы:
- гормональная возрастная перестройка организма;
- качественное изменение цикла синтеза тестостерона;
- генетическая предрасположенность (наличие подобных заболеваний у ближайших родственников);
- высокий уровень сывороточного тестостерона;
- загрязнение окружающей среды, чрезмерное употребление синтетических и жирных продуктов;
- работа на вредных производствах;
- злоупотребление бытовыми наркотиками (никотин, алкоголь);
- наличие «предраковых» заболеваний (простатит, гиперплазия предстательной железы).
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы рака предстательной железы
Как распознать первые симптомы рака простаты
Следует знать, что рак предстательной железы на ранних стадиях протекает совершенно бессимптомно.
По мере распространения опухоли и появления метастазов начинают проявляться определённые клинические симптомы:
- частое, иногда затруднённое мочеиспускание;
- слабая («вялая») струя мочи;
- возникновение чувства, что мочевой пузырь опорожнён не полностью;
- задержки нормального мочеиспускания, запоры;
- недержание мочи;
- болевые ощущения различной интенсивности в промежности, крестце, головке полового члена, внизу живота, пояснице;
- наличие крови в моче и сперме;
- отёк нижних конечностей;
- параплегия (онемение нижних конечностей) при компрессии (сдавлении) спинного мозга;
- заметное снижение массы тела, истощение (кахексия);
- анемия (снижение гемоглобина) и уремия. [6]
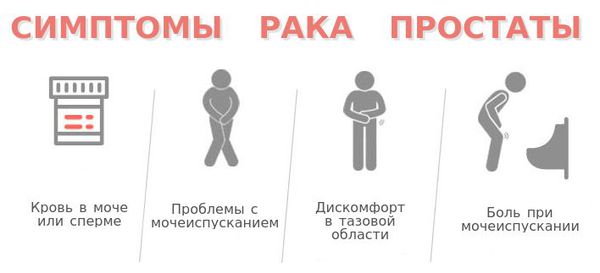
Патогенез рака предстательной железы
Причины, по которым возникает рак простаты, разнообразны и до конца не установлены. Выделяют следующие механизмы молекулярного возникновения РПЖ:
- Внутри трансформированных клеток простаты происходят множественные видоизменения синтеза генов, которые контролируют пролиферацию (новообразование клеток). Повышается уровень образования факторов роста и их рецепторов, осуществляется активация сигнальных каскадов, связанных с андрогенновыми и эстрогенновыми рецепторами, увеличивается активность эмбриональных сигнальных путей, характерных для стволовых клеток. Совокупность этих компонентов придаёт изменённым клеткам простаты агрессивные свойства, стимулирует их избыточное деление, миграцию и метастатическую активность.
- В клетках предстательной железы, которые начали злокачественно перерождаться, нарушается экспрессия генов и белков, контролирующих апоптоз (механизм, обеспечивающий выживание клеток опухоли, развитие их устойчивости к химиотерапии).
- Генетические мутации и разнообразные генетические факторы играют важную роль в развитии рака простаты, сигнальных белков, которые стимулируют более поздние стадии канцерогенеза — канцероматозный неоангиогенез (образование сосудов, снабжающих развивающуюся опухоль кислородом и питательными веществами). [7]
Классификация и стадии развития рака предстательной железы
Классификация рака предстательной железы по системе TNM
Классификацию стадий развития рака разработал французский хирург Пьер Денуа в 1952 году. В дальнейшем она была многократно переработана. В 2002 году было принято решение о прекращении внесения изменений до возникновения радикальных перемен в диагностике и лечении злокачественных опухолей. Идею новой знаковой классификации по системе TNM поддержали национальные комитеты TNM различных стран, данная система получила признание во всём мире. Классификация 2002 года помогает интерпретации полученных результатов, оптимизирует алгоритмы лечения. Система TNM в последней редакции повсеместно используется в установлении диагноза и определении стадии рака предстательной железы.
Т — опухоль первичная:
— ТX — недостаточно сведений для интерпретации первичной опухоли;
— Т0 — первичная опухоль не выявляется;
— Т1 — клинических проявлений опухоли нет, она не проявляется при пальпации, её не удаётся визуализировать специальными методами:
- Т1а — опухоль случайно обнаруживается при гистологическом исследовании и составляет менее 5% ткани, полученной при биопсии;
- Т1b — опухоль случайно обнаруживается при гистологическом исследовании и составляет более 5% ткани, полученной при биопсии;
- Т1с — опухоль диагностируется при помощи игольчатой биопсии простаты, которая производится по причине высокого уровня ПСА);
— Т2 — опухоль, ограниченная предстательной железой или распространённая в капсуле:
- Т2а — опухоль поражает меньше половины или половину одной доли;
- Т2b — опухоль поражает более половины одной доли (но не две доли);
- Т2c — опухоль поражает две доли;
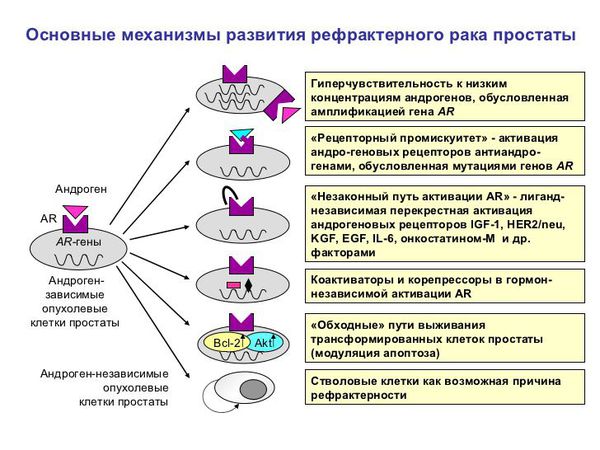
— Т3 — опухоль распространяется за пределы капсулы предстательной железы:
- Т3а — опухоль распространяется за пределы капсулы (одно- или двустороннее распространение);
- Т3b — опухоль распространяется на семенной пузырёк;
— Т4 — несмещаемая опухоль или опухоль, которая распространяется на соседние ткани и органы, но не на семенные пузырьки: шейку мочевого пузыря, наружный сфинктер, прямую кишку, мышцу, поднимающую задний проход, и/или тазовую стенку.
N — регионарные лимфоузлы
Регионарные лимфоузлы предстательной железы — это узлы малого таза, находящиеся ниже бифуркации общих подвздошных артерий. Категория N не зависит от стороны локализации регионарных метастазов.
— NX — недостаточно данных для оценки регионарных лимфоузлов;
— N0 — отсутствие метастаз в регионарных лимфоузлах;
— N1 — метастазы в регионарных лимфоузлах присутствуют.
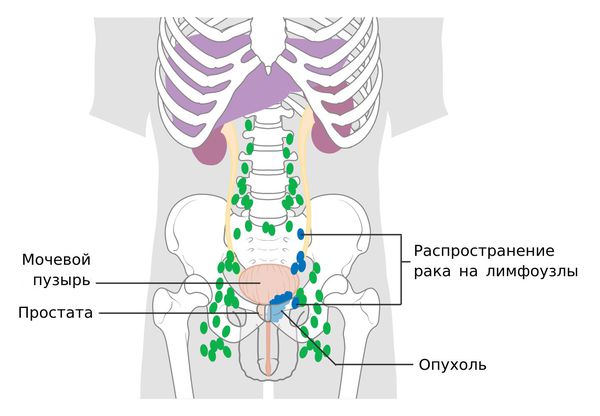
M — отдалённые метастазы:
— МX — определение наличия отдалённых метастазов невозможно;
— М0 — признаки отдалённых метастазов отсутствуют;
— М1 — присутствие отдалённых метастазов:
- M1a — поражение регионарных лимфатических узлов;
- M1b — происходит поражение костей;
- M1c — возникают отдалённые метастазы иных локализаций (в лёгких, печени и т.д.).
Классификация рака простаты по шкале Глисона (Gleason score)
Шкала Глисона позволяет определить степень злокачественности опухоли, выявленной при биопсии предстательной железы. Об уровне опасности опухоли свидетельствуют набранные баллы по данной шкале: чем бал больше, тем опаснее опухоль. В основе оценки опухоли лежит сравнение раковых клеток, полученных при биопсии простаты, с нормальными клетками. Так, отсутствие отличия раковых клеток от обычных позволяет оценить опухоль в 1 балл по шкале Глисона. При радикальном отличии клеток опухоли ставится максимальная оценка в 5 баллов.
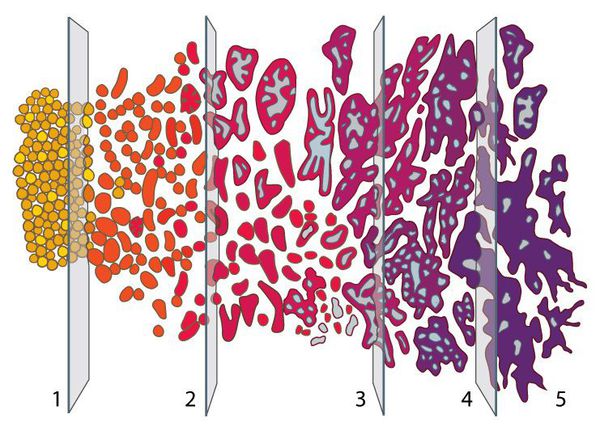
Степень злокачественной опухоли определяется по сумме Глисона, то есть путём суммирования баллов данной шкалы (от 1 до 5) по двум самым обширным и злокачественным новообразованиям, которые обнаружили в тканях предстательной железы.
Оценка злокачественных опухолей по сумме Глисона:
- умеренно выраженные, если сумма Глисона ≤ 6 баллам;
- средне выраженные, если сумма Глисона = 7 баллам;
- высоко выраженные, если сумма Глисона = 8-10 баллам.
Классификация рака простаты по системе Джюит-Уайтмор
По системе Джюит-Уайтмора классификация рака предстательной железы делится на стадии: А, В, С и D. Стадии А и В — излечимы, стадии С и D также вылечиваются, но прогноз их излечения менее благоприятный.
Стадия А. Она является самой ранней стадией. Симптомы не проявляются, хотя раковые клетки уже локализуются в простате:
- А 1 — дифференциация раковых клеток хорошая, аномалия клеток умеренная;
- А 2 — умеренная или плохая дифференциация раковых клеток в нескольких участках простаты.
Стадия В. Опухоль не выходит за пределы простаты. Определяется при пальпировании, и/или фиксируется повышенный уровень ПСА:
- В 0 — опухоль в пределах простаты, не пальпируется; повышенный уровень ПСА;
- В 1 — наличие одиночного опухолевого узла в одной доле простаты;
- В 2 — экстенсивный рост опухоли в одной или в обеих долях простаты.
Стадия С. Опухоль выходит за пределы капсулы простаты и распространяется на соседние ткани и органы, включая семенные пузырьки:
- С 1 — прорастание опухоли за пределы капсулы простаты;
- С 2 — перекрытие просвета уретры или мочевого пузыря опухолью.
Стадия D. Опухоль распространяет метастазы в регионарные лимфатические узлы или в отдалённые органы и ткани (лёгкие, печень, кости, желудок и т. д.):
- D 0 — клиническое обнаружение метастаз при повышенном уровне ПСА;
- D1 — поражение регионарных лимфоузлов;
- D2 — поражение отдаленных лимфоузлов, органов и тканей;
- D3 — метастазы после лечения. [8][9][10]
Осложнения рака предстательной железы
Метастазы при раке простаты
Раковые клетки продвигаются через соединительную ткань и в результате проникают внутрь кровеносной или лимфатической системы. Затем они переносятся с кровью или лимфой, пока не закрепятся на новом месте, — так образуются метастазы.
Наиболее часто метастазы рака простаты поражают кости. При этом возникает боль в поражённой костной ткани, иногда в отдалённых участках. Если сдавливается нерв, боль может отдавать в другие участки, особенно такое характерно для рук и ног. При поражении метастазами позвоночника часто сдавливается спинной мозг и возникают переломы. Сдавливание нервных стволов может приводить к различным неврологическим симптомам: боли, парестезии (ощущению покалывания, жжения, «ползания мурашек»), гиперестезии (повышенной чувствительности) и т. д.
Помимо костей, метастазы рака простаты часто развиваются в лимфоузлах. Выделяют поражение ближайших лимфатических узлов и отдалённых. Если опухоль распадается и продукты её распада разносятся по организму, метастазы могут появиться в любом лимфатическом узле. Увеличенные лимфоузлы сдавливают органы, что приводит к нарушению их работы и характерным проявлениям. Симптомы зависят от того, где именно локализовались очаги опухоли.
Диагностика рака предстательной железы
Пальцевое исследование предстательной железы через прямую кишку (задний проход) долгое время являлось основным и чуть ли не единственным методом диагностики рака простаты. Метод не потерял своего значения и на сегодняшний день. Специфической характеристикой РПЖ при ректальном исследовании является плотность узлов в одной или двух долях предстательной железы, доходящая до так называемой «каменистости». Однако низкий процент выявления первичного рака простаты (меньше 6% по последним данным), при развитии более информативных методов, постепенно сводит диагностическую ценность метода к минимуму. Кроме того, пальцевое исследование приводит к ложному повышению уровня простатического специфического антигена в результате вынужденной стимуляции предстательной железы. [11] [12]
Простатический специфический антиген (ПСА) является онкомаркером рака предстательной железы и обладает высокой чувствительностью и хорошей специфичностью в отношении данного процесса. ПСА — это белок гликопротеин, который может вырабатываться только эпителием простаты. При раке он старается блокировать развитие клеток эндотелия простаты.
В норме содержание ПСА в крови равно 4,0 нг/мл. Значения 4,0-10,0 нг/мл являются промежуточными (так называемая «серая зона»), а более 10,0 нг/мл — диагностически значимые. ПСА является калликреиноподобной сериновой протеазой, секретируемой клетками эпителия предстательной железы. Этот маркер считается не опухолеспецифическим, а органоспецифическим, в связи с этим сывороточный уровень ПСА может увеличиваться не только при раке простате, но и при доброкачественной гиперплазии предстательной железы, хроническом простатите, а также при любой стимуляции предстательной железы. [13]
Простатический специфический антиген 3 (ПСА 3) (PCA 3 (Prostate Cancer Gen 3) важен при решении вопроса о повторной биопсии после отрицательного результата первоначально проведённого исследования. PCA — наиболее значимый новый биомаркер. Антиген определяется в моче после 3-кратного массажа предстательной железы во время ректального исследования. Показатель РСА 3 превосходит чувствительность общего ПСА и свободного ПСА. Показатель РСА 3 стоит применять вместе с ПСА и иными клиническими факторами риска в номограммах или других системах стратификации риска для того, чтобы принять решение о проведении первичной или повторной биопсии. Считается, что уровень РСА 3 повышается с увеличением объёма РПЖ. [14]
Индекс здоровья простаты (показатель PHI — Prostate healthindex). Его определение основано на определении фракции свободного ПСА (-2проПСА). [15]
Инструментальная диагностика
Ультразвуковое исследование рака предстательной железы (трансректальное УЗИ предстательной железы, ТРУЗИ). Эхографическая диагностика рака предстательной железы неоднозначна. Классическая ультразвуковая картина представлена гипоэхогенными очаговыми зонами в периферических отделах предстательной железы. С увеличением площади опухолевых очагов эти зоны содержат как гипо-, так и гиперэхогенные участки. 40 % опухолей предстательной железы, которые диагностированы при биопсии, представлены изоэхогенными участками. [16]
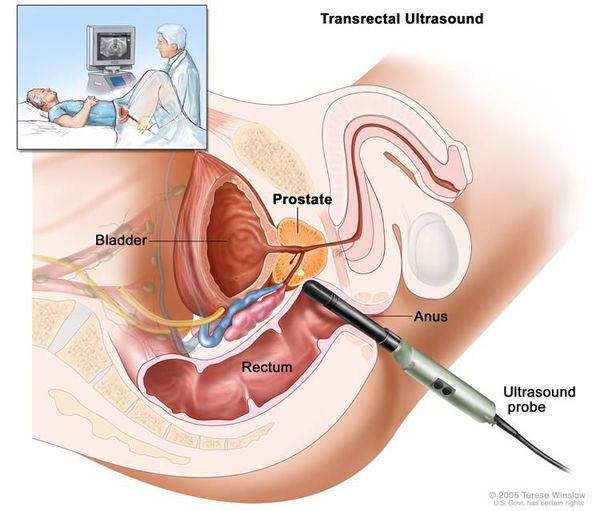
ТРУЗИ проводится для решения двух первоочерёдных задач:
- Выявление патологических участков в предстательной железе, в которых подозревается рак;
- Повышение точности трансректальной биопсии предстательной железы.
Биопсия простаты — самый точный метод диагностики рака предстательной железы. Стандартная методика выполнения биопсии предстательной железы — трансректальная биопсия под контролем трансректального УЗИ, которая обязательно выполняется, как минимум, из 12 точек. Проводится по результатам одного из трёх методов диагностики: пальцевого ректального исследования, определения концентрации ПСА в сыворотке крови и ТРУЗИ. [17]
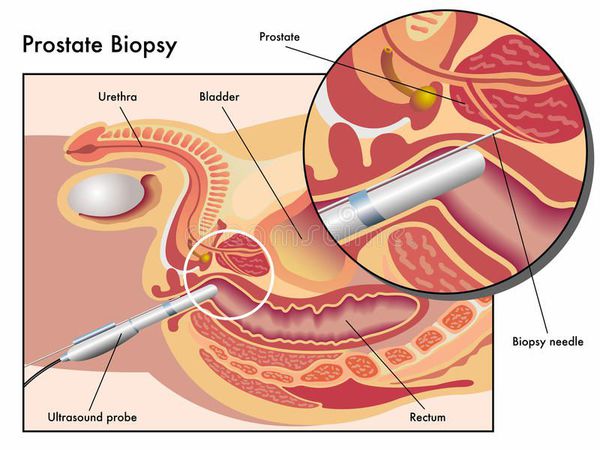
Магнитно-резонансная томографии (МРТ) предстательной железы является наиболее чувствительным методом диагностики экстрапростатической инвазии опухоли, а применение динамической магнитно-резонансной простатовезикулографии с помощью контрастного усиления и эндоректальной магнитной катушки повышает точность диагностики ещё на 18%. [18]
Компьютерная томография (КТ). Выполнение КТ предстательной железы для определения стадии процесса не рекомендуется, так как КТ предстательной железы менее информативна, чем МРТ, для дифференциальной диагностики локализованного и экстрапростатического процесса. КТ чаще назначают для планирования дистанционной лучевой терапии (ДЛТ) (ссылка). [19]
Методы диагностики отдалённых метастазов. Для диагностики отдалённых метастазов рекомендуются следующие методы:
- сцинтиграфия скелета;
- УЗИ, КТ, МРТ органов брюшной полости;
- рентгенографическое исследование, КТ органов грудной клетки;
- рекомендуется определять уровень активности щелочной фосфатазы в сыворотке крови, являющейся косвенным признаком метастатического поражения скелета (выявляется у 70% больных с генерализацией процесса). [20]
Радиоизотопное исследование (сканирование) скелета применяется при первичном обследовании пациентов с высоким баллом злокачественного роста по шкале Gleason, высоким уровнем ПСА (> 10 нг/мл) и щелочной фосфатазы или при выраженном болевом синдроме (в таком случае риск костных метастазов достаточно высок).
Для радиоизотопного исследования внутривенно вводят аналог пирофосфата, объединённый с радиоактивным изотопом технеция-99.
Через три часа после введения препарата (пирофосфат + технеций-99), когда изотоп накопился в костной ткани, пациента укладывают на диагностический стол и с помощью гамма-камеры исследуют расположение радиоактивной метки в костной ткани. Обработка информации происходит с помощью компьютерной программы. Доза радиации, получаемая пациентом при обследовании, очень мала и безопасна.
Лечение рака предстательной железы
Радикальная простатэктомия (РПЭ) — полное удаление простаты
Хирургическое вмешательство в объёме полной простатэктомии является наиболее радикальным методом лечения. Большинство урологов рекомендуют радикальную простатэктомию как метод выбора при лечении локализованного рака предстательной железы. Под таким оперативным лечением подразумевается удаление предстательной железы с семенными пузырьками и участком мочеиспускательного канала. Целью операции при локализованном и некоторых вариантах местно распространённого РПЖ является полное излечение пациента. В редких случаях полное удаление простаты нацелено на паллиативную помощь при лечении местно распространённого процесса, т. е. для улучшения состояния больного. В этих случаях задача операции состоит в удалении основной массы опухоли для повышения эффективности консервативного лечения.
Радикальное хирургическое лечение обычно проводится у пациентов с РПЖ локализованной формы с ожидаемой продолжительностью жизни более 10 лет.
Варианты операционного доступа при выполнении радикальной простатэктомии:
- позадилонный;
- промежностный;
- лапароскопический (с помощью робота).
Показания к радикальной простатэктомии:
- опухоли T1a G1-G2 при ожидаемой продолжительности жизни более 15 лет; опухоли T1a G3; опухоли T1b-T2с; опухоли Т3а; ограниченная экстракапсулярная инвазия.
Преимущества радикальной простатэктомии перед консервативными методами лечения:
- полное удаление интракапсулярной опухоли;
- точное определение стадии опухолевого процесса;
- излечение сопутствующей доброкачественной гиперплазии предстательной железы, имеющей клинические проявления. [21]
В последние несколько лет стала широко применяться лапароскопическая радикальная простатэктомия, которую можно выполнить чрезбрюшинным или внебрюшинным доступами. Применение данной техники позволяет снизить число осложнений и ускорить процесс реабилитации больных.
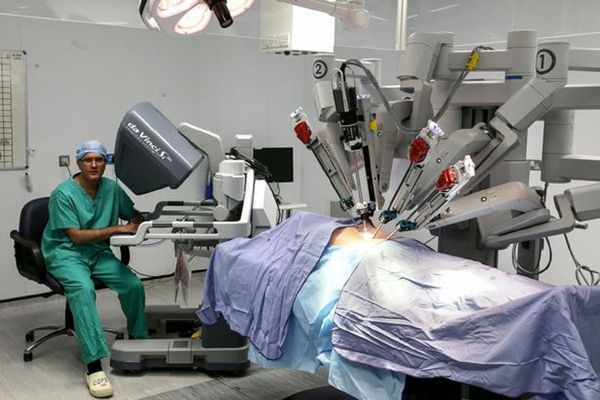
Один из вариантов лапароскопической операции — робот-ассистированная радикальная простатэктомия (согласно материалам Guidelines EAU 2015 года — клинического руководства Европейской ассоциации урологов). Робот-ассистированная радикальная простатэктомия (РАРП) активно «вытесняет» РПЭ в качестве «золотого стандарта» оперативного лечения локализованного рака простаты во всём мире. [22] При РАРП, по сравнению с РПЭ, достоверно уменьшается объём кровопотери, имеются преимущества при оценке восстановления удержания мочи и эректильной функции. [14]
Лучевая терапия (ЛТ)
Как и простатэктомия, лучевую терапию относят к радикальным методам лечения локализованного рака простаты. При местно распространённом РПЖ, ЛТ проводят для того, чтобы улучшить выживаемость больных, и чаще в сочетании с гормонотерапией. Цель лучевой терапии — максимально точное достижение терапевтической дозы ионизирующего излучения в ткани предстательной железы при условии минимального лучевого воздействия на окружающие органы и ткани. [23]
Брахитерапия (внутритканевая ЛТ) — имплантация радиоактивных источников в ткань предстательной железы. Для терапии РПЖ применяется постоянная (низкодозная) и временная (высокодозная) брахитерапия. Для временной брахитерапии применяют изотоп 192 Ir. Удаление радиоактивных игл осуществляется после подведения необходимой дозы к предстательной железе. Высокодозную брахитерапию применяют при местно распространённом РПЖ (T3 N0 M0), комбинируя с дистанционным облучением. При локализованном РПЖ чаще применяют постоянную брахитерапию: в предстательную железу вводятся радиоактивные гранулы 125I (период полураспада — 60 дней) или 103Pd (период полураспада — 17 дней). Более локализованное распределение ионизирующего излучения при брахитерапии позволяет подвести более высокую дозу облучения к предстательной железе с меньшим лучевым воздействием на окружающие ткани, чем при проведении дистанционной ЛТ. Внедрение радиоактивных источников производится через промежность под контролем трансректального УЗИ. Доза облучения при имплантации 125I составляет 140-160 гр, при имплантации 103Pd — 115-120 гр. [24]
Минимально инвазивные методы лечения РПЖ
К минимально инвазивным методам лечения РПЖ относятся криоабляция простаты и абляция предстательной железы с помощью высокоинтенсивного сфокусированного ультразвука — HIFU (англ. High Intensity Focused Ultrasound). Криоабляция простаты — хорошо изученный альтернативный метод терапии РПЖ, в то время как метод HIFU до конца не изучен. Фокальная терапия РПЖ с помощью различных методик, таких как криоабляция, ультразвуковая или лазерная абляция и пр.) активно изучается во многих клиниках. [14]
Гормональная терапия
Гормонотерапия, в качестве самостоятельного способа лечения РПЖ, рекомендуется с паллиативной целью. В то же время назначение гормональных препаратов может быть показано в сочетании с радикальным оперативным или лучевым лечением в качестве комбинированной противоопухолевой терапии. Основой механизма действия эндокринного лечения является снижение концентрации тестостерона в клетках предстательной железы, реализованное одним из следующих способов:
- подавление яичками секреции андрогенов (снижается концентрация сывороточного тестостерона);
- конкурентное взаимодействие с андрогенными рецепторами в ядрах клеток предстательной железы (снижается внутриклеточная концентрация тестостерона, уровень сывороточного тестостерона не уменьшается).
К методам гормонотерапии относят:
- двустороннюю орхидэктомию (удаление обоих яичек);
- терапию агонистами лютеинизирующего гормона рилизинг-гормона (ЛГРГ) — используются препараты гозерелин, лейпрорелин, трипторелин, бусерелин;
- терапию антагонистами ЛГРГ (дегареликс);
- эстрогенотерапию (диэтилстильбэстрол);
- максимальную (комбинированную) андрогенную блокаду;
- монотерапию антиандрогенами (стероидные — ципротерон, мегестрол и хлормадинон; нестероидные — бикалутамид, флутамид, нилутамид). [14][25]
Гормональные препараты других классов
Рекомендуется принимать кетоконазол — противогрибковый препарат, угнетающий синтез андрогенов надпочечников. Применяют в качестве второй линии гормональной терапии метастатического РПЖ на фоне прогрессирования процесса после проведения максимальной андрогенной блокады. Кетоконазол назначают внутрь в дозе 400 мг 3 раза в сутки.
Иммунотерапия рака простаты
Иммунная терапия рака предстательной железы активирует лимфоциты, способные уничтожить раковые клетки. Мишень — антигены, характерные для рака простаты. Это, прежде всего, PSA, а также простатическая фосфатаза и простатспецифический мембранный антиген (PSMA). При иммунологическом лечении злокачественных опухолей простаты применяются дендритно-клеточные вакцины, вакцины клеток всей опухоли, векторсвязанные вакцины и моноклональные антитела.
На сегодняшний день появились новые лекарственные средства, которые могут стать препаратами первой линии лечения данного заболевания. Абиратерон (Zytiga) — препарат, утверждённый в Израиле и предназначенный для лечения кастрат-резистентного рака предстательной железы. Проствак, как вакцина, стимулирует иммунитет для мобилизации организма на борьбу с раковыми клетками. Выживаемость пациентов с тяжёлыми формами рака простаты, принимающих проствак, повышается с 16-ти месяцев до 24-х. Алфарадин — радиофармпрепарат, выделяющий радиоактивные альфа-частицы, они локально воздействуют на метастазы. Деносумаб защищает кости при возникновении метастаз, препятствуя выводу кальция из костей, притормаживая развитие метастатического процесса в 5 раз эффективнее других препаратов. [14]
Химиотерапия рака простаты
На начальных этапах рака простаты химиотерапия малоэффективна. Это связано с тем, что злокачественные опухолевые клетки предстательной железы растут так же, как и здоровые. Цитостатики же действуют исключительно на быстрорастущие клеточные структуры. Чаще всего противоопухолевые препараты назначаются на III–IV стадии болезни — при больших размерах первичной опухоли, сильной боли, метастазах и наличии нескольких очагов в костной ткани.
Преимущество противоопухолевых химиопрепаратов — это возможность использовать их при агрессивных опухолях предстательной железы, которые уже дали метастазы и не могут быть удалены хирургически. В сочетании с операцией и гормональными препаратами химиотерапия позволяет стабилизировать или улучшить состояние пациента.
Химиотерапия заключается во внутривенном введении специальных химиотерапевтических средств. В среднем один цикл химиотерапии при раке простаты длится 1–4 недели. При раке предстательной железы применяется Доцетаксел с Гозерелином, Бусерелином и Трипторелином.
При неэффективности Доцетаксела или устойчивости к нему применяется Кабазитаксел (Джевтана). Результаты исследований показали, что этот химиопрепарат гораздо эффективнее Митоксантрона, который ранее выбирался для замены Доцетаксела.
Химиотерапевтические препараты останавливают деление злокачественных клеток, замедляя или полностью останавливая рост опухоли. В то же время эти препараты вызывают тяжёлые побочные эффекты, такие как:
- снижение уровня лейкоцитов и иммунитета;
- анемия, ухудшение свёртываемости крови и предрасположенность к кровотечениям;
- тошнота, рвота и диарея;
- стоматит и язвы в ротовой полости;
- ухудшение аппетита, вкусовые нарушения;
- выпадение волос;
- общая слабость и быстрая утомляемость;
- задержка жидкости и отёки;
- периферическая нейропатия.
Виротерапия
Вирусотерапия рака предстательной железы исследуется учёными и считается перспективным направлением [27] . Однако для лечения пациентов этот метод пока не используется.
Спасительная терапия
У всех пациентов с метастатическим процессом в костях, получающих терапию на основе доцетаксела, наблюдалось прогрессирование. В связи с этим были проведены многочисленные исследования, связанные с изучением роли спасительной терапии. Результаты этих исследований показали, что терапия кабазитакселом, интермиттирующая химиотерапия доцетакселом и молекулярно-направленная терапия — наиболее приемлемые режимы лечения. В настоящее время эти методики не рекомендуются в связи с малым количеством рандомизированных исследований.
Методы паллиативной терапии
- Терапия, направленная на лечение поражений костной системы при кастрационно-резистентном раке предстательной железы
У большинства пациентов с костно-распространённым раком предстательной железы с (КР РПЖ), костные метастазы сопровождаются выраженным болевым синдромом. Два радиоизотопа, Sr-89 и Sа-153, способны уменьшить или купировать боль в костях у 72 % пациентов. У больных с костными метастазами, которые сопровождаются болевым синдромом, применение Rа-233 оказалось весьма эффективным.
Осложнения, вызванные костными метастазами, выражаются в болевых ощущениях в костях, разрушении позвонков, деформирующих патологических переломах и компрессии спинного мозга. Ещё одна причина патологических переломов — остеопороз, поэтому необходимо проведение его профилактики.
Применение костного цемента — продуктивный метод лечения патологических переломов, который позволяет значительно уменьшить болевые ощущения и повысить качество жизни. При возникновении подозрения на существование компрессии спинного мозга необходимо как можно скорее назначить высокие дозы кортикостероидов и выполнить МРТ.
Бифосфонаты используются для торможения резорбции костной ткани. При применении золедроновой кислоты было отмечено увеличение времени до появления первого скелетного осложнения, что улучшало качество жизни пациентов. В настоящее время бифосфонаты показаны пациентам с КР РПЖ с костными метастазами для профилактики скелетных осложнений, хотя однозначного оптимального интервала между приёмами не существует (на данный момент он составляет 3 недели или менее).
Всегда стоит помнить о том, что у этих препаратов существуют побочные эффекты, в особенности у амино-бисфосфонатов (например, некроз верхней челюсти). Бисфосфонаты назначают на раннем этапе лечения КР РПЖ с клиническими проявлениями. При дополнительной системной терапии обнаруживают методы устранения возможных побочных эффектов — болевого синдрома, запора, отсутствия аппетита, тошноты, усталости, депрессии, которые развиваются при проведении паллиативного лечения. Терапия включает в себя паллиативную ДЛТ, кортизон, анальгетики и противорвотные средства.
- Ингибиторы лиганд RANK-рецептора-активатора ядерного фактора
Деносумаб — моноклональное антитело человека, направленное против рецептора-активатора ядерного фактора В-лиганда, является ключевым медиатором образования остеокластов (больших многоядерных клеток). У пациентов с КР РПЖ стадии М0 деносумаб привёл к увеличению показателя выживаемости без костного метастазирования по сравнению с плацебо. При проведении третьей фазы лечения было отмечено, что эффективность и безопасность деносумаба сопоставима с золедроновой кислотой у пациентов с метастатическим КР РПЖ. Деносумаб разрешён к применению Управлением по контролю качества пищевых продуктов и лекарственных средств США для профилактики скелетных осложнений у пациентов с костными метастазами, обусловленными наличием раковых опухолей.
После терапии доцетакселом, при прогрессии РПЖ рекомендовано применение кабазитаксела.
Рейтинг ведущих онкоцентров России:
- Российский онкологический научный центр им. Н.Н. Блохина РАМН, Москва.
- Городская клиническая больница имени С.П. Боткина, Москва.
- Клиническая больница № 85 ФМБА России, Москва.
- Онкологический центр ЛДЦ МИБС в Санкт-Петербурге.
- Клиника «К+31», Москва.
- Лечебно-диагностический центр (ЛДЦ) «ПАТЕРО КЛИНИК», Москва.
- Клинический госпиталь на Яузе, Москва.
Рейтинг ведущих зарубежных клиник, специализирующихся на лечении рака предстательной железы:
- Университетская клиника Кёльна.
- Университетская клиника «Рехтс дер изар», Мюнхен.
- Клиника «Вивантес Нойкёльн», Берлин.
- Академическая клиника «Асклепиос Бармбек», Гамбург.
- Медицинский центр «Рамбам», Хайфа (Израиль).
- Клиника «Вивантес Ам Урбен» Берлин.
- Клиника «Ленокс-Хилл», Нью – Йорк.
- Урологический центр в Алабаме (США).
- Бостонский медицинский центр (США).
- Клиника «Хирсланден перманенс» (Швейцария).
Далее рассмотрим осложнения различных методов лечения РПЖ.
Осложнения радикальной простатэктомии:
- смертность — 0-1,3%;
- травма прямой кишки — 0,5-2,8%;
- повреждение мочеточника — 0,3%;
- тромбоз вен нижних конечностей — 1,2-1,5%;
- тромбоэмболия лёгочной артерии — 0,6-1,4%;
- острый инфаркт миокарда — 0,4-0,7%;
- недержание мочи — 0,8-12%.
Нарушение эрекции может развиваться у всех больных после выполнения радикальной простатэктомии, не применяя при этом нервосберегающую технику. Для того, чтобы сохранить эректильную функцию, разработана техника операции, позволяющая сохранить кавернозные нервно-сосудистые пучки.
Осложнения дистанционной лучевой терапии:
- недержание мочи — 0,2-1,5 %;
- эректильная дисфункция — 54-66%;
- диарея — 1,4-7,7%;
- стриктуры уретры — 2,6-11,0%;
- гематурия — 2,5-10,0%:
- ректальное кровотечение — 2,5-14,2%.
Осложнения эстрогенотерапии:
- тромбоэмболические осложнения;
- сердечно-сосудистые осложнения;
- отёки;
- эректильная дисфункция;
- гинекомастия и болезненность грудных желёз;
- гастрологические расстройства (боль, тошнота, рвота). [26]
Прогноз. Профилактика
Классификация прогностических факторов риска по DAmico
По этой классификации учитывается вероятность прогрессирования рака на начальных стадиях до проявления клинических симптомов и летального исхода, а также риск возникновения рецидивов после локализованного лечения рака.
По классификации рака предстательной железы DAmico, пациентов относят к одной из трёх групп прогрессирования болезни: низкой, средней или высокой. Для оценки берутся следующие показатели:
- классификация рака по системе ТNM, а именно показатель Т — распространенность первичной опухоли;
- степень рака простаты по шкале Глисона;
- уровень простат-специфического антигена в крови (ПСА).
В группу низкого риска относятся пациенты, у которых уровень ПСА ≤ 10 нг/мл, шкала Глисона ≤ 6 баллов, клиническая стадия — T1-2a. К группе среднего риска относят пациентов, у которых уровень ПСА 10-20 нг/мл, шкала Глисона — 7 баллов, клиническая стадия — T2b. К группе высокого риска относят пациентов, у которых уровень ПСА > 20 нг/мл, шкала Глисона ≥ 8 баллов, клиническая стадия — T2c-3a.
Прогнозирование по таблицам Алана Партина (номограммам)
Таблицы Партина представляют собой шкалы, в которых учитываются математические модели, высчитанные на основании значения уровня ПСА, баллов по шкале Глисона и клинической стадии рака простаты по классификации по системе ТNM. График Партина позволяет сделать прогноз дальнейшей прогрессии заболевания. Номограммы составлялись на основании исследования данных о мужчинах, которые проходили лечение рака предстательной железы. Таким образом, базируясь на этих данных, были составлены таблицы, которые делятся следующим образом:
- степень рака простаты — от Т1с до Т2с;
- по уровню ПСА в крови выделяют следующие категории: 0-10 нг/мл и более 10,0 нг/мл;
- баллы шкалы Глисона делятся на 3 категории: 2-4, 5-6 или 8-10.
Вот так выглядят модифицированные номограммы Партина, по которым можно определить вероятность дальнейшего прогрессирования рака простаты:
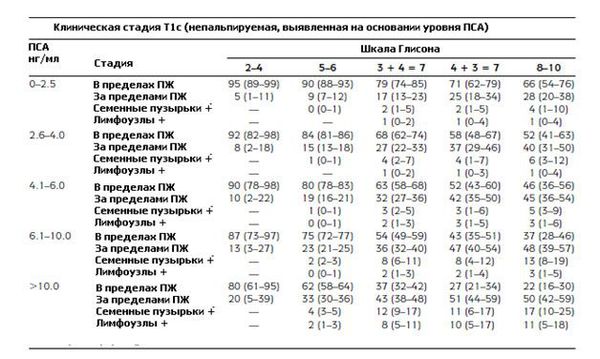
Прогноз выживаемости при раке простаты
Прогноз определяется стадией, на которой выявлен рак, а также степенью дифференцировки опухоли и уровнем простатического специфического антигена (ПСА). Пятилетняя выживаемость без рецидивов пациентов с I–II стадией после радикальной простатэктомии и лучевой терапии составляет 70–90 %, общая выживаемость — 85–97 %. При выявлении рака на стадии метастазов средний период до прогрессирования болезни на фоне лечения составляет 2–3 года [28] .
Профилактика
— Ежегодное урологическое обследование после 50 лет, а мужчин с генетической предрасположенностью — после 40 лет по стандартной программе обследования, включающее:
- анализ крови на ПСА, при необходимости — анализ на ПСА-3 в моче;
- пальцевое ректальное исследование простаты;
- ТРУЗИ.
— Правильное сбалансированное питание:
- с содержанием веществ, способных замедлить рак предстательной железы: прежде всего ликопена (содержится в арбузе, томатах, розовых грейпфрутах), катехина (содержится в зелёном чае) и фитоэстрогенов (имеются в чечевице, чесноке, горохе, шишках хмеля, календуле и бобовых растениях);
- употребление свежих овощей и фруктов, богатых клетчаткой;
- минимизация потребления жиров животного происхождения;
- имеет значение употребление свежевыжатых соков: морковного, свекольного, гранатового, яблочного и апельсинового;
- достаточное потребление хлеба с отрубями и из муки грубого помола;
- употребление риса, пшеницы и других круп, бобовых и сои;
- приём растительных масел первого «холодного» отжима (оливковое, кедровое, грецкого ореха и др.).
— Отказ от вредных привычек: курения, алкоголя, наркотиков.
— Физическая активность.
Одним из основных факторов, способствующих развитию болезни, является образ жизни. Умеренные физические нагрузки на свежем воздухе — бег трусцой, ходьба, плавание, езда на велосипеде — улучшают иммунитет, устраняют гиподинамию как фактор развития рака простаты, усиливают кровообращение малого таза мужчины.
Список литературы
- Greenlee R.T., HillHarmon M. B., Murray T. et al. Cancer statistics, 2001 // CA. Cancer. J. Clin. — 2001. — Vol. 51. — Р. 15–36.
- Ries L.A. G., Kosary C.L., Hankey B.F. et al. SEER Cancer Statistics Review 1973–1995. Bethesda, MD. — National Cancer Institute, 1998.
- Andriole G.L., Grubb R.L., Buys S.S. et al. Mortality results from a random- ized prostatecancer screening trial. N Engl J Med 2009;360:1310.
- Quinn M., Babb P. Patterns and trends in prostate cancer incidence, survival, prevalence and mortality. Part I: international comparisons // BJU Int. — 2002. — Jul. — Vol. 90. — № 2. — Р. 162–173.
- Stanford J.L., Stephenson R.A., Coyle L.M. et al. Prostate Cancer Trends 1973–1995,SEER Program, National Cancer Institute, NIH Pub., N 99–4543, Bethesda, MD, 1999.
- Debruyne F. Hormonal therapy of prostate cancer // Semin. Urol. Oncol. — 2002. — Vol. 3. — Suppl. 1. — Р. 4–9.
- Chang A., Yeap B., Davis T. et al. Doubleblind randomized study of primary hormonal treatment of stage D2 prostate carcinoma: flutamide versus diethylstilbestrol // J. Clin. Oncol. — 1996. — Vol. 14. — Р. 2250–2257.
- Albertsen P.C., Hanley J.A., Gleason D.F., Barry M.J. Competing risk analysis of men aged 55 to 74 years at diagnosis managed conservatively for clinically localized prostate cancer // JAMA.— 1998. — Vol. 280. — Р. 975–980.
- Allepus Losa C.A., Sana Velez J.I., Gil Sanz M.J. et al. Seminal vesical biopsy in prostate cancer staging // J. Urol. — 1995. — Vol. 154. — Р. 1407–1411.
- Andersson S.B., Gunnarsson P.O., Nilsson T. et al. Metabolism of estramustine phosphaye (Estracyt) in patients with prostatic carcinoma // Eur.J. Drug. Metab. Pharmacokinet. — 1981. — Vol. 6. — Р. 149–154.
- Chodak G.W. Early detection and screening for prostatic cancer // Urology. — 1989. — V. 34. — Suppl. 4. — Р. 10–12.
- Pedersen K.V., Carlson P., Varenhorst E. et al. Screening for carcinoma of the prostate by digital rectal examination in a randomly selected population // B.M. J. — 1990. — Vol. 300. — Р. 1041–1044.
- Oesterling J.E., Jacobsen S.J., Chute C.G. et al. Serum prostate specifi c antigen in a community based population of healthy men: establishment of age specific reference ranges // JAMA. — 1993. — Vol. 270. — Р. 860–864.
- N. Mottet (chair), P.J. Bastian, J. Bellmunt, R.C.N. van den Bergh, M. Bolla, N.J. van Casteren, P. Cornford, S. Joniau, M.D. Mason, V. Matveev, T.H. van der Kwast, H. van der Poel, O. Rouvière, T. Wiegel. Guidelines on Prostate Cancer // European Association of Urology. — 2014. — P. 184–355.
- Benson M.C., Olsson C.A. Prostate specific antigen density — roles in patient evaluation and management // Cancer. — 1994. — Vol. 74. — Р. 1667–1673.
- Ellis W.J., Chetner M.Р., Preston S.D., Brawer M.K. Diagnosis of prostatecarcinoma: the yield of serum prostate specific antigen, digital restal examination, and transrectal ultrasonography // J. Urol. — 1994. — Vol. 152. — Р. 1520–1525.
- Mettlin C., Murphy G.P., Babaian R.J. et al. The results of a five-year early prostate cancer detection intervention. Investigators of the American Cancer Society National Prostate Cancer Detection Project // Cancer. — 1996. — Vol. 77. — № 1. — Р. 150–159.
- Schnall M.D., Imai Y., Tomaszewski J. et al. Prostate cancer: local staging with endorectal surface coil MR imaging // Radiology. — 1991. — Vol. 178. — Р. 797–802.
- Platt J.F., Bree R.L., Schwab R.E. The accuracy of CT in the staging of carcinoma of the prostate // Am.J. Roentgenol. — 1987. — Vol. 149. — Р. 315–318.
- Oesterling J.E. PSA leads the way for detecting and following prostate cancer // Contemp. Urol. — 1993. — Vol. 5. — Р. 60–81.
- Kirby R.S., Christmas T.J., Brawer M.K. Treatment of localized prostatecancer: radical prostatectomy and radiation therapy. In: Prostate Cancer (2nd ed.). — Mosby, London, 2001. — P. 115–138.
- Rassweiler J., Frede T. Robotics, telesurgery and telementoring — their position in modern urological laparoscopy.
- Shipley W.U., Zietman A.L., Hanks G.E. et al. Treatment related sequelae following external beam radiation for prostate cancer: A review with an update in patients with stages T1 and T2 tumor // J. Urol. — 1994. — Vol. 152. — Р. 1799–1805.
- Scardino R.T., Abbas F., Bolla M. et al. Management of Localized and Regional Diseases. In: Prostate Cancer. L. Denis, G. Bartsch, S. Khoury et al. (eds.). — 2003. — P. 217–249.
- Kuhn J.M., Billebaud T., Navratil H. et al. Prevention of the transient adverse effects of agonadotropin releasing hormone analogue (buserelin) in metastaticprostatic carcinoma by administration of an antiandrogen (nilutamide) // N.Eng. J. Med. — 1989. — Vol. 321. — Р. 413–418.
- Zlotta A.R., Djavan B., Marberger M., Schulman C.C. Prostate specifi c antigen of the transition zone: a new parameter for prostate cancer prediction // J. Urol. — 1997. — Vol. 157. — Р. 1315–1321.
- Fukuhara H., Homma Y., Todo T. Oncolytic virus therapy for prostate cancer // Int J Urol. — 2010. — № 1. — Р. 20–30. ссылка
- Министерство здравоохранения РФ. Рак предстательной железы: клинические рекомендации. — М., 2020. — 142 с.
Рак простаты

Рак простаты, или рак предстательной железы (РПЖ) – это стремительно растущее онкологическое заболевание пожилых мужчин, прирост которого, по некоторым данным, составил более 500% (!) по сравнению с началом 90-х годов. Такой всплеск, в первую очередь, связан с повсеместным введением программы раннего выявления данной патологии.
С другой стороны, рак предстательной железы имеет явную корреляцию с возрастом: риск появления злокачественной опухоли в предстательной железе существенно выше у мужчин старше 65 лет по сравнению с мужчинами 50-летнего возраста. Учитывая, что продолжительность жизни, особенно в развитых странах, заметно увеличивается, данный фактор можно также считать причиной роста заболеваемости раком простаты.
Рак простаты занимает первое место среди всех злокачественных новообразований у мужского населения, поэтому сегодня уделяется огромное внимание вопросам лечения онкологии предстательной железы: пересматриваются хирургические подходы, развиваются малоинвазивные техники операций на опухолях, совершенствуется лучевая терапия (в том числе и контактная брахитерапия), разрабатываются новые препараты для лекарственного лечения.
Развивается рак простаты из-за мутаций в клетках предстательной железы. Эти мутации могут провоцировать бесконтрольное деление и образование опухоли.
Причины рака простаты
Причины возникновения мутаций в клетках, которые вызывают рак простаты и другие онкологические заболевания еще не выяснены до конца. Но есть некоторые факторы риска, которые повышают вероятность развития опухоли.
Основной причиной рака простаты можно назвать возраст. Чем больше продолжительность жизни мужчины, тем дольше андрогены – мужские половые гормоны – оказывают стимулирующий эффект на ткань предстательной железы. Именно это, по современным данным, предрасполагает к развитию злокачественной опухоли в простате, на этой же теории построена и система лекарственного лечения, основное направление которой – гормонотерапия.
Способствовать появлению и росту злокачественных клеток в простате могут также:
- избыточная масса тела;
- гиперплазия предстательной железы, хронический простатит и другие воспалительные заболевания и состояния предстательной железы;
- травмы;
- аденомы предстательной железы;
- «жирная» диета.
Большую роль в возникновении рака предстательной железы играет наследственность. Установлено, что злокачественная опухоль гораздо чаще встречается у мужчин, ближайшим родственникам которых также был установлен диагноз РПЖ.
Стадии рака простаты
- 1 стадия – опухоль не агрессивна, имеет маленькие размеры и находится в пределах предстательной железы;
- 2 стадия – опухоль увеличена в размерах, но все еще поражает только ткани предстательной железы;
- 3 стадия – рак простаты начинает выходить за пределы предстательной железы и поражать семенные пузырьки и другие соседние ткани и органы;
- 4 стадия – злокачественная опухоль захватывает мочевой пузырь, поражает лимфатические узлы и дает метастазы в другие органы (например, легкие) и ткани (костную).
Рак простаты терминальной четвертой стадии плохо поддается лечению и имеет неблагоприятный прогноз.
Виды рака простаты
Самый распространенный рак предстательной железы – это аденокарцинома. Эта опухоль развивается из железистых клеток органа. Встречаются также более редкие формы рака, такие как нейроэндокринный, мелкоклеточный рак, саркома, переходно-клеточный рак простаты.
Профилактика рака простаты
Способы профилактики этого онкологического заболевания пока точно не определены. Есть сведения, что риск рака предстательной железы снижает употребление томатов. Но этот вопрос исследован недостаточно. Однако улучшить прогноз и облегчить лечение опухоли, помогает регулярное обследование у уролога, чтобы обнаружить рак простаты на ранних стадиях. Самый доступный тест – анализ на простатспецифический антиген (ПСА). Это онкомаркер, который попадает в кровь из-за повреждений кровеносных сосудов предстательной железы и в норме не должен превышать 4 нг/мл. Более высокие значения могут свидетельствовать как о злокачественном процессе в этом органе, так и о других заболеваниях предстательной железы (например, об аденоме).
Симптомы рака простаты
Трудности раннего выявления рака простаты связаны с его бессимптомным течением на ранних стадиях. Появление клинических признаков заболевания, как правило, указывает на запущенный процесс. Все признаки рака предстательной железы можно разделить на две группы: симптомы местной опухоли и симптомы метастазов. К сожалению, они очень похожи на симптомы других заболеваний мужской мочеполовой системы.
Пациенты с раком простаты могут испытывать следующее:
- затруднения мочеиспускания;
- частое мочеиспускание небольшими порциями (особенно по ночам);
- жжение и боль при мочеиспускании;
- дискомфорт в области малого таза;
- кровь в моче.
Эти симптомы чаще являются признаками гиперплазии предстательной железы. Она доброкачественная. Но чтобы исключить риск онкологии, нужно обязательно обследоваться у врача.
В некоторых случаях пациент больше страдает от проявлений метастазов рака простаты, чем от основных симптомов заболевания, например на поздних стадиях могут появиться:
- боли в костях, пораженных метастазами (чаще поясница и кости таза);
- боль при сдавлении спинного мозга;
- нарушение работы мочевого пузыря;
- нарушение функций прямой кишки;
- отеки ног из-за сдавления вен и поражения лимфоузлов;
- увеличенные регионарные лимфоузлы;
- боль в пояснице;
- похудение, усталость и сонливость, кишечное кровотечение.
Диагностика рака простаты
Полностью излечить заболевание можно только на ранних стадиях рака простаты, пока опухоль еще небольшая. Поэтому очень важно регулярно проходить обследование.
Для выявления онкологии используют следующие методы:
- пальцевое ректальное обследование (ПРО) – прощупывание через прямую кишку предстательной железы, которое позволяет обнаружить уплотнения;
- анализ крови на наличие простатического специфического антигена (ПСА);
- ультразвуковое исследование предстательной железы при помощи ректального датчика (ТРУЗИ), который вводят в прямую кишку, с возможной биопсией опухоли;
- колоноскопия;
- компьютерная и магнитно-резонансная томография малого таза для оценки степени распространения рака предстательной железы на семенные пузырьки и другие рядом расположенные ткани.
Для верификации диагноза выполняется трепан-биопсия предстательной железы. Для исключения отдаленных метастазов делают УЗИ брюшной полости, сканирование скелета (остеосцинтиграфию), КТ или МРТ интересующей зоны, рентгенологическое исследование легких.
Анализ крови на уровень ПСА используется широко, но дает неоднозначные результаты. В норме этот уровень составляет 4 нг/мл. Повышение этого уровня до 10 нг/мл расценивается как 25% вероятность наличия рака простаты. А свыше 10 нг/мл – 50% вероятность. Однако в некоторых случаях и при уровне ПСА ниже 4 нг/мл выявляется рак. Но после того как диагноз рак простаты поставлен, анализы на ПСА можно использовать для контроля эффективности лечения и оценки степени распространения онкологии. Пока первым и основным методом диагностики рака предстательной железы является пальцевое ректальное исследование.
Процедура ТРУЗИ позволяет не только осуществить диагностику и сделать биопсию предстательной железы, но и проконтролировать проведение других методов лечения рака простаты, таких как брахитерапия или криотерапия.
Биопсия опухолевых клеток предстательной железы – это наиболее точный и надежный способ поставить окончательный диагноз. Для забора раковых клеток может назначаться пункционная биопсия предстательной железы, биопсия под контролем УЗИ с введением датчика в прямую кишку и другие методы. Биоматериал потом подвергается гистологическому исследованию в лаборатории.
Во время диагностики стоит задача выяснить тип опухоли, стадию рака предстательной железы и определить схему лечения. Если опухоль не успела распространиться за пределы простаты, возможно хирургическое удаление предстательной железы, если же имеются метастазы, то показана лекарственная терапия.
В нашей клинике для диагностики рака простаты используется современное оборудование для аппаратных обследований и лабораторных анализов. Во время биопсии применяется эффективное обезболивание и отдается предпочтение наиболее безопасным и наименее инвазивным способам диагностики рака предстательной железы.
Лечение рака простаты
Выбор метода лечения при раке простаты зависит от стадии заболевания, размера опухоли, а также от наличия сопутствующих возрастных заболеваний, которые могут повлиять на возможность проведения хирургического лечения. При лечении рака простаты применяется один из следующих способов либо их сочетание:
- Хирургия. При раке простаты с помощью хирургического вмешательства удаляют саму предстательную железу и ткани рядом с ней. Операцию выполняют традиционным способом (открытым), методом лапароскопии (щадящая операция) или с применением роботизированной системы «Да Винчи». Ранние формы рака предстательной железы подлежат хирургическому лечению. Хирурги клиники онкологии К+31 владеют современными операционными методиками, которые позволяют выполнять нервосберегающие операции. В клинике внедряются малоинвазивные технологии удаления простаты, после которых пациенты практически не нуждаются в реабилитационных мероприятиях.
- Лучевая терапия. Применяют в случаях, когда операция противопоказана, а также в сочетании с гормональной терапией, в лечении рецидивов рака предстательной железы и в качестве паллиативной терапии. Лучевая терапия может быть дистанционной и контактной. Современные методы дистанционной лучевой терапии:
- трехмерная конформная лучевая терапия – заключается в направленном воздействии с нескольких точек на опухоль, при этом здоровые ткани подвергаются минимальному воздействию;
- стереотаксическая терапия – метод, при котором аппарат концентрированно подает дозу облучения к опухоли предстательной железы, что позволяет сократить курс до дней вместо недель.
Метастатический рак простаты в некоторых случаях тоже поддается лечению. Лучевая терапия, химиотерапия и другие способы направлены на замедление деления раковых клеток, их разрушение, даже если они находятся в костях или легких.
Рак простаты на I стадии развития лечат с помощью лучевой терапии или проводят радикальную простатэктомию (удаление предстательной железы).
На II стадии рак простаты могут лечить хирургическими методами (простатэктомия), лучевой терапией, брахитерапией или сочетанием последних двух.
Лечение рака простаты на III стадии, когда злокачественная опухоль распространилась на соседние ткани, но еще не поразила мочевой пузырь и прямую кишку, нередко заключается в наблюдении за динамикой опухоли и контроле заболевания. Но могут применяться такие методы лечения, как гормональная терапия, химиотерапия, лучевая терапия, радикальная простатэктомия, трансуретральная резекция предстательной железы, а также различные комбинации этих методов.
Рак предстательной железы 4 стадии лечится теми же методами, что и опухоли 3 стадии. В основном это паллиативное лечение для уменьшения симптомов, снижения боли и продления жизни пациента.
Прогнозы при раке простаты
Пятилетняя выживаемость при раке простаты 1, 2 и даже 3 стадии – практически 100%. Но на 4 стадии рака предстательной железы прогнозы резко падают до 30% и менее. Правда в этом случае существуют достаточно эффективные методы продления жизни пациента даже с метастазами рака простаты в других органах и тканях.
Десятилетняя выживаемость после лечения рака простаты (а именно – удаления предстательной железы) на любой стадии составляет 98%, а 15-летняя – 96%. В большинстве случаев после лечения не наблюдается рецидивов.
Реабилитация после операции при раке предстательной железы
Восстановление после хирургического лечения рака простаты может занять всего несколько недель. Во время операции ставится катетер в мочевом пузыре, который извлекается через пару недель. А выписывают пациента из больницы уже через несколько дней. Чтобы предотвратить рецидив после операции при раке простаты пациенты должны регулярно обследоваться и сдавать анализы на ПСА.
После хирургического лечения рака простаты могут быть некоторые последствия, например, нарушение эрекции и бесплодие, недержание мочи, уменьшение длины пениса, паховая грыжа. Но есть способы борьбы с этими эффектами.
Недержание мочи после операции при раке простаты может быть из-за повреждения сфинктера мочевого пузыря, и во время напряжения (кашля, чихания, физических нагрузок) происходит утечка. В большинстве случаев это проходит со временем. Помочь процессу восстановления могут упражнения Кегеля, мочеприемники, хирургические методы, лекарственные препараты.
Эректильная дисфункция как побочный эффект хирургического лечения рака простаты лечится с помощью лекарств, имплантатов или специальных вакуумных устройств.
Лечение рака простаты в нашей клинике «К+31»
Для лечения рака простаты в нашей клинике собирается группа специалистов разного профиля, которые со всех сторон рассматривают проблему, учитывают состояние пациента, его особенности. Выбор метода лечения делается в сторону наиболее эффективной и безопасной в данном конкретном случае терапии.
Врачи нашей клиники занимаются также лечением рака молочной железы, рака желудка, рака легких, рака печени, рака матки, лимфомы, меланомы, а также новообразований любой этиологии и локализации. В своей клинической практике они используют только проверенные методы диагностики пациентов и эффективные техники лечения больных с минимум осложнений.
Звоните нам по телефону, чтобы записаться на консультацию или делайте это онлайн, прямо на нашем сайте.
Источник https://inuclear.ru/zabolevanija/rak-prostaty/
Источник https://probolezny.ru/rak-predstatelnoy-zhelezy/
Источник https://www.k31.ru/service/onkology/rak-predstatelnoy-zhelezy.html